
Wetenschap
Zijn de elektronenstructuren van boor en aluminium vergelijkbaar?
overeenkomsten:
* valentie -elektronen: Zowel Boron als Aluminium hebben drie valentie -elektronen in hun buitenste schaal. Dit is de belangrijkste reden waarom hun chemische gedrag vergelijkbaar is.
* Elektronenconfiguratie: Ze hebben allebei een configuratie die eindigt in ns²np¹ . De elektronenconfiguratie van Boron is 1S²2S²2P¹, terwijl aluminium's 1S²2S²2P⁶3S²3P¹ is.
Verschillen:
* Aantal elektronenschalen: Boron heeft slechts twee elektronenschalen, terwijl aluminium er drie heeft.
* Afscherming: De buitenste valentie -elektronen in aluminium ervaren meer afscherming van de binnenste elektronen, waardoor ze iets minder reactief zijn dan boor.
* Grootte: Aluminiumatomen zijn aanzienlijk groter dan booratomen vanwege de aanwezigheid van een extra elektronenschil.
gevolgen van overeenkomsten en verschillen:
* Zowel boor- als aluminium vormen verbindingen met een +3 oxidatietoestand, vanwege hun neiging om hun drie valentie -elektronen te verliezen.
* Boron is meestal covalenter in zijn binding vanwege zijn kleinere omvang en minder afscherming.
* Aluminium is meer metaalachtig van aard vanwege de grotere omvang en een grotere afscherming.
Samenvattend:
Terwijl boor- en aluminium vergelijkbare elektronenconfiguraties delen en een neiging om +3 kationen te vormen, leiden hun verschillen in grootte, afscherming en het aantal elektronenschalen tot enkele variaties in hun chemische gedrag.
 Welk element wordt meestal gevonden als onderdeel van een verbinding met een ander en waarom?
Welk element wordt meestal gevonden als onderdeel van een verbinding met een ander en waarom?  Wat is het gebruik van mierenzuur bij de synthese van benzimidazool?
Wat is het gebruik van mierenzuur bij de synthese van benzimidazool?  Kankerbewegingen in kaart brengen
Kankerbewegingen in kaart brengen Afval CO2 wordt omgezet in ingrediënten voor brandstof, plastic en zelfs voedsel
Afval CO2 wordt omgezet in ingrediënten voor brandstof, plastic en zelfs voedsel Studie onthult een unieke manier van celmigratie op zachte visco-elastische oppervlakken
Studie onthult een unieke manier van celmigratie op zachte visco-elastische oppervlakken
 Opdoemende klimaateffecten:10 afhaalrestaurants uit het ontwerp-VN-rapport
Opdoemende klimaateffecten:10 afhaalrestaurants uit het ontwerp-VN-rapport NASA ziet ontwikkeling van tropische cycloon 3S langs de kust van West-Australië
NASA ziet ontwikkeling van tropische cycloon 3S langs de kust van West-Australië Begrijpen hoe planten zonlicht gebruiken
Begrijpen hoe planten zonlicht gebruiken  Een nieuwe reeks doelen om de natuurlijke wereld te beschermen
Een nieuwe reeks doelen om de natuurlijke wereld te beschermen Koolstofuitstoot en El Nino zorgen ervoor dat de oceanen recordtemperaturen bereiken
Koolstofuitstoot en El Nino zorgen ervoor dat de oceanen recordtemperaturen bereiken
Hoofdlijnen
- De ontdekking van een atypische hitteschokfactor, HSF5, die betrokken is bij meiotische mechanismen, heeft implicaties voor mannelijke onvruchtbaarheid
- Waarom het een goed idee is om met je dronken oom over politiek te praten
- Heeft die astroloog u goed gelezen? Dat is het Barnum-effect
- Hoe je hersenen werken
- Waarom vormen wetenschappers een hypothese?
- Een nieuw venster op planten uit het verleden
- De warmere stroomtemperaturen in het afgebrande stroomgebied van Oregon hebben niet geleid tot minder forel
- Een gezondheidscentrum voor jonge zalm
- Wat wordt er weergegeven als geen enkele kopie van een allel de expressie maskeert?
- Nieuwe materialen maken met AI

- De witste verf is hier - en het is de coolste. Letterlijk.
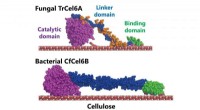
- Bacterieel cellulose-afbraaksysteem kan de productie van biobrandstoffen stimuleren
- Nieuwe studie stelt ongebruikelijke forensische onderzoekstechniek op de proef

- Simulaties maken het mogelijk om stereochemie te kiezen voor je eigen avontuur

 Vroege Pacific Islanders waren misschien de eerste natuurbeschermers
Vroege Pacific Islanders waren misschien de eerste natuurbeschermers Welk percentage van de sterren die zichtbaar zijn vanaf de aarde is te zien, evenaar?
Welk percentage van de sterren die zichtbaar zijn vanaf de aarde is te zien, evenaar?  Team laat zien hoe de honingbij sommige synthetische pesticiden verdraagt
Team laat zien hoe de honingbij sommige synthetische pesticiden verdraagt  Wat is een blockchain-token?
Wat is een blockchain-token?  Lekima wordt Supertyfoon, op weg naar Oost-China
Lekima wordt Supertyfoon, op weg naar Oost-China Wat zijn de twee prokaryotische rijken?
Wat zijn de twee prokaryotische rijken?  King of Cups:ontgrendel de diepten van emotioneel meesterschap
King of Cups:ontgrendel de diepten van emotioneel meesterschap  Elektrische auto's beter voor klimaat in 95% van de wereld
Elektrische auto's beter voor klimaat in 95% van de wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

