
Wetenschap
Hoeveel extra elektronen zitten er in de Lewis-structuur van fosfaation PO 4 3?
Zo bepaal je de extra elektronen:
Fosforatoom:Fosfor (P) heeft vijf valentie-elektronen.
Zuurstofatomen:Elk zuurstofatoom (O) heeft zes valentie-elektronen.
Negatieve lading:Het fosfaation heeft een 3-negatieve lading.
Extra elektronen berekenen:
Neutraal molecuul (PO₄):
- Fosfor:5 valentie-elektronen
- Zuurstof (4 atomen):4 x 6 =24 valentie-elektronen
Totale valentie-elektronen in neutrale PO₄:5 + 24 =29 elektronen
Fosfaat-ion (PO₄³⁻):
- Fosfor:5 valentie-elektronen
- Zuurstof (4 atomen):4 x 6 =24 valentie-elektronen
- Negatieve lading:3 extra elektronen (van de 3-lading)
Totale valentie-elektronen in PO₄³⁻:5 + 24 + 3 =32 elektronen
Extra elektronen:
Het verschil tussen de valentie-elektronen in het fosfaation (32) en het neutrale molecuul (29) vertegenwoordigt de extra elektronen.
32 valentie-elektronen (PO₄³⁻) - 29 valentie-elektronen (PO₄) =3 extra elektronen
Daarom heeft de Lewis-structuur van fosfaation (PO₄³⁻) drie extra elektronen vergeleken met het neutrale molecuul. Deze extra elektronen worden doorgaans weergegeven als negatieve ladingen rond de zuurstofatomen in de Lewis-structuur.
 Hoe zuurdesembrood werkt
Hoe zuurdesembrood werkt  Hoe de steno te schrijven Elektronconfiguratie voor Lead
Hoe de steno te schrijven Elektronconfiguratie voor Lead Onderzoekers ontwikkelen biomimetische-foto-gekoppelde katalyse voor de productie van H₂O₂
Onderzoekers ontwikkelen biomimetische-foto-gekoppelde katalyse voor de productie van H₂O₂  Wat is het proces waarbij ammoniumchloride en natriumchloride worden gescheiden?
Wat is het proces waarbij ammoniumchloride en natriumchloride worden gescheiden?  Unboil een eiermachine zorgt voor een verbeterde bacteriedetector
Unboil een eiermachine zorgt voor een verbeterde bacteriedetector
 Studie suggereert een grote toename van Arctische neerslag in de komende eeuw, veel van het regen
Studie suggereert een grote toename van Arctische neerslag in de komende eeuw, veel van het regen Op oceanen gebaseerde acties kunnen hiaten in de mitigatie van klimaatverandering dichten
Op oceanen gebaseerde acties kunnen hiaten in de mitigatie van klimaatverandering dichten NASA analyseert nieuwe tropische depressie in het oosten van de Stille Oceaan 7E
NASA analyseert nieuwe tropische depressie in het oosten van de Stille Oceaan 7E Klimaatverandering, vervuiling en verstedelijking bedreigen het water in Canada
Klimaatverandering, vervuiling en verstedelijking bedreigen het water in Canada Hoe bosbranden de klimaatverandering beïnvloeden - en vice versa
Hoe bosbranden de klimaatverandering beïnvloeden - en vice versa
Hoofdlijnen
- Hoe zijn fytoplankton reproductie?
- Een 3D-plantencel maken met huishoudelijke materialen
- Hoeveelheid water in stamcellen kan zijn lot bepalen als vet of bot
- Welke soorten cellen zijn bacteriën?
- Vertonen organismen die zijn geproduceerd als resultaat van binaire splijting een grote genetische variatie?
- Wat eten orka's in het noordpoolgebied?
- Hoe ontsnappen Mexicaanse grotvissen aan roofdieren?
- Door wetenschap ondersteunde manieren om een nieuwe studie te starten
- Video:Waarom hebben we nog geen synthetisch bloed?
- Onderzoekers onderzoeken ontstekingsremmende activiteit van curcumine

- Monitoring van de lichaamsvetverbranding door ademmonsters te nemen

- Ingenieurs bouwen chemisch aangedreven wielen die veranderen in tandwielen om mechanisch werk uit te voeren

- Dit computerprogramma maakt farmaceutische patenten luchtdicht
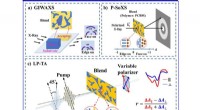
- Moleculaire oriëntatie onderzoeken door polarisatie-selectieve transiënte absorptiespectroscopie
 PAINS-killer:studie vindt ernstige problemen met populaire tool voor drugsscreening
PAINS-killer:studie vindt ernstige problemen met populaire tool voor drugsscreening Waarom oorlog een mannenspel is
Waarom oorlog een mannenspel is Hoe Pyramid Piramide te maken Math
Hoe Pyramid Piramide te maken Math Uw vergeten digitale voetafdrukken kunnen uw kansen op een baan schaden:hoe u dit opruimt
Uw vergeten digitale voetafdrukken kunnen uw kansen op een baan schaden:hoe u dit opruimt Rocketlab heeft deze engine naar de ruimte gestuurd en vervolgens opgehaald:een nieuwe test toont aan dat hij nog steeds goed werkt
Rocketlab heeft deze engine naar de ruimte gestuurd en vervolgens opgehaald:een nieuwe test toont aan dat hij nog steeds goed werkt CEO Musk:Tesla bereikt wekelijks doel om er 5 te maken 000 modellen 3s
CEO Musk:Tesla bereikt wekelijks doel om er 5 te maken 000 modellen 3s Kan een cent die van een gebouw is gevallen dodelijk zijn?
Kan een cent die van een gebouw is gevallen dodelijk zijn?  Die hechte gemeenschappen van vroeger hebben nooit bestaan
Die hechte gemeenschappen van vroeger hebben nooit bestaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

