
Wetenschap
Hoe varieert de viscositeit van vloeistoffen met de druk?
De omgekeerde relatie tussen viscositeit en druk kan worden verklaard door de moleculaire structuur van vloeistoffen. Vloeistoffen bestaan uit moleculen die bij elkaar worden gehouden door intermoleculaire krachten, zoals van der Waals-krachten, waterstofbruggen of ionische bindingen. Wanneer er druk wordt uitgeoefend op een vloeistof, worden de intermoleculaire krachten tussen de moleculen sterker, waardoor ze dichter bij elkaar komen te staan en de beschikbare ruimte om langs elkaar te bewegen kleiner wordt. Dit resulteert in een afname van de viscositeit van de vloeistof.
De snelheid waarmee de viscositeit afneemt bij toenemende druk varieert afhankelijk van het type vloeistof en de temperatuur. Voor de meeste vloeistoffen is de afname van de viscositeit bij druk groter bij lagere temperaturen. Dit komt omdat de intermoleculaire krachten tussen de moleculen sterker zijn bij lagere temperaturen, waardoor ze beter bestand zijn tegen de effecten van druk.
Samenvattend neemt de viscositeit van vloeistoffen over het algemeen af bij toenemende druk als gevolg van de dichtere pakking van moleculen en verminderde weerstand tegen stroming. De snelheid waarmee de viscositeit afneemt met druk hangt echter af van de specifieke vloeistof en de temperatuur.
 Cuba telt de kosten van dodelijke orkaan Irma
Cuba telt de kosten van dodelijke orkaan Irma Australië begint op lange termijn naar herstel als het water zich terugtrekt
Australië begint op lange termijn naar herstel als het water zich terugtrekt Gemeenschapseffecten van extreem weer vormen klimaatovertuigingen
Gemeenschapseffecten van extreem weer vormen klimaatovertuigingen NASA's Aqua-satelliet ziet tropische cycloon Mekunu sterker worden
NASA's Aqua-satelliet ziet tropische cycloon Mekunu sterker worden Steden kunnen groeien zonder riffen en oceanen te slopen. Hier is hoe
Steden kunnen groeien zonder riffen en oceanen te slopen. Hier is hoe
Hoofdlijnen
- Onderzoekers ontrafelen de kristalstructuur van een belangrijk enzym van SARS-CoV-2, wat de weg vrijmaakt voor nieuwe antivirale middelen
- Een dierencel maken voor een wetenschapsproject
- Twee als het over land gaat? Biologen ontdekken dodelijk TTX-toxine in twee terrestrische soorten
- Hoe eiwitaggregatie plaatsvindt in cellen
- Nieuw onderzoek werpt licht op hoe Salmonella zich in het lichaam verspreidt
- Nieuwe inzichten in hoe vasculaire netwerken zich vormen in de hersenen van vissen
- Het zien van voedsel kan vissen naar het land hebben gelokt
- Hoe een klein en vreemd zeedier gedurende zijn hele leven onbeperkt sperma produceert
- Wat zijn de veranderingen in de massa van eieren bij termosmose?
- Zonnewaterstof:Laten we eens kijken naar de stabiliteit van foto-elektroden

- Door poreus materiaal kunnen autonome onderwatervoertuigen verder reizen

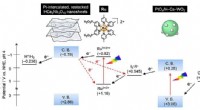
- Nieuwe fotokatalysator verhoogt de efficiëntie van watersplitsing voor schone waterstofproductie
- Van kantoorramen tot Mars:wetenschappers debuteren superisolerende gel

- Wat is groene stomerij? Een toxics-expert legt uit:

 Vastgelopen weerpatronen zullen groter worden door klimaatverandering
Vastgelopen weerpatronen zullen groter worden door klimaatverandering Een Brexit-blijver of -verlater zijn is meer psychologisch dan je denkt
Een Brexit-blijver of -verlater zijn is meer psychologisch dan je denkt Welk element komt voor als geel poeder?
Welk element komt voor als geel poeder?  Vrouwen die tijdens de spits pendelen worden blootgesteld aan hogere niveaus van verontreinigende stoffen
Vrouwen die tijdens de spits pendelen worden blootgesteld aan hogere niveaus van verontreinigende stoffen NASA ziet Mauritius bedekt door tropische storm Calvinia
NASA ziet Mauritius bedekt door tropische storm Calvinia De beweging en de gevolgen van microplasticvervuiling voorspellen
De beweging en de gevolgen van microplasticvervuiling voorspellen Ligt uw zwaartepunt rond het bekken als u opstaat?
Ligt uw zwaartepunt rond het bekken als u opstaat?  Stranderosie:satellieten laten zien hoe klimaatcycli de kustlijnen beïnvloeden
Stranderosie:satellieten laten zien hoe klimaatcycli de kustlijnen beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

