
Wetenschap
Hoeveel mol zn worden er verbruikt als 1,60 x 1024 moleculen hcl volledig reageren in de volgende vergelijking plus 2hcl is gelijk aan zncl2 h2?
Om het aantal mol verbruikt Zn te bepalen, moeten we rekening houden met de stoichiometrie van de reactie:
Zn + 2HCl → ZnCl2 + H2
Uit de uitgebalanceerde vergelijking kunnen we zien dat 1 mol Zn reageert met 2 mol HCl. Dus als 1,60 x 1024 moleculen HCl reageren, kunnen we de overeenkomstige mol HCl berekenen:
Mol HCl =(1,60 x 1024 moleculen HCl) / (6,022 x 1023 moleculen/mol) ≈ 0,266 mol HCl
Omdat 1 mol Zn reageert met 2 mol HCl, kunnen we het aantal verbruikte mol Zn bepalen:
Mol Zn =(0,266 mol HCl) / (2 mol HCl/mol Zn) ≈ 0,133 mol Zn
Daarom wordt ongeveer 0,133 mol Zn verbruikt wanneer 1,60 x 1024 moleculen HCl volledig reageren in de gegeven vergelijking.
 Hoe te testen op waterstofchloride
Hoe te testen op waterstofchloride  Zink reageert met ijzerchloride, waarbij zink plus neerslag ontstaat?
Zink reageert met ijzerchloride, waarbij zink plus neerslag ontstaat?  Wetenschappers tonen aan dat positief geladen hydrogels de overleving en groei van neurale stamcellen bevorderen
Wetenschappers tonen aan dat positief geladen hydrogels de overleving en groei van neurale stamcellen bevorderen  Als u azijn verdunt, hoe zal dit de pH-waarde beïnvloeden?
Als u azijn verdunt, hoe zal dit de pH-waarde beïnvloeden?  Wat is het gebruik van Cobalt?
Wat is het gebruik van Cobalt?
 Ethiopië begint tweede fase van vullen megadam, woedend Egypte
Ethiopië begint tweede fase van vullen megadam, woedend Egypte Forel in door mijnen vervuilde rivieren is genetisch geïsoleerd, blijkt uit nieuw onderzoek
Forel in door mijnen vervuilde rivieren is genetisch geïsoleerd, blijkt uit nieuw onderzoek  Geowetenschappers roepen op tot actie om raciale ongelijkheid in het veld aan te pakken
Geowetenschappers roepen op tot actie om raciale ongelijkheid in het veld aan te pakken Fundamentele vraag over hoe het leven begon opgelost?
Fundamentele vraag over hoe het leven begon opgelost?  In het noordpoolgebied, het smelten van de lentesneeuw zorgt voor de productie van verse kooldioxide
In het noordpoolgebied, het smelten van de lentesneeuw zorgt voor de productie van verse kooldioxide
Hoofdlijnen
- Hoe weet een bacterie dat het tijd is om zich te splitsen?
- Welk kenmerk wordt genoemd als het celmembraan alleen bepaalde moleculen en ionen de cel binnenlaat of verlaat?
- Hoe verouderende klokken tikken:nieuwe studie wijst op stochastische veranderingen in cellen
- Wat is insomina?
- Welke theorie verklaart waarom de populatie in de loop van de tijd kan worden gewijzigd?
- Pompoenboerderijen passen zich aan om de bodem te verbeteren en de uitstoot te verlagen
- Studie:Hoe een intern organel verdubbelt
- Wat hebben rommelige gazons te maken met bijenvoer? Een deskundige legt het uit
- Hoe bacteriën in vivo bacteriofagen ontwijken
- Onderzoekers ontwikkelen recycling voor koolstofvezelcomposieten

- Bio-geïnspireerde op MXene gebaseerde actuatoren voor programmeerbare slimme apparaten
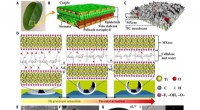
- Vervaardiging van door licht geactiveerde eiwitten

- Dundee-lab lost HOIL-1-mysterie op

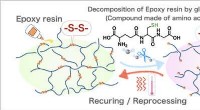
- Nieuwe strategie ter bevordering van hergebruik van met koolstofvezel versterkte kunststoffen
 Wat gebeurt er met de overblijfselen van de fusie van neutronensterren?
Wat gebeurt er met de overblijfselen van de fusie van neutronensterren?  Numerieke simulaties onthullen rivieren van lading in materialen die supergeleidend worden bij hoge temperaturen
Numerieke simulaties onthullen rivieren van lading in materialen die supergeleidend worden bij hoge temperaturen Het Japanse Sapporo beleeft de eerste dag van 25 graden Celsius sinds het begin van de metingen
Het Japanse Sapporo beleeft de eerste dag van 25 graden Celsius sinds het begin van de metingen  Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap
Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap Los niet alleen op voor x:als je kinderen real-world scenario's laat ontdekken, blijven ze in de wiskundeles
Los niet alleen op voor x:als je kinderen real-world scenario's laat ontdekken, blijven ze in de wiskundeles Hoe wolkenkrabbers werken
Hoe wolkenkrabbers werken  Palmlezers? Japans team bouwt tweede huid berichtweergave
Palmlezers? Japans team bouwt tweede huid berichtweergave Ontbindende bladeren zijn een verrassende bron van broeikasgassen
Ontbindende bladeren zijn een verrassende bron van broeikasgassen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

