
Wetenschap
Voor de reactie is Cl2 plus 2 KBr gelijk aan Br2. Bereken het opbrengstpercentage als 200 g reageert met overmaat KBr om 410 Br2 te produceren?
1 mol Cl2 reageert met 2 mol KBr en produceert 1 mol Br2.
De molaire massa van Cl2 is 70,9 g/mol en de molaire massa van Br2 is 159,8 g/mol.
Daarom is 200 g Cl2 gelijk aan 200 g / 70,9 g/mol =2,82 mol Cl2.
Volgens de stoichiometrie zal 2,82 mol Cl2 reageren met 2 x 2,82 =5,64 mol KBr, waardoor 2,82 mol Br2 ontstaat.
De theoretische opbrengst aan Br2 bedraagt derhalve 2,82 mol x 159,8 g/mol =452,3 g.
Nu kunnen we de procentuele opbrengst berekenen:
Percentage opbrengst =(werkelijke opbrengst / theoretische opbrengst) x 100%
De werkelijke opbrengst bedraagt 410 g.
Percentage opbrengst =(410 g / 452,3 g) x 100% =90,6%
Daarom is de procentuele opbrengst aan Br2 bij deze reactie 90,6%.
 Hoe de ozonlaag werkt
Hoe de ozonlaag werkt  Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?
Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?  Wetenschappers stellen nieuwe ladingsscheidingsstrategie voor in ferro-elektrische fotokatalysatoren
Wetenschappers stellen nieuwe ladingsscheidingsstrategie voor in ferro-elektrische fotokatalysatoren Nieuw membraan van twee polymeer verhoogt de prestaties van waterstofbrandstofcellen
Nieuw membraan van twee polymeer verhoogt de prestaties van waterstofbrandstofcellen Waarom zijn organische verbindingen zeer brandbaar?
Waarom zijn organische verbindingen zeer brandbaar?
 Ontbrekend lood in Flint waterleidingen bevestigt oorzaak van crisis
Ontbrekend lood in Flint waterleidingen bevestigt oorzaak van crisis Psychologische interventies kunnen het stationair draaien van de motor verminderen en de luchtkwaliteit verbeteren
Psychologische interventies kunnen het stationair draaien van de motor verminderen en de luchtkwaliteit verbeteren Wat zijn de acht belangrijkste ecosystemen?
Wat zijn de acht belangrijkste ecosystemen?  Zoektocht om het wereldwijde waterplantmysterie op te lossen
Zoektocht om het wereldwijde waterplantmysterie op te lossen Door klimaat veroorzaakte overstromingen brengen tegen 2050 300 miljoen in gevaar
Door klimaat veroorzaakte overstromingen brengen tegen 2050 300 miljoen in gevaar
Hoofdlijnen
- Inzicht in onze levensduur van meer dan 50 jaar die nog steeds in ontwikkeling is, genetische studie toont aan
- Biogeografie: definitie, theorie, bewijs & voorbeelden
- Hoe zaden weten dat het een goed moment is om te ontkiemen
- Nederlandse onderzoekers bouwen ecosysteem van de toekomst
- De lange en korte van een supergen voor efficiënte bestuiving
- Waarom verteren protease maag en dunne darm?
- Geen bewijs dat het onthoornen van zwarte neushoorns een negatieve invloed heeft op de voortplanting of overleving van de soort, studievondsten
- Hebben garnalen een zenuwstelsel?
- Nectarivoren:een wereld van zoetekauwen
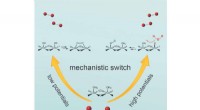
- Potentiaalafhankelijke schakelaar helpt bij het splitsen van water met behulp van kobaltoxidekatalysatoren
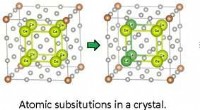
- Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen
- Wetenschappers ontwikkelen goedkope sensor die COVID-19 in afvalwater kan detecteren

- Nieuwe methode voor microbiële energieproductie ontdekt

- Synthesemethode vergroot materiële mogelijkheden

 Wat is de oorsprong van ijzer?
Wat is de oorsprong van ijzer?  Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden
Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt
Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt Grafeenoxidepapier verandert met spanning
Grafeenoxidepapier verandert met spanning Wanneer zijn consumenten loyaal aan merken? Nieuw model helpt verklaren
Wanneer zijn consumenten loyaal aan merken? Nieuw model helpt verklaren  Onderzoekers onderzoeken hoe inktvissen in het donker communiceren
Onderzoekers onderzoeken hoe inktvissen in het donker communiceren  Grote hit voor Facebook aangezien de laatste resultaten scheuren in de groei laten zien
Grote hit voor Facebook aangezien de laatste resultaten scheuren in de groei laten zien Kwantumelektronensnelwegen verkennen met laserlicht
Kwantumelektronensnelwegen verkennen met laserlicht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

