
Wetenschap
Potentiaalafhankelijke schakelaar helpt bij het splitsen van water met behulp van kobaltoxidekatalysatoren
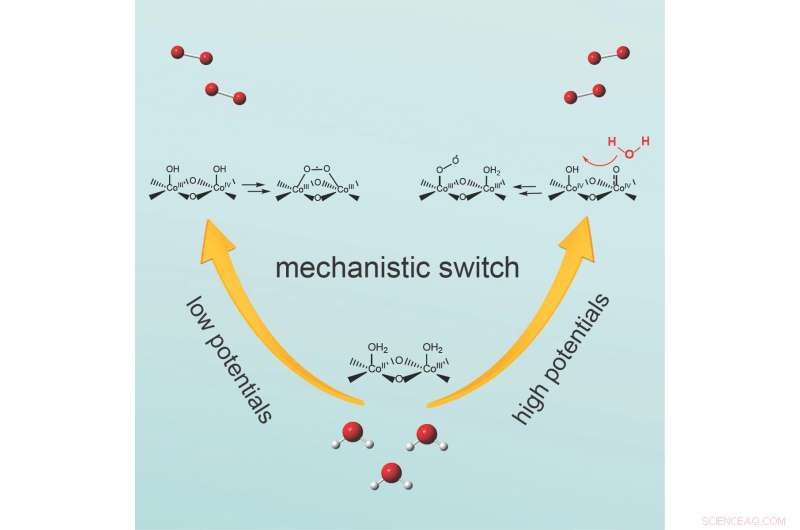
Een potentiaalafhankelijke schakelaar helpt bij het splitsen van water met behulp van kobaltoxidekatalysatoren, Onderzoekers van Boston College en Yale University rapporteren in het tijdschrift Chem. Kleine elektrische lading drijft een zuurstofontwikkelingsreactie aan die water gebruikt om waterstofgas te produceren. Credit: Chemo
Met behulp van overvloedig kobalt en een unieke experimentele benadering om manieren te onderzoeken om een trage katalytische reactie te versnellen om waterstof uit water te halen, onderzoekers van Boston College en Yale University ontdekten een mechanistische schakelaar in de zuurstofevolutiereactie, een belangrijke stap in de richting van het optimaliseren van elektrokatalysatoren voor het splitsen van water om schone energie te produceren.
Het mechanisme schakelt door de hoeveelheid spanning te variëren, of toegepast potentieel, het team rapporteert in het journaal Chemo . Bij matig potentieel, twee zuurstofatomen gebonden aan het katalysatoroppervlak reageren om de zuurstof-zuurstofbinding te vormen. Daarentegen, bij hogere potentiëlen, de zuurstof-zuurstofbinding wordt gevormd door een watermolecuul dat een aan het oppervlak gebonden zuurstofsoort aanvalt.
De bevindingen laten zien dat in deze materiaalklasse, een elektrokatalysator voor deze reactie moet worden gekozen, of geoptimaliseerd, afhankelijk van het potentiële regime waarin het naar verwachting zal werken in een reactor. Met andere woorden, een bepaalde katalysator kan bijzonder efficiënt zijn in het bevorderen van één mechanisme, maar niet de ander.
"Wat ons verraste, was hoe steil de omschakeling plaatsvindt van het ene mechanische regime naar het andere met toegepast potentieel, " zei Dunwei Wang, hoogleraar scheikunde aan het Boston College, een hoofdauteur van het rapport. "Er is slechts ongeveer 100 mV nodig om tussen de twee mechanismen te schakelen. Het herinnert ons eraan hoe gevoelig reactiemechanismen zijn. Meer in het algemeen, de gemakkelijke omschakeling kan een andere indicatie zijn van hoe fotosynthese zich kan aanpassen aan veranderingen in de reactieomgeving voor optimale prestaties."
Onderzoekers hebben gewerkt aan het splitsen van water in moleculaire waterstof en zuurstof in een poging om overvloedige hernieuwbare energie te leveren in de vorm van transporteerbaar en op te slaan waterstofgas. De splitsing kan worden bereikt met elektrokatalyse, een proces waarbij de waterstof- en zuurstofontwikkelingsreacties plaatsvinden in ruimtelijk gescheiden compartimenten op elektroden. Dat maakt elektrokatalyse een veelbelovend middel om schoon waterstofgas te produceren.
Echter, de zuurstofevolutiereactie (OER) is traag, zei Wang. Als resultaat, de snelheid van de algehele watersplitsingsreactie wordt beperkt door de trage OER. De reactie moet worden vergemakkelijkt door katalysatoren, dat is, materialen die de reactie bevorderen zonder zelf in het proces te worden verbruikt. Daten, economisch levensvatbare elektrokatalysatoren voor de bevordering van de zuurstofontwikkelingsreactie zijn nog niet ontwikkeld. Wang en zijn collega's concentreerden zich op de OER in veelbelovende elektrokatalysatoren in een poging om de reactieprocessen beter te begrijpen en die inzichten te gebruiken om efficiëntere en stabielere elektrokatalysatoren voor deze reactie te ontwerpen.
Ze richtten zich op de reactie in een klasse van elektrokatalysatoren die zijn gebaseerd op oxiden van kobalt, een goedkoop en aardrijk materiaal, attributen die zich efficiënt zouden vertalen naar gebruik op industriële schaal, zei Wang.
In het laatste decennium, verschillende op kobaltoxide gebaseerde elektrokatalysatoren zijn naar voren gekomen als veelbelovende kandidaten voor het promoten van de OER. In samenwerking met collega's van Yale University, Wang en zijn team bestudeerden de OER op twee soorten kobaltoxide-elektrokatalysatoren met elektrochemische technieken, infrarood spectrosopie, en dichtheidsfunctionaaltheorie.
Wang zei dat het team de waterconcentratie controleerde door water-in-zoutelektrolyten te gebruiken. die een zoutconcentratie hebben die ongeveer tien keer hoger is dan die van zeewater. Als resultaat, de onderzoekers konden de activiteit van water regelen door de hoeveelheid zout in de elektrolyt aan te passen. Ze controleerden hoe de reactiesnelheid reageerde op verschillende concentraties water. Dit onthulde het mechanisme van de OER op op kobalt gebaseerde elektrokatalysatoren, zei Wang. Co-auteur en BC Associate Professor of Chemistry Matthias Waegele en zijn onderzoeksteam gebruikten infraroodspectroscopie, die berust op de interactie van infrarood licht met moleculen, om reactietussenproducten van de OER onder bedrijfsomstandigheden te detecteren.
Ze waren in staat om een belangrijk reactietussenproduct te detecteren, die werd voorspeld door de berekeningen van Yale-chemicus Victor Batista en zijn onderzoeksgroep. Gary Brudvig, een anorganische chemicus aan Yale, adviseerde ook het team tijdens het project.
Wang zei dat het team de zuurstofevolutiereactie van dichtbij wilde bekijken, vooral de eigenschap dat het een stapsgewijs proces is, geen enkele gebeurtenis. Water bevat slechts één zuurstofatoom. Het product van de OER is moleculaire zuurstof, die twee zuurstofatomen bevat. Daarom, tijdens de OER wordt een zuurstof-zuurstofbinding gevormd, hij merkte.
Wang zei dat onderzoekers op dit gebied zich hebben gericht op twee centrale vragen:hoe vormt deze zuurstofbinding en in welke stap? In eerdere studies zijn twee hoofdmechanismen voorgesteld, onderzoekers moesten echter nog beslissen onder welke experimentele omstandigheden - temperatuur, of aangelegde elektrodepotentiaal, bijvoorbeeld - de zuurstof-zuurstofbinding vormt en welke van de mechanismen de dominante is.
Wang en zijn collega's besloten goed te kijken hoe de aangelegde elektrodepotentiaal het mechanisme van de vormingsstap van zuurstof-zuurstofbinding dicteert, aangezien reacties in elektrokatalyse worden aangedreven door een elektrische potentiaal die op de katalysator wordt toegepast.
De bevindingen suggereren dat de mechanistische schakelaar algemeen kan zijn voor op oxide gebaseerde elektrokatalysatoren, zei Wang.
"We zijn erg benieuwd of deze observatie ook van toepassing is op andere veelbelovende elektrokatalysatoren, "zei hij. "In het bijzonder, we werken momenteel aan katalysatoren met atomair gedefinieerde actieve centra. In tegenstelling tot de op kobalt gebaseerde elektrokatalysatoren, waarvan de atomaire structuur in het actieve centrum onopgelost blijft, ons nieuwe studieplatform bevat katalytische centra die atomair goed gedefinieerd zijn. Het zal heel interessant zijn om te zien of de potentiaal-geïnduceerde mechanistische omschakeling ook op die katalysatoren optreedt."
 Eenstaps 3D-printen van katalysatoren
Eenstaps 3D-printen van katalysatoren Verdeel en heers:onderzoekers vinden de sleutel tot het maken van betere medicijnen met minder bijwerkingen
Verdeel en heers:onderzoekers vinden de sleutel tot het maken van betere medicijnen met minder bijwerkingen Hoe PPM naar PPT te converteren
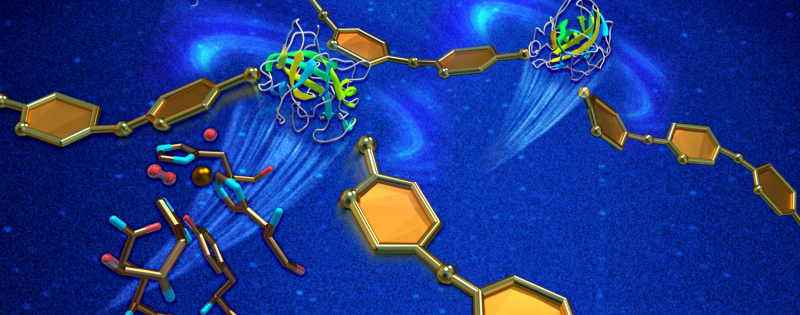
Hoe PPM naar PPT te converteren  Eiwitten choreograferen de oneindig kleine dans van levende cellen en functionele biomaterialen
Eiwitten choreograferen de oneindig kleine dans van levende cellen en functionele biomaterialen Hoe de neutronen te vinden in het periodiek systeem
Hoe de neutronen te vinden in het periodiek systeem
 Onderzoekers beweren dat langdurige blootstelling aan luchtvervuiling in China tussen 2000 en 2016 30,8 miljoen mensen heeft gedood
Onderzoekers beweren dat langdurige blootstelling aan luchtvervuiling in China tussen 2000 en 2016 30,8 miljoen mensen heeft gedood De Arctische koolstofcyclus versnelt, studieverslagen
De Arctische koolstofcyclus versnelt, studieverslagen Vulkaanonderzoekers leren hoe de aarde supereruptie-voedende magmasystemen bouwt
Vulkaanonderzoekers leren hoe de aarde supereruptie-voedende magmasystemen bouwt Onderzoek schetst de effecten van klimaatopwarming op microbiële netwerkinteracties
Onderzoek schetst de effecten van klimaatopwarming op microbiële netwerkinteracties Met as bedekte St. Vincent zet zich schrap voor meer vulkaanuitbarstingen
Met as bedekte St. Vincent zet zich schrap voor meer vulkaanuitbarstingen
Hoofdlijnen
- Hoe maak je een celmodel van een Amoeba
- Woordproblemen schrijven voor Math
- Voorbeelden van archaebacteriën met hun wetenschappelijke naam en classificatie
- Onderzoek onthult hoe verontreinigende stoffen de vroege embryonale ontwikkeling beïnvloeden
- Onderzoekers maken doorbraak in dodelijke kattenziekte
- Valse oogvlekken intimideren roofdieren, onderzoekers vinden
- Ziekteverwekkers identificeren die sojastamkanker veroorzaken
- Onderzoek naar superstil gemaakte DNA hints naar nieuwe manieren om cellen te herprogrammeren
- Twee zeldzame aanvallen van zeeleeuwen sluiten baai in San Francisco Bay af
- Schrijf met warmte, afkoelen en herhaal dan met herschrijfbaar papier

- Wetenschappers ontwikkelen betere manier om virussen te blokkeren die luchtweginfecties bij kinderen veroorzaken
- Op je plaats, klaar - Neutronen voeren de reactiviteit van enzymen uit voor een betere productie van biobrandstoffen
- Het aantal ionen in een verbinding vinden

- Wetenschappers creëren een chemische methode voor het in kaart brengen van de ruimte en ontrafelen het mysterie van het getal van Mendelejev

 Hoe succesvol zijn supersaver-evenementen met een winkelthema?
Hoe succesvol zijn supersaver-evenementen met een winkelthema? Wetenschappers lossen mysterie op van kleurrijke nanobuisjes in fauteuils
Wetenschappers lossen mysterie op van kleurrijke nanobuisjes in fauteuils Belangrijkste soorten ecosystemen
Belangrijkste soorten ecosystemen Stervend meer in Guatemala onderstreept bedreiging van klimaatverandering
Stervend meer in Guatemala onderstreept bedreiging van klimaatverandering Onderzoekers leggen uit hoe wanorde in kleine kristallen warmte-therapeutische systemen mogelijk maakt
Onderzoekers leggen uit hoe wanorde in kleine kristallen warmte-therapeutische systemen mogelijk maakt GM investeert $ 2,2 miljard in Detroit om elektrische voertuigen te bouwen
GM investeert $ 2,2 miljard in Detroit om elektrische voertuigen te bouwen Moeten we zenuwachtig zijn over treinreizen?
Moeten we zenuwachtig zijn over treinreizen?  Een doorbraak in het ontwerpen van moleculaire motoren
Een doorbraak in het ontwerpen van moleculaire motoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

