
Wetenschap
Wordt H2 beschouwd als een polaire binding?
De H-H-binding in moleculaire waterstof (H2) wordt geclassificeerd als een niet-polaire covalente binding. Dit betekent dat de elektronen in de binding gelijkelijk worden verdeeld tussen de twee waterstofatomen, wat resulteert in geen significant verschil in elektronegativiteit.
Daarom bezit het H2-molecuul geen netto elektrisch dipoolmoment, wat een karakteristiek kenmerk is van polaire bindingen.
 Door klimaatverandering te zeggen in plaats van opwarming van de aarde, verkleint de partijdige kloof met 30 procent in de VS.
Door klimaatverandering te zeggen in plaats van opwarming van de aarde, verkleint de partijdige kloof met 30 procent in de VS. Grote branden vragen om een grote reactie:lessen uit de Big Burn uit 1910
Grote branden vragen om een grote reactie:lessen uit de Big Burn uit 1910 Wetenschapsbeurs over hoe vitamine C en ibuprofen de plantengroei beïnvloeden
Wetenschapsbeurs over hoe vitamine C en ibuprofen de plantengroei beïnvloeden Een blik op klimaatverandering vanaf de boomtoppen van West-Afrika
Een blik op klimaatverandering vanaf de boomtoppen van West-Afrika Kooldioxide-emissies van wereldwijde visserijen groter dan eerder gedacht
Kooldioxide-emissies van wereldwijde visserijen groter dan eerder gedacht
Hoofdlijnen
- Wat is er nodig om de regent-honingeter te redden?
- Waarom wordt informatie opgeslagen in DNA-bewijsmateriaal vóór een schepper en tegen de evolutie?
- Worden virussen als levend of niet-levend beschouwd?
- Onderzoekers voltooien eerste uitgebreide dreigingsanalyse van alle bomen in de VS
- Wie kan profiteren van klimaatverandering? Ratelslangen, suggereert onderzoek
- Inzicht in cellulaire transcriptiereacties op zuurstofgebrek
- Hoe wordt citroenzuur aangemaakt in het menselijk lichaam?
- Vechten of vluchten? Hoe vogels de mysteries van evolutie helpen onthullen
- Stadia van een typische celcyclus
- Nieuw retroreflecterend materiaal kan worden gebruikt in nachtelijke, van kleur veranderende verkeersborden

- Onderzoekers ontwikkelen synthetische steigers om gewonde pezen en ligamenten te genezen

- Het identificeren van designer medicijnen die worden ingenomen door patiënten met een overdosis

- Rundvleespeptiden blokkeren bittere smaken
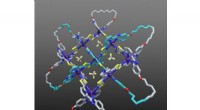
- Wetenschappers ontdekken een nieuw type moleculaire knoop met behulp van röntgendiffractietechnieken
 Interagerende Antarctische gletsjers kunnen sneller smelten en bijdragen aan de zeespiegel
Interagerende Antarctische gletsjers kunnen sneller smelten en bijdragen aan de zeespiegel Nuttig of griezelig? Machines stellen Gmail-antwoorden voor
Nuttig of griezelig? Machines stellen Gmail-antwoorden voor  Boom en buste voor oude zeedraken
Boom en buste voor oude zeedraken COVID-19 en het effect ervan op religieuze overtuigingen
COVID-19 en het effect ervan op religieuze overtuigingen Hoe snel kunnen vingers bewegen?
Hoe snel kunnen vingers bewegen?  Hoe het volume te berekenen voor Ice
Hoe het volume te berekenen voor Ice Zonne-elektrische voortstuwing zorgt ervoor dat NASA's Psyche-ruimtevaartuig gaat
Zonne-elektrische voortstuwing zorgt ervoor dat NASA's Psyche-ruimtevaartuig gaat Amerikaanse biologische klok-genetici winnen Nobelprijs voor Geneeskunde 2017
Amerikaanse biologische klok-genetici winnen Nobelprijs voor Geneeskunde 2017
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

