
Wetenschap
Waarom wordt geconcentreerd zwavelzuur niet gebruikt om ammoniak te drogen?
Geconcentreerd zwavelzuur wordt niet gebruikt om ammoniak te drogen, omdat het een zuur-base-reactie ondergaat met ammoniak om ammoniumsulfaat te vormen. Bij deze reactie komen watermoleculen vrij en ontstaat er een witte vaste stof, ammoniumsulfaat, in plaats van dat de ammoniak uitdroogt.
De chemische vergelijking voor de reactie tussen geconcentreerd zwavelzuur (H2SO4) en ammoniak (NH3) is:
H2SO4 + 2 NH3 → (NH4)2SO4 + H2O
Deze reactie is zeer exotherm, wat betekent dat er een aanzienlijke hoeveelheid warmte vrijkomt. De watermoleculen die tijdens deze reactie worden geproduceerd, kunnen ook bijdragen aan de vochtigheid in de omgeving, in plaats van de ammoniak uit te drogen.
Daarom is geconcentreerd zwavelzuur geen geschikt droogmiddel voor ammoniak vanwege het reactieve karakter ervan en de vorming van ammoniumsulfaat als bijproduct.
 Wetenschappers gebruiken coöperatieve actie van een ligand-tegenionsysteem voor duurzame etherproductie
Wetenschappers gebruiken coöperatieve actie van een ligand-tegenionsysteem voor duurzame etherproductie Hoeveel ongepaarde elektronen bevinden zich in een kobaltatoom in zijn grondtoestand?
Hoeveel ongepaarde elektronen bevinden zich in een kobaltatoom in zijn grondtoestand?  Diagnostisch hulpmiddel voor coronavirus maakt belangrijke stap voorwaarts
Diagnostisch hulpmiddel voor coronavirus maakt belangrijke stap voorwaarts Nieuwe oplosmiddelen om plantaardige cellulose af te breken voor bio-ethanol
Nieuwe oplosmiddelen om plantaardige cellulose af te breken voor bio-ethanol Een bijgewerkt begrip van hoe chemicaliën met toegevoegde waarde kunnen worden gesynthetiseerd
Een bijgewerkt begrip van hoe chemicaliën met toegevoegde waarde kunnen worden gesynthetiseerd
 Stroomuitval en slapeloze nachten in recordhittegolf in China
Stroomuitval en slapeloze nachten in recordhittegolf in China Nieuw-Zeeland markeert verwoestende verjaardag van vulkaanuitbarsting
Nieuw-Zeeland markeert verwoestende verjaardag van vulkaanuitbarsting Delen van veel kuststeden zinken sneller dan de zee stijgt
Delen van veel kuststeden zinken sneller dan de zee stijgt COVID-19-lockdowns gekoppeld aan vervuilingspieken in sommige steden
COVID-19-lockdowns gekoppeld aan vervuilingspieken in sommige steden Onderzoekers onthullen de mate waarin rivieren in het hele land stroom verliezen aan watervoerende lagen
Onderzoekers onthullen de mate waarin rivieren in het hele land stroom verliezen aan watervoerende lagen
Hoofdlijnen
- Japanse wetenschappers kweken medicijnen in kippeneieren
- Vier hoofdgroepen organische verbindingen waaruit levende organismen bestaan
- Hoe voelen ziekteverwekkers de omgeving? Wetenschappers identificeren de structuren van belangrijke eiwitten
- Waarom slapen we?
- Top 5 manieren om slimmer te worden
- De structuur en functie van ribosomen in eukaryoten en prokaryoten
- Deskundigen maken zich zorgen over rauw vlees-diëten voor katten en honden
- Is er een gen voor elke ziekte?
- Onderzoekers verduidelijken hoe cellen zichzelf verdedigen tegen virussen
- Licht op efficiëntieverlies in organische zonnecellen

- Onderzoekers ontdekken de kunst van het feilloos printen van extreem harde staalsoorten
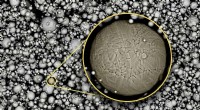
- Wetenschappers observeren voor het eerst katalysator tijdens Fischer-Tropsch-synthese

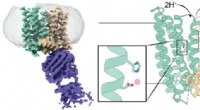
- Onthulling van de onverwachte structuur van ijzer-exporteur ferroportine
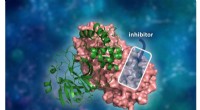
- Geschiedenis van inzichtelijk hiv-onderzoek inspireert neutronenverstrooiingsbenadering bij het bestuderen van COVID-19
 Uit onderzoek blijkt dat aardbevingen nog jaren doorgaan nadat de injectie van afvalwater in het gasveld is gestopt
Uit onderzoek blijkt dat aardbevingen nog jaren doorgaan nadat de injectie van afvalwater in het gasveld is gestopt Tech op proef:House panel begint beoordeling van marktmacht
Tech op proef:House panel begint beoordeling van marktmacht Waarom zou je alleen testen op één variabele per keer in een experiment?
Waarom zou je alleen testen op één variabele per keer in een experiment?  Een enorme aardverschuiving treft Papoea-Nieuw-Guinea, waarvan velen vreesden dat er doden zouden vallen
Een enorme aardverschuiving treft Papoea-Nieuw-Guinea, waarvan velen vreesden dat er doden zouden vallen  Alleen oesters eten in maanden met een 'r'? De vuistregel is minstens 4.000 jaar oud
Alleen oesters eten in maanden met een 'r'? De vuistregel is minstens 4.000 jaar oud  NA61/SHINE helpt neutrino-experimenten een handje
NA61/SHINE helpt neutrino-experimenten een handje Vraagt u zich af hoe u uw kinderen over toestemming kunt leren? Hier is een op leeftijd gebaseerde gids waarmee u aan de slag kunt
Vraagt u zich af hoe u uw kinderen over toestemming kunt leren? Hier is een op leeftijd gebaseerde gids waarmee u aan de slag kunt  Wat zijn de overeenkomsten tussen eierdoppen en tanden?
Wat zijn de overeenkomsten tussen eierdoppen en tanden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

