
Wetenschap
Hoeveel ongepaarde elektronen bevinden zich in een kobaltatoom in zijn grondtoestand?
[Ar] 3d^7 4s^2
In deze configuratie zijn de 3D-orbitalen gedeeltelijk gevuld. De 3D-orbitalen bestaan uit vijf gedegenereerde orbitalen, en de zeven elektronen in de 3D-orbitalen van kobalt verdelen zich over deze orbitalen op een manier die de elektron-elektronenafstoting minimaliseert.
Volgens de regel van Hund hebben elektronen in dezelfde orbitaal de neiging dezelfde spin te hebben, maar met de maximaal mogelijke spinmultipliciteit. Met andere woorden, elektronen zullen gedegenereerde orbitalen afzonderlijk bezetten voordat ze paren vormen.
In het geval van kobalt bezetten de zeven 3D-elektronen de vijf 3D-orbitalen, waarbij de spins van vier van de elektronen in één richting zijn uitgelijnd (spin-up) en de resterende drie elektronen hun spins in de tegenovergestelde richting hebben uitgelijnd (spin-down).
Daarom heeft een kobaltatoom in zijn grondtoestand drie ongepaarde elektronen .
 Klikreactie voor levende systemen:Bioorthogonale hydroaminering van geactiveerde lineaire alkynen
Klikreactie voor levende systemen:Bioorthogonale hydroaminering van geactiveerde lineaire alkynen CRISPR-methode voor voorwaardelijke genregulatie
CRISPR-methode voor voorwaardelijke genregulatie Cross-coupling ketonen:flexibiliteit toevoegen aan de toolbox voor synthetische chemie
Cross-coupling ketonen:flexibiliteit toevoegen aan de toolbox voor synthetische chemie Hoe olieraffinage werkt
Hoe olieraffinage werkt  Hoe te converteren van molariteit naar molaliteit
Hoe te converteren van molariteit naar molaliteit
Hoofdlijnen
- DNA-bewijs zet neushoornstropers achter tralies, studie toont
- Plasmamembraan: definitie, structuur en functie (met diagram)
- Nieuwe 'atlas' biedt ongekende inzichten over hoe genen functioneren in de vroege embryo-ontwikkeling
- Hoe elimineer je een virus in planten?
- Gel elektroforese lezen
- Onderzoekers maken betere kikkererwten mogelijk door genetische eigenschappen van wilde neven te benutten
- Onderzoek toont aan hoe de chemische eigenschappen van RNA-moleculen het oorspronkelijke leven hadden kunnen vergemakkelijken
- Fazantvlees dat als voedsel wordt verkocht, blijkt veel kleine stukjes giftig lood te bevatten
- Jagen op ooien met dikhoornschapen zou meer trofeerammen kunnen opleveren
- Een hydrogel die bloedingen uit een slagader kan stoppen

- Listeria-reproductie stoppen in zijn sporen
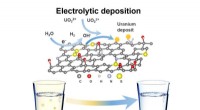
- Grafeenschuim gebruiken om gifstoffen uit drinkwater te filteren
- Poreuze enkelkristallijne monolieten op centimeterschaal met Lewis-zuurplaatsen met hoge dichtheid om propaandehydrogena te verbeteren
- Multisample-techniek om celadhesie te analyseren
 Studie koppelt fosforbelasting in meren aan extreme neerslaggebeurtenissen
Studie koppelt fosforbelasting in meren aan extreme neerslaggebeurtenissen Meteorologen verbeteren multivariabele geïntegreerde evaluatiemethode voor klimaatmodel
Meteorologen verbeteren multivariabele geïntegreerde evaluatiemethode voor klimaatmodel Het werk aan een zeldzame molecule heeft tot doel de celtherapie te verbeteren en een functionele genezing voor HIV te leveren
Het werk aan een zeldzame molecule heeft tot doel de celtherapie te verbeteren en een functionele genezing voor HIV te leveren Datering van vulkanische as in Sangiran toont aan dat Homo erectus later arriveerde dan gedacht
Datering van vulkanische as in Sangiran toont aan dat Homo erectus later arriveerde dan gedacht Bewijs opgraven van meer geavanceerde productie in de bronstijd
Bewijs opgraven van meer geavanceerde productie in de bronstijd Visual discovery opstarten Pinterest-bestanden voor IPO (Update)
Visual discovery opstarten Pinterest-bestanden voor IPO (Update) Chemici testen een nieuwe nanokatalysator voor het verkrijgen van waterstof
Chemici testen een nieuwe nanokatalysator voor het verkrijgen van waterstof Zelfcorrigerende kwantumcomputers binnen handbereik?
Zelfcorrigerende kwantumcomputers binnen handbereik?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

