
Wetenschap
Hoe verschilt een vaste stof van de vloeibare fase op moleculair niveau?
Moleculaire rangschikking:
1. Vaste stoffen :In vaste stoffen zijn moleculen of deeltjes dicht op elkaar gepakt in een regelmatige en zich herhalende opstelling. De deeltjes worden vaak in vaste posities gehouden door sterke intermoleculaire krachten, waardoor een stijve structuur ontstaat. Deze opstelling geeft vaste stoffen een bepaalde vorm en volume.
2. Vloeistoffen :In vloeistoffen zitten moleculen ook dicht op elkaar, maar ze hebben meer bewegingsvrijheid vergeleken met vaste stoffen. De deeltjes zitten niet vast en kunnen relatief gemakkelijk langs elkaar heen bewegen. Hierdoor kunnen vloeistoffen stromen en de vorm aannemen van hun container.
Intermoleculaire krachten:
1. Vaste stoffen :Vaste stoffen hebben sterke intermoleculaire krachten, zoals covalente bindingen, ionische bindingen of waterstofbruggen. Deze krachten houden de deeltjes stevig bij elkaar, waardoor aanzienlijke bewegingen worden voorkomen en de solide structuur behouden blijft.
2. Vloeistoffen :Vloeistoffen hebben zwakkere intermoleculaire krachten vergeleken met vaste stoffen. Deze krachten omvatten Van der Waals-krachten (inclusief dipool-dipoolkrachten en Londense dispersiekrachten), die zwakker zijn dan covalente of ionische bindingen. De zwakkere krachten zorgen voor een grotere moleculaire mobiliteit in vloeistoffen.
Diffusie en viscositeit:
1. Vaste stoffen :Diffusie is de beweging van deeltjes van een gebied met een hogere concentratie naar een gebied met een lagere concentratie. In vaste stoffen is de diffusie erg langzaam vanwege de sterke intermoleculaire krachten en vaste posities van de deeltjes.
2. Vloeistoffen :Vloeistoffen hebben een hogere diffusiesnelheid vergeleken met vaste stoffen. De zwakkere intermoleculaire krachten en de verhoogde moleculaire mobiliteit zorgen ervoor dat deeltjes vrijer kunnen bewegen, wat een snellere diffusie mogelijk maakt.
Viscositeit verwijst naar de weerstand van een vloeistof tegen stroming. Vaste stoffen hebben een hoge viscositeit vanwege de sterke intermoleculaire krachten, terwijl vloeistoffen een lagere viscositeit hebben vanwege zwakkere intermoleculaire krachten.
Samenvattend:vaste stoffen verschillen op moleculair niveau van vloeistoffen in termen van hun moleculaire rangschikking en intermoleculaire krachten. Vaste stoffen hebben een stijve structuur met sterke intermoleculaire krachten, terwijl vloeistoffen zwakkere intermoleculaire krachten en meer moleculaire mobiliteit hebben. Deze verschillen resulteren in de verschillende eigenschappen die we waarnemen in vaste en vloeibare toestanden van materie.
 Fast-tracking endocriene assays
Fast-tracking endocriene assays Hoe wordt het vrijkomen van overtollige waterdamp via de huidmondjes genoemd?
Hoe wordt het vrijkomen van overtollige waterdamp via de huidmondjes genoemd?  Hete randen van elektroden zetten CO2-gas om in brandstoffen en chemicaliën
Hete randen van elektroden zetten CO2-gas om in brandstoffen en chemicaliën Voorkomen van lithiumverlies voor lithium-ionbatterijen met hoge capaciteit
Voorkomen van lithiumverlies voor lithium-ionbatterijen met hoge capaciteit Bouwstenen van DNA en RNA hadden samen kunnen verschijnen voordat het leven op aarde begon
Bouwstenen van DNA en RNA hadden samen kunnen verschijnen voordat het leven op aarde begon
 Tropische storm let op in Guam, NASA ziet 02W-vorm
Tropische storm let op in Guam, NASA ziet 02W-vorm Grote aardbeving in Roemenië kan veel scholen doen omvallen gebouwen
Grote aardbeving in Roemenië kan veel scholen doen omvallen gebouwen Uit onderzoek blijkt dat schonere scheepsbrandstoffen de astma bij kinderen wereldwijd met 3,6 procent zullen verminderen
Uit onderzoek blijkt dat schonere scheepsbrandstoffen de astma bij kinderen wereldwijd met 3,6 procent zullen verminderen Oh, wat had jij grote tanden! Uitgestorven soorten hadden een groot gehemelte
Oh, wat had jij grote tanden! Uitgestorven soorten hadden een groot gehemelte  Hier is methaan:wetenschappers onderzoeken de oorsprong van een gapende permafrostkrater
Hier is methaan:wetenschappers onderzoeken de oorsprong van een gapende permafrostkrater
Hoofdlijnen
- Hoe kan licht virussen doden?
- Waarom leven mannen niet zo lang als vrouwen?
- Door nabootsing kunnen kleinere lachlijstervogels profiteren van het leven tussen grotere verwante soorten
- Smartphone-app gebruikt computervisie om verloren dieren te identificeren
- Verschillende populaties bosolifanten bijna instorten in Centraal-Afrika
- Hoe hydrofobiciteit eiwitassemblages vormt
- Hoe bacteriën hypothiocyaniet onschadelijk maken, een antimicrobieel wapen van het aangeboren immuunsysteem
- Wie geeft er om WA-uilen?
- Mobiele genetische elementen kunnen onbedoeld bacteriële immuunsystemen onderdrukken, zo blijkt uit onderzoek
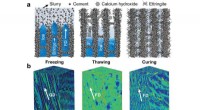
- Op hout geïnspireerd cement met hoge sterkte en multifunctionaliteit
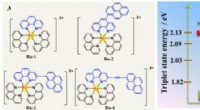
- Fijnafstemming van de aangeslagen toestand van Ru(II)-fotosensibilisatoren voor het stimuleren van de omzetting van kooldioxide
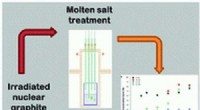
- Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen
- Onderzoekers ontwikkelen duurzame methode om vanilline te winnen uit houtverwerkingsafval

- Op textiel gebaseerde composieten kunnen de toekomst van lucht- en ruimtevaarttechniek weven

 Waarom wordt uw regenwater minder zuur?
Waarom wordt uw regenwater minder zuur?  Oplossen door Simpsons Regel met Excel
Oplossen door Simpsons Regel met Excel Californië geeft EPA de schuld van vastgelopen plannen om vervuiling te beteugelen
Californië geeft EPA de schuld van vastgelopen plannen om vervuiling te beteugelen Replica van gouden maanmodule gestolen uit museum nog steeds vermist
Replica van gouden maanmodule gestolen uit museum nog steeds vermist Breedspectrumremming van ontstekingsactivatie door anorganische nanomaterialen
Breedspectrumremming van ontstekingsactivatie door anorganische nanomaterialen  Pakistaanse burgers snakken naar schone lucht
Pakistaanse burgers snakken naar schone lucht Studie naar dinosaurusveren ontkracht:overweldigend bewijs ondersteunt Jurassic-fossiel wel degelijk van Archaeopteryx
Studie naar dinosaurusveren ontkracht:overweldigend bewijs ondersteunt Jurassic-fossiel wel degelijk van Archaeopteryx Ongelijke mate van zeespiegelstijging gekoppeld aan klimaatverandering
Ongelijke mate van zeespiegelstijging gekoppeld aan klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

