
Wetenschap
Wat is een isotoop?
Isotopen van hetzelfde element hebben dezelfde chemische eigenschappen, maar ze kunnen verschillende fysische eigenschappen hebben. Koolstof-12 en koolstof-13 zijn bijvoorbeeld beide stabiele isotopen, terwijl koolstof-14 een radioactieve isotoop is. Dit betekent dat koolstof-14 in de loop van de tijd vervalt in andere elementen.
Isotopen zijn belangrijk op verschillende gebieden, waaronder scheikunde, natuurkunde en geologie. Ze worden gebruikt in een verscheidenheid aan toepassingen, waaronder het dateren van objecten, het volgen van de beweging van elementen in de omgeving en het ontwikkelen van kernenergie.
Hier zijn enkele aanvullende details over isotopen:
* Het aantal protonen in een atoom bepaalt welk element het is.
* Het aantal neutronen in een atoom bepaalt de isotoop van dat element.
*Isotopen van hetzelfde element hebben hetzelfde aantal elektronen.
*Isotopen van hetzelfde element hebben dezelfde chemische eigenschappen.
* Isotopen van hetzelfde element kunnen verschillende fysieke eigenschappen hebben.
* Isotopen worden op verschillende gebieden gebruikt, waaronder scheikunde, natuurkunde en geologie.
 Ingenieurs creëren een inhaleerbare vorm van boodschapper-RNA
Ingenieurs creëren een inhaleerbare vorm van boodschapper-RNA Keramische membranen scheiden kleine organische moleculen met een molecuulmassa van 200 Dalton
Keramische membranen scheiden kleine organische moleculen met een molecuulmassa van 200 Dalton Wanneer chemie met groen licht nabootst wat er in het leven gebeurt
Wanneer chemie met groen licht nabootst wat er in het leven gebeurt Groene waterstof:onderzoek om efficiëntie te verhogen
Groene waterstof:onderzoek om efficiëntie te verhogen Vijftig jaar na de brand in Cuyahoga
Vijftig jaar na de brand in Cuyahoga
 Wat als alcohol niet bestond?
Wat als alcohol niet bestond?  Studie zegt dat door China gesteunde dam Mekong . zou vernietigen
Studie zegt dat door China gesteunde dam Mekong . zou vernietigen Het PhenoCam-netwerk maakt gebruik van big data om de impact van een warmer klimaat op de productiviteit van ecosystemen en koolstofcycli te voorspellen
Het PhenoCam-netwerk maakt gebruik van big data om de impact van een warmer klimaat op de productiviteit van ecosystemen en koolstofcycli te voorspellen Langer vechten, intensere brandseizoenen
Langer vechten, intensere brandseizoenen Aardbevingsprobleem oplossen door aardwarmte
Aardbevingsprobleem oplossen door aardwarmte
Hoofdlijnen
- Hoe Cytoplasma voor een celproject te maken
- Waarom zijn sommige mensen muggenmagneten en anderen niet? Entomoloog wijst op stofwisseling, lichaamsgeur en mindset
- Darmmicrobioom helpt beren met zeer verschillende diëten om dezelfde grootte te bereiken
- Waarom dromen we?
- Hoe slaaplabs werken
- Hoe u een mRNA-reeks kunt berekenen
- Daling van huismus in verband met luchtvervuiling en slechte voeding
- Snake Plant:een geweldige plant voor mensen die niet zo goed zijn met planten
- Is er een zaak tegen geluk?
- De sleutel tot het verminderen van de uitstoot van kooldioxide is gemaakt van metaal

- Onderzoekers ontwikkelen een nieuwe manier om belangrijke biologische processen te bestuderen

- Strijd tegen antibioticaresistente bacteriën heeft een gloednieuw wapen
- Een katalytisch ondersteunend materiaal speelt een hoofdrol

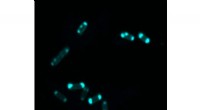
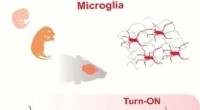
- Microglia in hersenweefsel visualiseren met een fluorescentie-aanzetsubstraat
 Hoe maak je een model van Mars voor 5e rang
Hoe maak je een model van Mars voor 5e rang  Vrouwen zijn wat voorzichtiger dan mannen, nietwaar?
Vrouwen zijn wat voorzichtiger dan mannen, nietwaar?  Wetenschappers ontdekken een nieuwe staat van materie voor water
Wetenschappers ontdekken een nieuwe staat van materie voor water Wetenschappers bieden bedrijven een nieuwe chemie voor groener polyurethaan
Wetenschappers bieden bedrijven een nieuwe chemie voor groener polyurethaan Een tand kraken:3D-kaart van atomen werpt licht op nanoschaalinterfaces in tanden, kan helpen bij het ontwerpen van materialen
Een tand kraken:3D-kaart van atomen werpt licht op nanoschaalinterfaces in tanden, kan helpen bij het ontwerpen van materialen Onderzoekers bootsen kristalroosters na om sterkere 3D-geprinte objecten te maken
Onderzoekers bootsen kristalroosters na om sterkere 3D-geprinte objecten te maken China's kolenproject in Servië roept zorgen over klimaatverandering op
China's kolenproject in Servië roept zorgen over klimaatverandering op Nieuw onderzoek naar poolgebieden terwijl de wereld zich schrap zet voor klimaatveranderingen:UN
Nieuw onderzoek naar poolgebieden terwijl de wereld zich schrap zet voor klimaatveranderingen:UN
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

