
Wetenschap
Moleculaire superlijm toont belofte van platform voor de ontdekking van geneesmiddelen tegen kanker
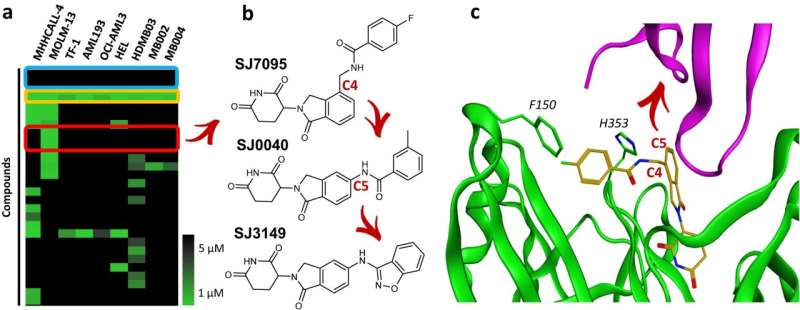
Wetenschappers van het St. Jude Children's Research Hospital hebben hun werk gepubliceerd over SJ3149, een stof met brede activiteit tegen vele soorten kanker, met name acute myeloïde leukemie (AML). SJ3149 blijft plakken aan het kankergerelateerde eiwit caseïnekinase 1 alfa (CK1α), wat tot de vernietiging ervan leidt.
Het werk is gepubliceerd in het tijdschrift Nature Communications .
"We hebben een moleculaire superlijm gemaakt", zegt senior co-corresponderend auteur Zoran Rankovic, Ph.D., St. Jude Department of Chemical Biology and Therapeutics. "SJ3149 is de eerste krachtige en selectieve CK1α-afbreker in zijn klasse, die werkzaamheid aantoont in zowel in vitro als in vivo kankermodellen."
Moleculaire lijmen werken door het natuurlijke eiwitrecyclingmechanisme van de cel te kapen. De moleculaire lijm rekruteert het beoogde eiwit voor een enzym dat het markeert voor vernietiging via een proces dat proteasomale afbraak wordt genoemd. Voor veel kankergerelateerde eiwitten die niet goed kunnen worden aangepakt door conventionele remmers van kleine moleculen, kunnen moleculaire lijmen een haalbaar therapeutisch alternatief zijn. Dit bracht de wetenschappers van St. Jude ertoe een grote eigen bibliotheek van moleculaire lijmen te ontwikkelen en deze te screenen tegen een reeks kankercellijnen, waarbij ze een eerste hit vonden.
Nadat de onderzoekers de geïdentificeerde hit hadden geoptimaliseerd, vertoonde het resulterende SJ3149-molecuul een hogere potentie en minder off-target-effecten dan vergelijkbare verbindingen. SJ3149 vertoonde een veelbelovende brede antikankeractiviteit, zelfs voor een moleculaire lijm, vandaar de bijnaam 'superlijm'. De verbinding lijkt ook een vergelijkbaar profiel te hebben als een klasse van goedgekeurde geneesmiddelen tegen kanker, muriene dubbele minuut 2 (MDM2)-remmers, wat er verder op wijst dat het klinische bruikbaarheid kan hebben.
Platform voor het ontdekken van moleculaire lijm
Moleculaire lijmen zijn een veelbelovende bron voor het vinden van nieuwe therapieën, omdat ze zich kunnen richten op voorheen ondrugbare eiwitten. Het vinden en aanpassen van deze moleculen voor klinisch gebruik was echter een uitdaging. Het identificeren en verfijnen van zo'n molecuul levert proof of concept dat de St. Jude-aanpak dit ontdekkingsproces kan versnellen.
"Ons werk biedt een blauwdruk om soortgelijke onderzoeken uit te voeren voor andere doelen", zegt co-corresponderende auteur Marcus Fischer, Ph.D., St. Jude Department of Chemical Biology and Therapeutics. De onderzoekers ontdekten de verbinding, veranderden deze door middel van een rationeel ontwerp en testten de werkzaamheid ervan. Om te begrijpen hoe de verbinding zo goed werkte, kristalliseerde de groep van Fischer het grote complex van het beoogde eiwit en SJ3149 bond zich aan de machinerie van de cel die verantwoordelijk is voor het merken van eiwitten voor afbraak, een eiwit-ubiquitine-ligase-apparaat.
"We konden zien dat het mooie van deze verbinding is dat het direct interageert met CK1α", legt Fischer uit. "SJ3149 strekt zich uit en verbindt CK1α rechtstreeks met het enzym dat het markeert voor de cellulaire afbraakmachinerie, wat een reden biedt voor de hoge afbraakeffectiviteit van de verbinding."
Begrijpen hoe dergelijke verbindingen op atomair niveau werken, kan de weg vrijmaken voor het rationele ontwerp van moleculaire lijmen.
"Dit is een perfect voorbeeld van het nemen van chemische materie en het maken van structurele en mechanistische inzichten om de werkzaamheid en cellulaire activiteit te begrijpen", zegt co-corresponderend auteur Jeffery Klco, MD, Ph.D., St. Jude Department of Pathology, een arts-wetenschapper met een focus op AML. "In dit stadium is het nog steeds slechts een leidend middel, maar dit zou zich kunnen ontwikkelen tot een andere potentiële optie voor de behandeling van verschillende kinderkankers, wat spannend is."
Het creëren van de verbinding was een grote gezamenlijke inspanning. Het werk omvatte het ontwerpen, synthetiseren en screenen van de moleculaire lijmbibliotheek, structuurgestuurde optimalisatie van de medicinale chemie en het testen in van patiënten afkomstige kankercellen. Dit was alleen mogelijk dankzij de gecombineerde expertise van de laboratoria van Rankovic, Fischer en Klco, in samenwerking met interne en externe medewerkers. De aanpak kan nu worden gebruikt als basis voor verdere ontdekking.
"De chemische biologie is een nieuw paradigma binnengegaan met moleculaire lijmen," zei Rankovic. "Met deze studie hebben we nu een pijplijn opgezet om nieuwe, veelbelovende moleculaire lijmen voor kankerbehandelingen te identificeren."
Meer informatie: Gisele Nishiguchi et al., Selectieve CK1α-afbrekers oefenen antiproliferatieve activiteit uit tegen een breed scala aan menselijke kankercellijnen, Nature Communications (2024). DOI:10.1038/s41467-024-44698-1
Journaalinformatie: Natuurcommunicatie
Aangeboden door St. Jude Children's Research Hospital
 Verwijderen van Mucus
Verwijderen van Mucus Driedimensionale Mn-gedoteerde nanosheets als efficiënte elektrokatalysatoren voor het splitsen van alkalisch water
Driedimensionale Mn-gedoteerde nanosheets als efficiënte elektrokatalysatoren voor het splitsen van alkalisch water 302 Vs. 304 roestvrij staal
302 Vs. 304 roestvrij staal  Onderzoekers ontwikkelen tool voor snelle diagnose van bacteriële infecties
Onderzoekers ontwikkelen tool voor snelle diagnose van bacteriële infecties Waarom is het belangrijk om vertrouwd te zijn met laboratoriumapparatuur en hun gebruik?
Waarom is het belangrijk om vertrouwd te zijn met laboratoriumapparatuur en hun gebruik?
 5 Basisbehoeften van een dier
5 Basisbehoeften van een dier  Boombedekking is niet genoeg voor duurzame ontwikkeling, een globale kaart van de natuurlijkheid van bossen is ook vereist
Boombedekking is niet genoeg voor duurzame ontwikkeling, een globale kaart van de natuurlijkheid van bossen is ook vereist Graslandgebieden moeten verstandig worden gekozen
Graslandgebieden moeten verstandig worden gekozen Kun je geroosterde zonnebloempitten aan vogels voeren?
Kun je geroosterde zonnebloempitten aan vogels voeren?  Onderzoek naar regenwormen zet boeren aan tot actie
Onderzoek naar regenwormen zet boeren aan tot actie
Hoofdlijnen
- Paarse plant is in de verdediging
- Onderzoek identificeert het mechanisme achter medicijnresistentie bij malariaparasieten
- Hoe mariene roofdieren voedselhotspots vinden in open oceaanwoestijnen
- Wat gebeurt er in de interfase van de celcyclus?
- Vrouwelijke mangoesten helpen hun pups door rivalen te verdrijven
- Hoe maak je een glad endoplasmatisch reticulum uit klei
- Federale overheid:geen lijst van bedreigde soorten voor walrus
- Verborgen biosfeer ontdekt onder de droogste hete woestijn ter wereld
- Oud skelet onthult amputatie-operatie 31.000 jaar geleden
- Nieuwe technologie voor enzymontwerp
- Wetenschappers bouwen zeer nauwkeurig moleculair watermodel met behulp van machine learning

- Video:Is uw katalysator gestolen? Dit is waarom

- Spontane synthese van homogene polymeernetwerken

- Beeldvorming van mRNA precies daar waar het is gemaakt - op de plaats van vertaling
 Docenten melden zwakkere relaties met gekleurde leerlingen, kinderen van immigranten
Docenten melden zwakkere relaties met gekleurde leerlingen, kinderen van immigranten Hoe Exponents
Hoe Exponents Wat doen we met plastic?
Wat doen we met plastic? Waarom is een atoom elektrisch neutraal?
Waarom is een atoom elektrisch neutraal?  Op triazine gebaseerde, grafietkoolstofnitride als nieuwe tweedimensionale halfgeleider
Op triazine gebaseerde, grafietkoolstofnitride als nieuwe tweedimensionale halfgeleider Neural Lander gebruikt AI om drones soepel te laten landen
Neural Lander gebruikt AI om drones soepel te laten landen Wat consumenten bedoelen als ze zeggen dat uw producten authentiek zijn
Wat consumenten bedoelen als ze zeggen dat uw producten authentiek zijn Team maakt hoogwaardig grafeen met sojabonen
Team maakt hoogwaardig grafeen met sojabonen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

