
Wetenschap
Onderzoekers observeren het oplossen van zout op atomair niveau
Een onderzoeksteam, aangesloten bij UNIST, heeft een baanbrekende prestatie geleverd door de oplossing van zout in water op atomair niveau te observeren en experimenteel het onderliggende principe bloot te leggen.
Onder leiding van professor Hyung-Joon Shin en zijn onderzoekers van de afdeling Materials Science and Engineering van UNIST introduceerde het team de innovatieve 'single ion control technology'. Deze baanbrekende aanpak maakt de nauwkeurige manipulatie van individuele watermoleculen mogelijk om selectief specifieke ionen uit zout te extraheren.
De bevindingen van het onderzoek zijn gepubliceerd in Nature Communications op 16 maart 2024.
Zout, samengesteld uit robuuste ionische bindingen tussen natriumkationen (Na + ) en chlooranionen (Cl - ), ondergaat een transformatief proces wanneer het in water wordt ondergedompeld. De interactie tussen de positieve en negatieve polariteiten van watermoleculen verstoort de binding tussen de natrium- en chloorionen, wat leidt tot hun scheiding en de vorming van zout water.
Hoewel het principe van het oplossen van zout in water eenvoudig lijkt, hebben eerdere studies dit fenomeen voornamelijk theoretisch onderzocht. Het vermogen om experimenteel te bevestigen welke ionen het eerst in water oplossen en het mechanisme op te helderen waarmee watermoleculen de ionische bindingen van zout verzwakken, was tot nu toe ongrijpbaar gebleven. Professor Shin merkte op:"De uitdaging lag in de ingewikkelde aard van het bestuderen en controleren van individuele ionen te midden van de dynamische beweging van opgeloste ionen in water."
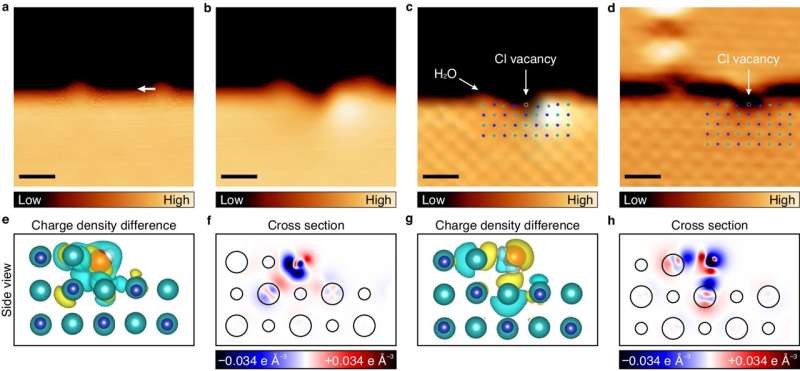
In een zorgvuldig gecontroleerd experiment, uitgevoerd in cryogene en ultrahoogvacuümomstandigheden bij -268,8 °C, plaatste het onderzoeksteam een watermolecuul op een dun zoutmembraan dat uit twee tot drie atomaire lagen bestond. Met behulp van een scanning tunneling microscoop (STM) die metingen op atomaire schaal kon uitvoeren, observeerde het team een minieme hoogteverandering van 10 picometer (pm) terwijl watermoleculen horizontaal over het zoutmembraan werden gemanoeuvreerd. Deze waarneming werd toegeschreven aan de sterke interactie tussen chlooranionen en watermoleculen.
Door watermoleculen strategisch langs de zoutfilm te bewegen met verschillende atomaire diktes, hebben de onderzoekers met succes de verdwijning van een chlooranion van zijn pad teweeggebracht. De polariteit van watermoleculen speelde een cruciale rol bij het verbreken van de ionische binding van zout, waardoor het chlooranion vóór het natriumkation tevoorschijn kwam.
Het team benadrukte verder dat de polarisatiesnelheid van chlooranionen, die twintig keer zo uitgesproken zijn als die van natriumkationen, ze zeer gevoelig maakt voor externe elektrische veranderingen veroorzaakt door watermoleculen. Deze verhoogde responsiviteit was vooral duidelijk in gebieden waar atomen onvoldoende binding met de omringende omgeving hadden.
Huijun Han (Combined MS/Ph.D. Program of Materials Science and Engineering, UNIST), de hoofdauteur van het artikel, verklaarde:"Hoewel het theoretische begrip van het smelten van zout in water al lang bekend is, is ons succes bij het extraheren van afzonderlijke ionen via nauwkeurige controle van watermoleculen betekent een belangrijke experimentele doorbraak."
"Ionen spelen een cruciale rol bij het veranderen van de prestaties van batterijen en halfgeleidermaterialen", benadrukte professor Shin. "Wij voorzien het gebruik van de technologie voor de controle van afzonderlijke ionen om fundamentele technologieën met betrekking tot ionenfunctionaliteiten te bevorderen."