
Wetenschap
Berekeningen van scheikundigen kunnen de voorspelling van kanker bevorderen
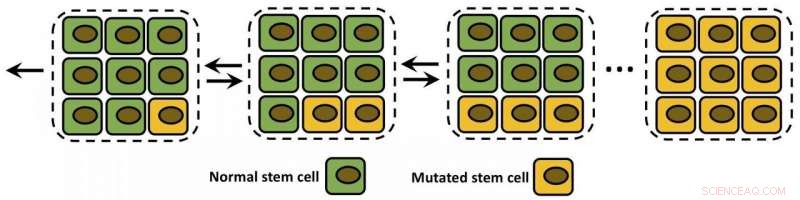
Een schema toont een enkelvoudig mutatiefixatieproces in een weefselcompartiment. Normale stamcellen zijn groen, en gemuteerde cellen zijn geel. Rice University-onderzoekers gebruikten een stochastisch model in discrete toestand om te zien hoe naar kanker neigende mutaties de waarschijnlijkheid beïnvloedden dat cellen weefsel in een tumor veranderen, en hoe goed het model correleert met veelgebruikte berekeningen van kankerrisico's. Krediet:Hamid Teimouri/Rice University
Wanneer veranderen kankergevoelige cellen in volwaardige kanker? Een wetenschapper van Rice University en zijn collega geloven dat er een manier is om erachter te komen.
Het kan mogelijk worden voor biomarkers in bloed om te onthullen of gemuteerde cellen een hoek hebben omgeslagen in de richting van het vormen van tumoren, en hoe lang het proces - afhankelijk van het type kanker - waarschijnlijk zal duren. Dat zou patiënten een idee kunnen geven van het risico dat ze lopen voordat ze ziek worden.
Rijstchemicus Anatoly Kolomeisky, met postdoctoraal onderzoeksmedewerker Hamid Teimouri en afgestudeerde alumna Maria Kochugaeva, richtten hun theoretische expertise in het modelleren van willekeurige (stochastische) processen op het probleem waarom kankercellen die gewoonlijk worden vernietigd door het immuunsysteem van het lichaam, soms een handschoen van verdediging overwinnen om tumoren te worden.
De studie in Wetenschappelijke rapporten is bedoeld om microscopische aspecten van kankerinitiatie te verduidelijken, het punt waarop willekeurige mutaties "vast" worden in cellen, die ze doorgeven en uiteindelijk het weefsel overweldigen.
Als onderdeel van hun studie hebben de onderzoekers berekenden fixatiewaarschijnlijkheden voor 28 soorten kanker om te zien hoe ze correleren met beschikbare klinische gegevens over de risico's van kanker tijdens het leven - en ontdekten dat correlatie allesbehalve zeker was.
"Het probleem met kanker is dat we het te laat ontdekken, " zei Kolomeisky, een professor in de chemie en voorzitter van de afdeling in Rice's Wiess School of Natural Sciences. De onderzoekers stellen hun "handige, eenvoudige en veelzijdige" methode om de dynamiek van kankerinitiatie te evalueren, moet de initiatiedynamiek voor specifieke kankertypes omvatten, evenals vastgestelde levenslange risico's.
Kolomeisky heeft een lange staat van dienst op het gebied van ontdekkingen met betrekking tot cellulaire mechanismen, vooral gerelateerd aan motoreiwitten die vracht in cellen vervoeren en genoombewerking. Geïnspireerd door een terloopse opmerking van een collega dat zijn berekeningen eruit zagen alsof ze verband konden houden met kanker, Kolomeisky ging op pad om uit te zoeken of zijn wiskundige benadering kon worden toegepast op de dynamiek van kankerinitiatie.
Op basis van hun formules, de onderzoekers ontwikkelden een grafiek die levenslange risico's en aanvangstijden correleerde voor 28 soorten kanker - en vonden heel weinig om de twee met elkaar te verbinden. "Het geeft aan dat de levenslange risico's van kanker alleen niet kunnen worden gebruikt om het risico op het krijgen van kanker te evalueren, ’ schreven de onderzoekers, suggereren dat fixatietijden die wijzen op tumorinitiatie een belangrijkere maatstaf zijn.
Bijvoorbeeld, de grafiek laat zien dat colorectaal adenocarcinoom met FAP het hoogste levenslange risico met zich meebrengt, maar de fixatietijd van 15 jaar is bijna drie keer die van duodenumadenocarcinoom met FAP, waarvan wordt gedacht dat het een veel lager levenslang risico heeft. Aan het andere uiteinde van de fixatieschaal bevinden zich hepatocellulaire carcinomen, op meer dan 31, 000 jaar.
Hun berekeningen vergeleken de "fitheid" van individuele cellen met kankergerelateerde mutaties met normale cellen zonder, en hoe snel ze verdeelden. Weefsel met mutante cellen die zich in een 1-op-1-verhouding met normale cellen deelden, waren de langzaamste om tumoren te "repareren".
De onderzoekers gingen ervan uit dat gemuteerde cellen met een snelheidsvoordeel tumoren sneller zouden herstellen, en ze hadden gelijk. Maar ze waren verrast toen hun modellen aantoonden dat cellen met nadelige mutaties (langzamer dan normale deling) ook af en toe sneller dan normale cellen te repareren waren.
"Mensen gaan ervan uit, meestal onbewust, dat iets waarschijnlijkers sneller zal gebeuren, " Zei Kolomeisky. "Maar we ontdekten dat dat niet het geval is voor kankers. Artsen moeten niet alleen beslissingen nemen over levenslange risico's, zoals gewoonlijk wordt gedaan, maar ook op de dynamiek die we als onze belangrijkste resultaten hebben berekend.
"De belangrijkste punten zijn dat we kunnen berekenen, met veel aannames, de gemiddelde tijd voordat kanker begint, " zei hij. "Wij stellen ook dat de waarschijnlijkheid van kanker niet typisch goed met de tijd correleert het begint. Iets waarschijnlijkers is niet per se snel."
Mutante cellen die biomarkers aan de bloedbaan afgeven, kunnen een betere manier zijn om precancereuze aandoeningen te herkennen.
"In de toekomst, dit kan onderdeel worden van gepersonaliseerde geneeskunde, ' zei Kolomeisky. 'Een dokter geeft je een test en controleert de fractie gemuteerde cellen in je weefsels.
Dan kun je inschatten hoe lang het duurt voordat de gemuteerde cellen het hele weefsel innemen. Als het 100 jaar is, je moet je waarschijnlijk niet al te veel zorgen maken. Maar als het een jaar is, dan moet je misschien drastische maatregelen nemen."
Hij zei dat het model zeker zal verbeteren naarmate er meer relevante parameters worden opgenomen. Maar alles wat het nu en in de toekomst produceert, mag iemand niet afschrikken van een gezonde levensstijl.
"We zeggen niet dat je wel of geen kanker krijgt, wat je ook doet, ' zei Kolomeisky. 'Alleen de kans is anders. Als je rookt, als u niet goed eet of niet sport, de kans zal groter zijn."
 Nieuwe online tool om circulair ecodesign te verbeteren
Nieuwe online tool om circulair ecodesign te verbeteren Ultradunne transparante zilverfilms voor zonnecellen
Ultradunne transparante zilverfilms voor zonnecellen Het nieuwe groene alternatief voor de productie van medicijnen
Het nieuwe groene alternatief voor de productie van medicijnen Wat zijn de effecten van koken en vriezen op enzymactiviteit?
Wat zijn de effecten van koken en vriezen op enzymactiviteit?  Een betere zoutvanger bouwen:wetenschappers synthetiseren een moleculaire kooi om chloride op te vangen
Een betere zoutvanger bouwen:wetenschappers synthetiseren een moleculaire kooi om chloride op te vangen
 Britse olie- en gasreserves gaan misschien maar tien jaar mee, studie suggereert:
Britse olie- en gasreserves gaan misschien maar tien jaar mee, studie suggereert: Zachte koralen bij Maagdeneilanden herstellen van orkanen, maar steenkoralen nemen af
Zachte koralen bij Maagdeneilanden herstellen van orkanen, maar steenkoralen nemen af Hoe groeit schimmel op kaas?
Hoe groeit schimmel op kaas?  Technologie kan bodemherstel na olielozingen helpen versnellen
Technologie kan bodemherstel na olielozingen helpen versnellen De poolgebieden van de aarde communiceren via oceanische ansichtkaarten, sfeervolle sms-berichten
De poolgebieden van de aarde communiceren via oceanische ansichtkaarten, sfeervolle sms-berichten
Hoofdlijnen
- Wat zijn enkele kenmerken van DNA?
- Hoe werken Mexicaanse springbonen?
- Wat gebeurt er als dieren geïsoleerd evolueren?
- Nieuwe soorten ontdekt in Maleisisch regenwoud tijdens ongekende, onderzoek van boven naar beneden
- DNA-onderzoek in de Stille Oceaan onthult een toename van 2000 procent in onze kennis van de biodiversiteit van weekdieren
- Wat zijn de twee processen die ATP produceren?
- Unicorn Root herleeft zichzelf na 130 jaar
- De effecten van temperatuur op enzymactiviteit en biologie
- Onderzoekers identificeren moleculaire motor die chromosomen transformeert
 COVID een jaar later:ongelijkheden en zorgen over terugkeer naar de werkplek worden duidelijker
COVID een jaar later:ongelijkheden en zorgen over terugkeer naar de werkplek worden duidelijker Hoe echte volumes te berekenen in Excel
Hoe echte volumes te berekenen in Excel Nano-software biedt verbeterde bescherming voor zowel werknemers als de industrie
Nano-software biedt verbeterde bescherming voor zowel werknemers als de industrie Hoe ruimteregeling werkt
Hoe ruimteregeling werkt  Netflix voegt 9,6 miljoen abonnees toe in het eerste kwartaal naarmate de concurrentie heviger wordt
Netflix voegt 9,6 miljoen abonnees toe in het eerste kwartaal naarmate de concurrentie heviger wordt Duidelijke taal over gezondheidsgegevens is essentieel voor transparantie en vertrouwen
Duidelijke taal over gezondheidsgegevens is essentieel voor transparantie en vertrouwen Trump vertelt NASA om Amerikanen naar de maan te sturen
Trump vertelt NASA om Amerikanen naar de maan te sturen Wetenschappers vinden krachtig potentieel wapen om antibioticaresistentie te overwinnen
Wetenschappers vinden krachtig potentieel wapen om antibioticaresistentie te overwinnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com






