
Wetenschap
Lichtgewicht van periodiek systeem speelt grote rol in het leven op aarde
Krediet:Panimoni/Shutterstock.com
Hoewel waterstof het lichtgewicht is van de chemische elementen, het pakt echt uit als het gaat om zijn rol in het leven en zijn potentieel als oplossing voor enkele van de uitdagingen van de wereld. Terwijl we de 150ste verjaardag van het periodiek systeem vieren, het lijkt redelijk om onze hoed hiervoor te kantelen, het eerste element op tafel.
Waterstof is het meest voorkomende element in het heelal, maar niet op aarde vanwege het lichte gewicht, waardoor het gas gewoon de ruimte in kan drijven. Waterstof is essentieel voor ons leven – het voedt de zon, die elke seconde honderden miljoen ton waterstof omzet in helium. En twee waterstofatomen zijn vastgemaakt aan één zuurstofatoom om water te maken. Beide dingen maken onze planeet bewoonbaar.
Niet alleen stelt waterstof de zon in staat de aarde te verwarmen en het water te creëren dat het leven in stand houdt, maar deze eenvoudigste van alle elementen kan ook de sleutel zijn tot het vinden van een schone brandstofbron om de planeet van energie te voorzien.
Yin en yang van waterstof als energiebron
Net als veel andere chemische elementen, hoewel waterstof voor ons van onschatbare waarde is, het heeft ook een donkere kant. Lichter zijn dan lucht, het laat dingen drijven, daarom werd het gebruikt in vroege luchtschepen. Maar waterstof is zeer explosief, en in 1937 explodeerde het Duitse luchtschip de Hindenburg bij zijn poging om met zijn meermast aan te meren na een transatlantische reis, 36 mensen vermoord.
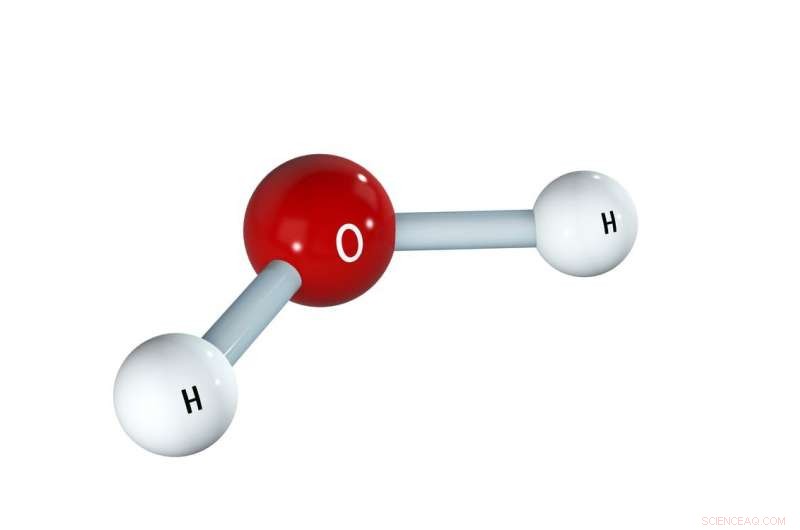
Eén zuurstofatoom is verbonden met twee waterstofatomen om water te maken. Krediet:Liaskovskaia Ekaterina/SHutterstock.com
neven van waterstof, deuterium en tritium, zware waterstof genoemd, zijn gebruikt om waterstofbommen te maken. Hier, de zware waterstofatomen smelten samen in een proces dat kernfusie wordt genoemd om helium te maken, een beetje zoals de reactie die plaatsvindt in de zon. De hoeveelheid energie die door dit proces wordt geproduceerd, is groter dan enig ander bekend proces - het gebied in het midden van de explosie is in wezen verdampt, schokgolven genereren die alles op hun weg vernietigen. Het heldere witte licht dat wordt geproduceerd, kan mensen op vele kilometers afstand verblinden. Het produceert ook radioactieve producten die in de lucht worden vervoerd en wijdverbreide besmetting van het milieu veroorzaken.
Het beest temmen, echter, zou de oplossing kunnen zijn voor de energieproblemen van de toekomst. Bij verbranding op een gecontroleerde manier, waterstof biedt de schoonste brandstof, alleen water als afvalproduct produceren. Dat is verfrissend in vergelijking met een benzinemotor die klimaatverandering veroorzaakte kooldioxide en een reeks andere vervelende gassen produceert. Bij opslag onder hoge druk en zeer lage temperatuur van -400 graden Fahrenheit, waterstof bestaat als een vloeistof, en de verbranding ervan met zuurstof wordt gebruikt om raketten de ruimte in te stuwen.
Echter, een auto met een tank zeer explosieve waterstofraketbrandstof klinkt niet als een veilige gok. Er is momenteel veel onderzoek gericht op het oplossen van het opslagprobleem. Grote aantallen wetenschappers proberen chemische verbindingen te ontwikkelen die waterstof veilig vasthouden en afgeven. Dit is eigenlijk een harde noot om te kraken en het kost tijd en veel geweldige geesten om op te lossen.
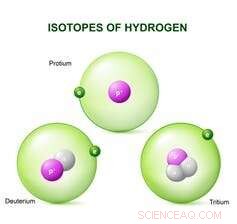
Isotopen van waterstof:protium, deuterium en tritium. Krediet:Designua/Shutterstock.com
De kracht van waterstof
Waterstofatomen geven ook dingen als citroensap en azijn hun kenmerkende zure smaak. Positief geladen waterstofatomen, protonen genoemd, ontdaan van hun enige elektron, drijven rond in deze oplossingen en zijn het belangrijkste bestanddeel van zuren. De chemie van deze protonen is ook verantwoordelijk voor het aansturen van fotosynthese, het proces waarbij planten lichtenergie omzetten in chemische energie, en het aandrijven van vele processen in het menselijk lichaam.
Protonen zijn ook het belangrijkste onderdeel van brandstofcellen. In plaats van de waterstof te verbranden, brandstofcellen zetten het om in elektriciteit en worden gezien als de weg van de toekomst. Dit doen ze door het waterstofgas aan één kant van de brandstofcel te splitsen in protonen en elektronen. De positief geladen protonen gaan naar de andere kant van de cel, waarbij de negatief geladen elektronen achterblijven. Dit creëert een stroom van elektriciteit tussen de zijkanten van de cel wanneer deze is aangesloten op een extern circuit. Deze stroom kan een elektromotor aandrijven die in dit circuit is geplaatst. In Duitsland rijden al treinen op waterstof, en verschillende internationale autofabrikanten ontwikkelen brandstofcelaangedreven auto's. Opnieuw, het enige bijproduct van het proces is water.
In de toekomst, Ik denk dat we een toenemend gebruik van waterstof als brandstof zullen zien. Om nuttig te zijn, er zijn twee grote uitdagingen. Een grote is het opslagprobleem. Ingenieurs moeten uitzoeken hoe ze waterstof veilig kunnen opslaan en beginnen met het bouwen van plaatsen waar mensen kunnen tanken. Met snelle vooruitgang in chemie en techniek, waterstofstations zouden binnenkort kunnen verschijnen, worden net zo gewoon als benzinetankstations tegenwoordig zijn. Dit soort infrastructuur zal essentieel zijn. U wilt niet zonder brandstof komen te zitten tijdens een reis omdat, in tegenstelling tot een auto op gas, je kunt geen vriend bellen om je een bus waterstof te brengen.

Dit is het symbool en elektronendiagram voor waterstof. Krediet:BlueRingMedia/Shutterstock.com
De andere uitdaging is het verkrijgen van de waterstof zelf. Er is heel weinig natuurlijk voorkomend waterstofgas voor ons beschikbaar omdat het omhoog en uit de atmosfeer drijft. In plaats daarvan, het moet van een andere bron worden gemaakt en worden vastgelegd.
Momenteel, het grootste deel van 's werelds waterstof wordt geproduceerd uit hout of uit fossiele brandstoffen, zoals aardgas en olie. Dit verslaat het doel dat het een schone energiebron is. De grootste bron van waterstof is de veiligste, meest gemakkelijk beschikbare vloeistof op aarde:water. Als wij chemici manieren kunnen vinden om watermoleculen af te breken om de waterstofatomen eruit te halen, dit zou een enorme stap voorwaarts zijn.
Dit artikel is opnieuw gepubliceerd vanuit The Conversation onder een Creative Commons-licentie. Lees het originele artikel. 
 Recordbrekende bosbranden in Californië overtreffen 4 miljoen hectare
Recordbrekende bosbranden in Californië overtreffen 4 miljoen hectare Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen
Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie
Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie De onbedoelde gevolgen van voorraden:voedselverspilling
De onbedoelde gevolgen van voorraden:voedselverspilling Overstromingen in Indonesië doden 29, dozijn vermist
Overstromingen in Indonesië doden 29, dozijn vermist
Hoofdlijnen
- Wat zijn de algemene kenmerken van Monerans?
- Puin van de tsunami van 2011 bracht honderden soorten over de Stille Oceaan
- Verouderd DNA kan genen anders activeren
- Saharastof:het goede,
- Hoeveel onontdekte wezens zijn er in de oceaan?
- Natuurbeschermers moeten het Hollywood-effect benutten om dieren in het wild te helpen
- Evolutie van parasietvirussen geeft aan hoe Leishmania voor het eerst gewervelde dieren heeft geïnfecteerd
- Epigenetische reostaat onthult hoe genregulatie wordt geërfd en onderhouden
- Waarom zetten we de radio zachter als we verdwaald waren?
- Rood, wit maar zelden blauw - de wetenschap van vuurwerkkleuren, uitgelegd

- Video:Waarom wordt kunstmest gebruikt in explosieven?

- Eriochrome Black T Solution Preparation

- Onderzoekers gebruiken schuifkrachten om zelf-geassembleerde supramoleculaire hydrogel te maken

- Recente vorderingen in de optimalisatie van gedispergeerde platinakatalysatoren

 Hoe te weten of een stof een reductiemiddel of een oxidatiemiddel is door het periodiek systeem?
Hoe te weten of een stof een reductiemiddel of een oxidatiemiddel is door het periodiek systeem?  Op lucht levende microben een wereldwijd fenomeen
Op lucht levende microben een wereldwijd fenomeen Ecotax verdedigde, omstreden en nog steeds marginaal in de EU
Ecotax verdedigde, omstreden en nog steeds marginaal in de EU Hoe maak je een Roterend Zonnestelselproject voor School
Hoe maak je een Roterend Zonnestelselproject voor School Verschillen tussen codering en sjabloonstrengen
Verschillen tussen codering en sjabloonstrengen  Amerikaanse universiteiten domineren de wetenschappelijke Nobels
Amerikaanse universiteiten domineren de wetenschappelijke Nobels Afbeelding:Nieuw Europees rack geleverd aan ISS
Afbeelding:Nieuw Europees rack geleverd aan ISS Universiteiten moeten leren van beoordelingsmethoden die tijdens de pandemie worden gebruikt - en voorgoed minder examens doen
Universiteiten moeten leren van beoordelingsmethoden die tijdens de pandemie worden gebruikt - en voorgoed minder examens doen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Norway | Swedish | Danish |

-
Wetenschap © https://nl.scienceaq.com

