
Wetenschap
Een betere zoutvanger bouwen:wetenschappers synthetiseren een moleculaire kooi om chloride op te vangen
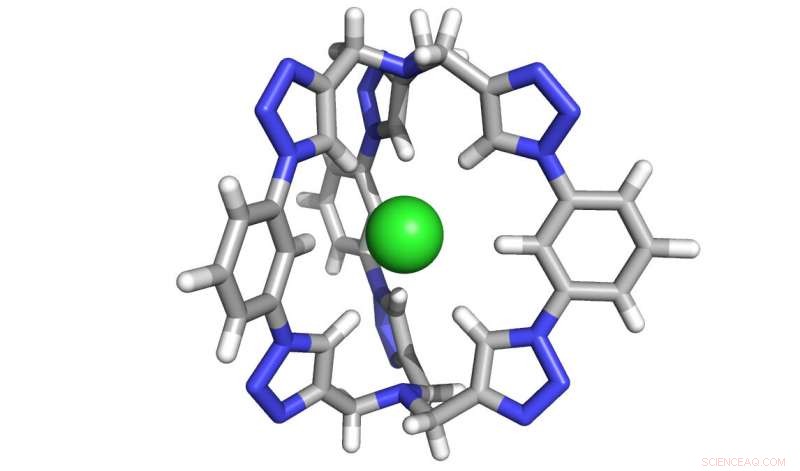
Een computerweergave van de zes-triazoolmolecuulkooi ontworpen om chloridezouten op te vangen. Krediet:Yan Liu, Universiteit van Illinois in Urbana-Champaign
Onderzoekers van de Universiteit van Indiana hebben een krachtig nieuw molecuul gemaakt voor de extractie van zout uit vloeistof. Het werk heeft de potentie om de hoeveelheid drinkbaar water op aarde te helpen vergroten.
Gebouwd met behulp van chemische bindingen die voorheen als te zwak werden beschouwd, het nieuwe molecuul is ongeveer tien miljard keer verbeterd in vergelijking met een vergelijkbare structuur die meer dan 10 jaar geleden bij IU werd gecreëerd. Het ontwerp van de moleculen werd op 23 mei gerapporteerd in het tijdschrift Wetenschap .
"Als je een miljoenste van een gram van dit molecuul in een ton water zou plaatsen, 100 procent van hen zal nog steeds in staat zijn om een zout te vangen, " zei Yun Liu, die de studie leidde als een Ph.D. student in het lab van Amar Flood, de James F. Jackson Professor of Chemistry en Luther Dana Waterman Professor in de IU Bloomington College of Arts and Sciences' Department of Chemistry.
Het molecuul is ontworpen om chloride op te vangen, die wordt gevormd wanneer het element chloor paren met een ander element om een elektron te krijgen. Het meest bekende chloridezout is natriumchloride, of gewoon keukenzout. Andere chloridezouten zijn kaliumchloride, calciumchloride en ammoniumchloride.
Terwijl de menselijke bevolking blijft groeien, het sijpelen van zout in zoetwatersystemen vermindert de toegang tot drinkbaar water over de hele wereld. Alleen al in de VS, de U.S. Geological Survey schat 271 ton opgeloste vaste stoffen, inclusief zouten, komen per jaar in zoetwaterstromen. Factoren die bijdragen zijn onder meer de chemische processen die betrokken zijn bij oliewinning, het gebruik van strooizout en waterontharders, en de natuurlijke verwering van gesteente. Er is maar één theelepel zout nodig om vijf liter water permanent te vervuilen.
Het nieuwe zoutextractiemolecuul dat bij IU is gemaakt, bestaat uit zes triazool-"motieven" - vijfledige ringen bestaande uit stikstof, koolstof en waterstof - die samen een driedimensionale "kooi" vormen die perfect is gevormd om chloride op te vangen. In 2008, Flood's lab creëerde een tweedimensionaal molecuul, in de vorm van een platte donut, die vier triazolen gebruikten. De twee extra triazolen geven het nieuwe molecuul zijn driedimensionale vorm, en een tien miljardvoudige toename van de werkzaamheid.
Het molecuul is ook uniek omdat het chloride bindt met behulp van koolstof-waterstofbindingen, voorheen beschouwd als te zwak om stabiele interacties met chloride te creëren in vergelijking met het traditionele gebruik van stikstof-waterstofbindingen. Ondanks de verwachtingen, de onderzoekers ontdekten dat het gebruik van triazolen een kooi creëerde die zo stijf was dat er een vacuüm in het midden ontstond, die chloride-ionen aantrekt.

Yun Liu heeft een 3D-geprint model van het zes-triazoolmolecuul dat is ontworpen om chloridezouten op te vangen. Krediet:Fred Zwicky, Universiteit van Illinois in Urbana-Champaign.
Daarentegen, kooien met stikstof-waterstofbindingen zijn vaak flexibeler - en het vacuümachtige centrum dat nodig is voor het opvangen van chloride vereist energietoevoer, het verlagen van hun efficiëntie in vergelijking met een op triazool gebaseerde kooi.
"Als je ons molecuul zou nemen en het zou opstapelen tegen andere kooien die [sterkere] bindingen gebruiken, we hebben het over veel ordes van grootte van prestatieverhoging, " zei Flood. "Deze studie toont echt aan dat rigiditeit ondergewaardeerd wordt in het ontwerp van moleculaire kooien."
De stijfheid zorgt er ook voor dat het molecuul zijn vorm behoudt nadat het centrale chloride verloren is gegaan, in vergelijking met andere ontwerpen die onder dezelfde omstandigheden bezwijken vanwege hun flexibiliteit. Dit geeft het molecuul een grotere werkzaamheid en veelzijdigheid.
Het werk is ook reproduceerbaar. Het eerste molecuul duurde bijna een jaar om te synthetiseren, zei Liu, die geschokt was om de kristallen te ontdekken die nodig zijn om de unieke structuur van het molecuul te bevestigen, gevormd nadat het experiment enkele maanden alleen in het laboratorium was gelaten - een verrassende gebeurtenis omdat dit proces doorgaans zorgvuldige monitoring vereist.
De vorming van het kristal vertegenwoordigde een "eureka" -moment, bewijzen dat het unieke ontwerp van het molecuul echt levensvatbaar was. Later, Wei Zhao, een postdoctoraal onderzoeker in het laboratorium van Flood, was in staat om het molecuul in enkele maanden opnieuw te creëren.
 Onderzoekers fabriceren transparant keramiek van hoge kwaliteit
Onderzoekers fabriceren transparant keramiek van hoge kwaliteit Duurzaam transport:de lucht zuiveren met stikstofdoping
Duurzaam transport:de lucht zuiveren met stikstofdoping Hoe droog ijs te maken voor mist
Hoe droog ijs te maken voor mist  Simulaties maken het mogelijk om stereochemie te kiezen voor je eigen avontuur
Simulaties maken het mogelijk om stereochemie te kiezen voor je eigen avontuur Er kan zich nieuwe substantie vormen in het georiënteerde aanhechtingsproces van kristalgroei, studie onthult
Er kan zich nieuwe substantie vormen in het georiënteerde aanhechtingsproces van kristalgroei, studie onthult
 Zelfgemaakt skeletmodel
Zelfgemaakt skeletmodel  Water stroomt over Antarctica:uit nieuw onderzoek blijkt dat vloeistofstroom wijdverspreider is dan gedacht
Water stroomt over Antarctica:uit nieuw onderzoek blijkt dat vloeistofstroom wijdverspreider is dan gedacht Hoe beïnvloeden grote waterlagen het klimaat van de kustgebieden?
Hoe beïnvloeden grote waterlagen het klimaat van de kustgebieden?  Afbeelding:Sharm El Sheikh
Afbeelding:Sharm El Sheikh Het snel bevolkte kustgebied van de Golf tot Pakistan wordt geconfronteerd met een enorm tsunami-risico
Het snel bevolkte kustgebied van de Golf tot Pakistan wordt geconfronteerd met een enorm tsunami-risico
Hoofdlijnen
- Hoe de darmbacteriën van honingbijen helpen bij het verteren van hun stuifmeelrijke voeding
- Is Rust Dust schadelijk?
- Genen dicteren niet altijd dat jongens jongens zullen zijn
- Noorwegen zet hek op om rendierslachting te stoppen
- Genomisch onderzoek onthult aanwijzingen voor het wilde verleden van druiven
- Hoeveel spieren heb je nodig om te glimlachen?
- Hoe is de katoenplant aangepast om te overleven?
- Wetenschappers afluisteren onbekende spitssnuitdolfijnen af om te zien hoe diep ze duiken
- Handelen of niet handelen? De ivoren impasse doorbreken
- Ademanalysator ter grootte van schoenendoos detecteert dodelijke longziekte sneller, nauwkeuriger dan artsen

- De vorm in water:eerste nanoschaalmetingen van het vouwen van biomoleculen in vloeistof
- Ontwikkelen van elektrisch actieve materialen om beschadigde harten te herstellen

- Onderzoekers kwantificeren thermodynamisch samenspel tijdens co-aggregatie van eiwitten
- Wetenschappers identificeren moleculen die cellen hadden kunnen helpen om te overleven - en te gedijen - op de vroege aarde

 NASA-ruimtevaartuig begint 2-jarige reis naar huis met asteroïde puin
NASA-ruimtevaartuig begint 2-jarige reis naar huis met asteroïde puin Sociaaleconomische status voorspelt de ontwikkeling van essentiële denkvaardigheden bij jongens in het VK
Sociaaleconomische status voorspelt de ontwikkeling van essentiële denkvaardigheden bij jongens in het VK Ecosysteem: definitie, types, structuur en voorbeelden
Ecosysteem: definitie, types, structuur en voorbeelden  Na de verwoesting van de cycloon, terug naar af voor Mozambiques Beira
Na de verwoesting van de cycloon, terug naar af voor Mozambiques Beira Hoe intelligente werkstations AI zullen gebruiken om gezondheid en geluk te verbeteren
Hoe intelligente werkstations AI zullen gebruiken om gezondheid en geluk te verbeteren Nieuw onderzoek suggereert dat de wereldwijde ijstijd het gezicht van de planeet heeft veranderd
Nieuw onderzoek suggereert dat de wereldwijde ijstijd het gezicht van de planeet heeft veranderd Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering Wetenschappers ontwikkelen fagocytische protocellen die in staat zijn tot gerichte afgifte van enzymen
Wetenschappers ontwikkelen fagocytische protocellen die in staat zijn tot gerichte afgifte van enzymen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

