
Wetenschap
Een fosfineoxidekatalysator gebruiken om nucleofiele substitutiereacties van alcoholen groener te maken

Krediet:CC0 Publiek Domein
Een team van onderzoekers van de Universiteit van Nottingham, Jealott's Hill International Research Center en de GlaxoSmithKline, Geneesmiddelenonderzoekscentrum, heeft een manier gevonden om een fosfineoxidekatalysator te gebruiken om nucleofiele substitutiereacties van alcoholen groener te maken. In hun artikel gepubliceerd in het tijdschrift Wetenschap , de groep beschrijft hun proces en de voordelen ervan. Lars Longwitz en Thomas Werner van het Leibniz Institute for Catalysis hebben in hetzelfde tijdschriftnummer een Perspective-artikel gepubliceerd waarin het werk van het team wordt beschreven.
Nucleofiele substituties zijn een soort substitutiereactie die wordt gebruikt in de organische chemie - ze omvatten het gebruik van een nucleofiel om een goede vertrekkende groep te vervangen. Dergelijke reacties (Mitsunobu-chemie) worden vaak gebruikt als onderdeel van een proces om een grote verscheidenheid aan commerciële producten te synthetiseren. Longwitz en Werner merken op dat alcoholen doorgaans als nucleofiel worden gebruikt omdat ze goedkoop en gemakkelijk verkrijgbaar zijn. Maar omdat alcoholen niet reageren met pronucleofielen, tenzij ze actief zijn vóór de substitutie, de reactie leidt tot de productie van een ongewenst bijproduct van fosfineoxide - een minder dan schoon resultaat. In deze nieuwe poging de onderzoekers hebben een manier bedacht om dit probleem te vermijden, en bieden dus een veel schonere methode voor het omkeren van de configuratie van alcoholen.
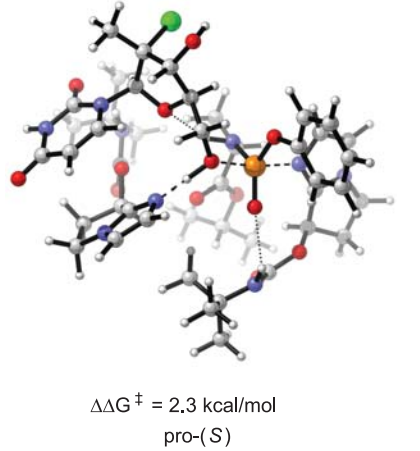
De door de onderzoekers ontwikkelde methode was acht jaar in de maak en omvatte het gebruik van een door het team ontworpen fosfineoxide dat geen reductiemiddelen of oxidanten vereist. De techniek vereist geen azoreagens. Om de fosfineoxidekatalysator te activeren, ze gebruikten zure protonen die bedoeld waren voor de nucleofiel die bij de vervanging werd gebruikt. Volgende, ze hebben de katalysator gedehydrateerd, dwingen het in een ringvormige structuur. Door dit te doen, verbreek je de fosfor-zuurstof dubbele bindingen, die, in eerdere pogingen, blijkt vrij moeilijk te zijn. Hierdoor konden zuurstofmoleculen zich hechten aan de fosforatomen, door de ring open te forceren - en dat stelde de koppelingspartner in staat om het resulterende zout aan te vallen, waaruit het eindproduct is voortgekomen. Het proces produceert niet alleen water als bijproduct, maar regenereert ook de katalysator. Longwitz en Werner suggereren dat de methode een nieuwe weg inslaat naar een meer duurzame organische synthese.
© 2019 Wetenschap X Netwerk
 Onderzoekers ontwikkelen 3D-printsubstraat met dynamische bindingen voor instelbare eigenschappen
Onderzoekers ontwikkelen 3D-printsubstraat met dynamische bindingen voor instelbare eigenschappen Techniek kan het gemakkelijker maken om mRNA te gebruiken om ziekten te behandelen of vaccins af te leveren
Techniek kan het gemakkelijker maken om mRNA te gebruiken om ziekten te behandelen of vaccins af te leveren Dog Science Fair Projectideeën
Dog Science Fair Projectideeën  Hoe een mengsel van zand en zout te scheiden
Hoe een mengsel van zand en zout te scheiden Fotoreversibele moleculaire schakelaar verandert de fysieke eigenschap van thermoresponsief polymeer
Fotoreversibele moleculaire schakelaar verandert de fysieke eigenschap van thermoresponsief polymeer
 5 ideeën om de voedselvoorziening ter wereld te verdubbelen
5 ideeën om de voedselvoorziening ter wereld te verdubbelen  Spanningen van eerdere aardbevingen verklaren de locatie van seismische gebeurtenissen
Spanningen van eerdere aardbevingen verklaren de locatie van seismische gebeurtenissen Ammoniak uit bemeste rijstvelden komt meestal niet in de lucht terecht
Ammoniak uit bemeste rijstvelden komt meestal niet in de lucht terecht Dust Bowl zou de oogst van vandaag verwoesten, studie vondsten
Dust Bowl zou de oogst van vandaag verwoesten, studie vondsten Drie dagen regen in Pakistan doden 90, het leven in Karachi . verstoren
Drie dagen regen in Pakistan doden 90, het leven in Karachi . verstoren
Hoofdlijnen
- Taxonomie (biologie): definitie, classificatie en voorbeelden
- Een ezelsverhaal:Nigeria wordt de belangrijkste exporthub voor verstoppingen
- Hebben alle mensen een uniek genotype en fenotype?
- Onderzoekers voeren een nieuwe analyse van het tarwemicrobioom uit onder vier managementstrategieën
- Bescherming van het wild:professor helpt recreatieverstoring voor dieren in het wild tot een minimum te beperken
- Mariene wetenschappers ontdekken kleptopredatie - een nieuwe manier om prooien te vangen
- Röntgenfoto's van het skelet van Dolly vertonen geen tekenen van abnormale artrose
- Glimlachende menselijke gezichten zijn aantrekkelijk voor honden - dankzij oxytocine
- Is Algae een Decomposer, Scavenger of Producer?
- Efficiënte katalysator ontwikkeld voor het produceren van pronucleotiden
- Nieuwe technologie maakt snelle eiwitsynthese mogelijk

- Onderzoekers vinden nieuwe manier om kankercellen aan te pakken
- Onderzoekers gebruiken groen goud om schadelijke bacteriën snel te detecteren en te identificeren

- Verschil tussen natriumchloride en natriumchloride

 NASA onderzoekt tropische storm Uesis zware regenval
NASA onderzoekt tropische storm Uesis zware regenval Klimaatengineering:internationale bijeenkomst onthult spanningen
Klimaatengineering:internationale bijeenkomst onthult spanningen Onderzoekers vinden eiwit dat antibioticaresistentie kan helpen bestrijden
Onderzoekers vinden eiwit dat antibioticaresistentie kan helpen bestrijden Lage druk vermindert bellenproblemen
Lage druk vermindert bellenproblemen Brandende chili houdt olifanten op afstand, nieuwe studie vondsten
Brandende chili houdt olifanten op afstand, nieuwe studie vondsten Peptidepapieren wijzen op nieuwe manieren om bacteriën aan te pakken
Peptidepapieren wijzen op nieuwe manieren om bacteriën aan te pakken Studies suggereren meer originele migranten naar Australië dan gedacht - en ze kwamen met opzet
Studies suggereren meer originele migranten naar Australië dan gedacht - en ze kwamen met opzet Waarom de productie van giftige methylkwik toenam in een estuarium van de Grote Meren
Waarom de productie van giftige methylkwik toenam in een estuarium van de Grote Meren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

