
Wetenschap
Onderzoekers maken de eerste kaarten van twee melatoninereceptoren die essentieel zijn voor slaap
Het slaapbevorderende hormoon melatonine (weergegeven als een sterrenbeeld aan de nachtelijke hemel) wordt 's nachts gesynthetiseerd uit serotonine (weergegeven als een vlieger), en beide archaïsche moleculen dateren van vóór de dierlijke evolutie. Hoge melatoninespiegels 's nachts stellen het in staat zijn slaapbevorderende eigenschappen vast te stellen door te werken via receptoren met hoge affiniteit, afgebeeld aan de rechterkant van de beeldcompositie. Krediet:Yekaterina Kadyshevskaya, Bridge Institute bij USC Michelson Center for Convergent Bioscience.
Een internationaal team van onderzoekers gebruikte een röntgenlaser bij het SLAC National Accelerator Laboratory van het Department of Energy om de eerste gedetailleerde kaarten te maken van twee melatoninereceptoren die ons lichaam vertellen wanneer het moet gaan slapen of wakker worden en andere biologische processen begeleiden. Een beter begrip van hoe ze werken, zou onderzoekers in staat kunnen stellen betere medicijnen te ontwerpen om slaapstoornissen te bestrijden, kanker en diabetes type 2. Hun bevindingen werden vandaag in twee papers gepubliceerd Natuur .
Het team, geleid door de Universiteit van Zuid-Californië, gebruikte röntgenstralen van SLAC's Linac Coherent Light Source (LCLS) om de receptoren in kaart te brengen, MT1 en MT2, gebonden aan vier verschillende verbindingen die de receptoren activeren:een medicijn tegen slapeloosheid, een medicijn dat melatonine vermengt met het antidepressivum serotonine, en twee melatonine-analogen.
Ze ontdekten dat beide melatoninereceptoren nauwe kanaaltjes bevatten die ingebed zijn in de vetmembranen van de cellen in ons lichaam. Deze kanalen laten alleen melatonine - dat zowel in water als in vet kan voorkomen - door, serotonine blokkeren, die een vergelijkbare structuur heeft, maar alleen gelukkig is in waterige omgevingen. Ze ontdekten ook hoe sommige veel grotere verbindingen mogelijk alleen gericht zijn op MT1 en niet op MT2. ondanks de structurele overeenkomsten tussen de twee receptoren. Dit zou het ontwerp van geneesmiddelen die selectief gericht zijn op MT1 moeten informeren. wat tot nu toe een uitdaging was.
"Deze receptoren vervullen enorm belangrijke functies in het menselijk lichaam en zijn belangrijke doelwitten voor geneesmiddelen die van groot belang zijn voor de farmaceutische industrie, " zei Linda Johansson, een postdoctoraal onderzoeker bij het USC die het structurele werk aan MT2 leidde. "Door dit werk konden we een zeer gedetailleerd inzicht krijgen in hoe melatonine zich aan deze receptoren kan binden."
Bedtijd
Mensen doen het, vogels doen het vissen doen het. Bijna alle levende wezens in het dierenrijk slapen, en met een goede reden.
"Het is van cruciaal belang voor de hersenen om rust te nemen en herinneringen te verwerken en op te slaan die we gedurende de dag hebben verzameld, " zei co-auteur Alex Batyuk, een wetenschapper bij SLAC. "Melatonine is het hormoon dat onze slaap-waakcyclus regelt. Als er licht is, de aanmaak van melatonine wordt geremd, maar als het donker wordt, is dat het signaal voor onze hersenen om te gaan slapen."
Melatoninereceptoren behoren tot een groep membraanreceptoren die G-eiwitgekoppelde receptoren (GPCR's) worden genoemd en die bijna alle fysiologische en sensorische processen in het menselijk lichaam reguleren. MT1 en MT2 worden op veel plaatsen in het lichaam aangetroffen, inclusief de hersenen, netvlies, cardiovasculair systeem, lever, nier, milt en darm..
Deze receptoren houden toezicht op onze klokgenen, de tijdwaarnemers van de interne klok van het lichaam, of circadiaans ritme. In een perfecte wereld, onze interne klokken zouden synchroon lopen met het opkomen en ondergaan van de zon. Maar als mensen door tijdzones reizen, nachtdiensten werken of te veel tijd doorbrengen voor schermen of andere kunstmatige bronnen van blauw licht, deze tijdwaarnemers zijn van slag.
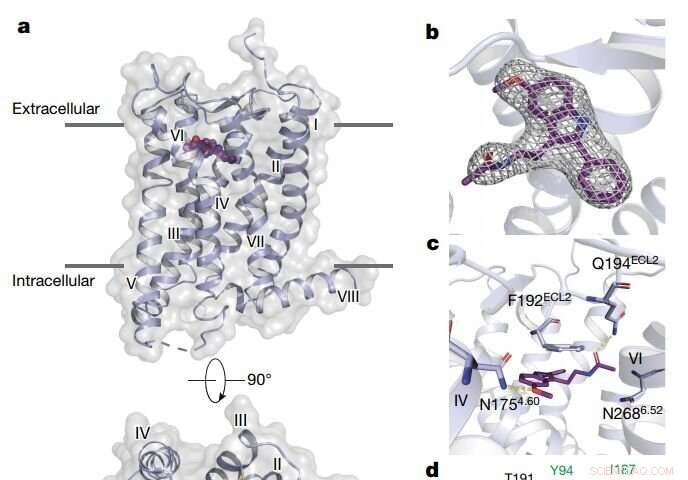
Overzicht van de MT2-structuur. Credit: Natuur (2019). DOI:10.1038/s41586-019-1144-0
Het ritme beheersen
Wanneer onze circadiane ritmes worden verstoord, het kan leiden tot psychiatrische, metabool, oncologische en vele andere aandoeningen. Vooral MT1 speelt een belangrijke rol bij het beheersen van deze ritmes, maar het ontwerpen van medicijnen die zich selectief op deze receptor kunnen richten, is moeilijk gebleken. Veel mensen nemen vrij verkrijgbare melatoninesupplementen om slaapproblemen te bestrijden of hun circadiane ritme te veranderen, maar de effecten van deze medicijnen verdwijnen vaak binnen enkele uren.
Door de blauwdrukken van deze receptoren te kraken en in kaart te brengen hoe liganden eraan binden en ze activeren, de onderzoekers baanden de weg voor anderen om medicijnen te ontwerpen die veiliger zijn, effectiever en in staat om zich selectief op elke receptor te richten.
"Sinds de ontdekking van melatonine 60 jaar geleden, er zijn veel historische ontdekkingen geweest die tot dit moment hebben geleid, " zei Margarita L. Dubocovich, een vooraanstaande SUNY-professor in farmacologie en toxicologie aan de universiteit van Buffalo, die in de vroege jaren 80 pionierde met de identificatie van functionele melatoninereceptoren en een extern perspectief op dit onderzoek verschafte. "Ondanks opmerkelijke vooruitgang, ontdekking van selectieve MT1-medicijnen is ongrijpbaar gebleven voor mijn team en onderzoekers over de hele wereld. De opheldering van de kristalstructuren voor de MT1- en MT2-receptoren opent een opwindend nieuw hoofdstuk voor de ontwikkeling van medicijnen voor de behandeling van slaap- of circadiane ritmestoornissen waarvan bekend is dat ze psychiatrische, metabool, oncologische en vele andere aandoeningen."
Kristallen oogsten
Om biomoleculen zoals eiwitten in kaart te brengen, onderzoekers gebruiken vaak een methode genaamd röntgenkristallografie, het verstrooien van röntgenstralen van gekristalliseerde versies van deze eiwitten en het gebruiken van de patronen die dit creëert om een driedimensionale structuur te verkrijgen. Tot nu, de uitdaging met het in kaart brengen van MT1, MT2- en vergelijkbare receptoren waren hoe moeilijk het was om kristallen te kweken die groot genoeg waren om structuren met een hoge resolutie te verkrijgen.
"Met deze melatoninereceptoren, we moesten echt een stapje extra doen, " zei Benjamin Stauch, die leiding gaf aan de structurele werkzaamheden aan MT1. "Veel mensen hadden geprobeerd ze te kristalliseren zonder succes, dus we moesten een beetje inventief zijn."
Een belangrijk onderdeel van dit onderzoek was de unieke methode die de onderzoekers gebruikten om hun kristallen te laten groeien en er röntgendiffractiegegevens van te verzamelen. Voor dit onderzoek is het team bracht deze receptoren tot expressie in insectencellen en haalde ze eruit met wasmiddel. Ze muteerden deze receptoren om ze te stabiliseren, kristallisatie mogelijk maken. Na het zuiveren van de receptoren, ze plaatsten ze in een membraanachtige gel, die kristalgroei rechtstreeks vanuit de membraanomgeving ondersteunt. Na het verkrijgen van microkristallen gesuspendeerd in deze gel, ze gebruikten een speciale injector om een smalle stroom kristallen te creëren die ze met röntgenstralen van LCLS zapten.
"Vanwege de kleine kristalgrootte, dit werk kon alleen gedaan worden bij LCLS, " zei Vadim Cherezov, een USC-hoogleraar die beide studies begeleidde. "Dergelijke kleine kristallen buigen niet goed af bij synchrotronbronnen, omdat ze snel last hebben van stralingsschade. Röntgenlasers kunnen het probleem van stralingsschade overwinnen door het 'diffractie-voor-destructie'-principe."
De onderzoekers verzamelden honderdduizenden beelden van de verstrooide röntgenstralen om de driedimensionale structuur van deze receptoren te achterhalen. Ze testten ook de effecten van tientallen mutaties om hun begrip van hoe de receptoren werken te verdiepen.
Naast het ontdekken van kleine, poortwachter melatonine kanalen in de receptoren, de onderzoekers waren in staat om type 2 diabetes-geassocieerde mutaties op de MT2-receptor in kaart te brengen, voor het eerst de exacte locatie van deze mutaties in de receptor zien.
De basis te leggen
Bij deze experimenten de onderzoekers keken alleen naar verbindingen die de receptoren activeren, bekend als agonisten. Opvolgen, ze hopen de aan antagonisten gebonden receptoren in kaart te brengen, die de receptoren blokkeren. Ze hopen met hun technieken ook andere GPCR-receptoren in het lichaam te kunnen onderzoeken.
"Als structuurbioloog het was opwindend om voor het eerst de structuur van deze receptoren te zien en ze te analyseren om te begrijpen hoe deze receptoren selectief hun signaalmoleculen herkennen, "Zei Cherezov. "We kennen ze al tientallen jaren, maar tot nu toe kon niemand zeggen hoe ze er in werkelijkheid uitzien. Nu kunnen we ze analyseren om te begrijpen hoe ze specifieke moleculen herkennen, waarvan we hopen dat het de basis legt voor beter, effectievere medicijnen."
 NASA-beelden onthullen Neoguri nu extra-tropisch
NASA-beelden onthullen Neoguri nu extra-tropisch Inkomenspatronen en verstedelijking hebben invloed op de biodiversiteit van zoogdieren in steden
Inkomenspatronen en verstedelijking hebben invloed op de biodiversiteit van zoogdieren in steden Rook van westerse bosbranden veroorzaakt waas aan de oostkust, levendige zonsondergangen
Rook van westerse bosbranden veroorzaakt waas aan de oostkust, levendige zonsondergangen Juridische pot in Californië brengt tal van milieuregels met zich mee
Juridische pot in Californië brengt tal van milieuregels met zich mee Boomringen kunnen de uitbarstingsdatum van de Thera-vulkaan bepalen
Boomringen kunnen de uitbarstingsdatum van de Thera-vulkaan bepalen
Hoofdlijnen
- De meeste zeeschildpadden zijn nu vrouwelijk in het noorden van het Great Barrier Reef
- Virusstamping - een veelzijdige nieuwe methode voor genetische manipulatie van afzonderlijke cellen
- Te veel charisma kan de effectiviteit van een leider schaden
- Kan een Vision Board uw toekomst echt beïnvloeden?
- Hoe HeLa-cellen werken
- Is vissen met elektriciteit minder destructief dan de zeebodem opgraven met boomkorren?
- DNA Extraction by Spooling Method
- Commensalisme: definitie, types, feiten en voorbeelden
- Wat zijn de vier eukaryotische koninkrijken?
- Een nieuw ligand verlengt de halfwaardetijd van peptiden van minuten tot dagen
- De knoestige kwestie van het aroma van zachte krakeling oplossen
- Nieuwe hydrogel benut luchtvochtigheid voor praktische toepassingen
- Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën
- Nieuwe theorie laat zien hoe spanning zorgt voor betere katalysatoren
 SpaceX lanceert vier astronauten naar ISS
SpaceX lanceert vier astronauten naar ISS Steden met meer zwarte inwoners zijn meer afhankelijk van verkeersboetes en boetes voor inkomsten
Steden met meer zwarte inwoners zijn meer afhankelijk van verkeersboetes en boetes voor inkomsten Een op een ballon gebaseerd zonne-observatorium
Een op een ballon gebaseerd zonne-observatorium Methoden voor het testen van PH of Liquids
Methoden voor het testen van PH of Liquids Verwarmt oceaanmaan Enceladus miljarden jaren lang
Verwarmt oceaanmaan Enceladus miljarden jaren lang Directe detectie van circulerende tumorcellen in bloedmonsters
Directe detectie van circulerende tumorcellen in bloedmonsters De weg naar het bereiken van netto nul vloeibare brandstof
De weg naar het bereiken van netto nul vloeibare brandstof Nieuw onderzoek naar een recent ontdekt chlorofylmolecuul kan de sleutel zijn tot betere zonnecellen
Nieuw onderzoek naar een recent ontdekt chlorofylmolecuul kan de sleutel zijn tot betere zonnecellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

