
Wetenschap
Waarom macrofagen rusten in gezond weefsel?
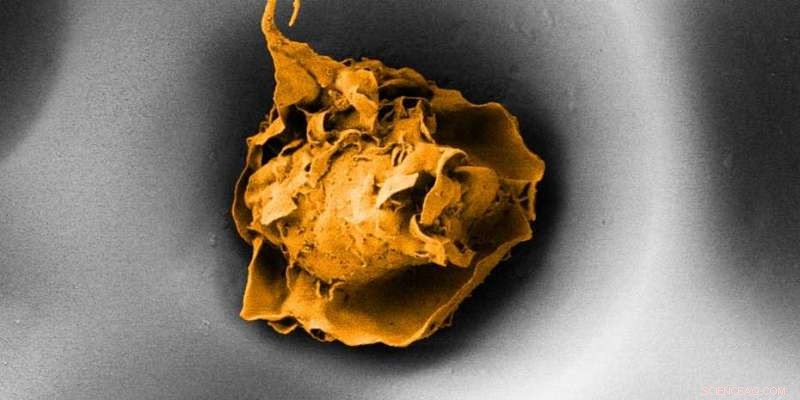
Een macrofaag in een porie van 20 micrometer doorsnee (elektronenmicroscoopopname). Krediet:ETH Zürich / Nikhil Jain en Isabel Gerber
ETH-wetenschappers hebben aangetoond dat de macrofagen van het immuunsysteem niet alleen biochemisch worden gereguleerd, maar ook mechanisch. Dit zou kunnen verklaren waarom de cellen minder actief zijn in gezond lichaamsweefsel.
Macrofagen zijn een soort witte bloedcellen. De term komt uit het Grieks voor "grote eter", die een van de rollen beschrijft die deze cellen in ons lichaam spelen:ze detecteren en verzwelgen pathogene bacteriën, veroorzaakt een ontstekingsreactie die de infectie bestrijdt. Macrofagen worden gereguleerd door cytokinen en andere biochemische stoffen. Deze moleculen stimuleren macrofagen om hun activiteit te verhogen wanneer dat nodig is en om te kalmeren zodra hun werk gedaan is.
altviool Vogel, Hoogleraar bij de afdeling Gezondheidswetenschappen en Technologie, en postdoc Nikhil Jain hebben nu een ander regulerend mechanisme voor pro-inflammatoire macrofagen ontdekt:ruimtelijke informatie. Wanneer macrofagen in het weefsel tussen andere cellen zitten en daardoor worden vernauwd, hun activiteit wordt verlaagd - zelfs als er stimulerende prikkels aanwezig zijn.
Geen onnodige ontstekingsreacties
"Niet alleen circuleren macrofagen in het bloed, ze zijn ook te vinden in alle weefsels van het lichaam. Ze wachten rustig af, als bewakers, totdat ze nodig zijn, " legt Vogel uit. Ze zegt dat het heel belangrijk is voor het lichaam dat in weefsel aanwezige macrofagen inactief blijven, omdat ze anders onnodige ontstekingsreacties zouden kunnen veroorzaken:"Macrofagen hoeven niet te worden geactiveerd totdat het weefsel is beschadigd." Echter, de mechanismen die pro-inflammatoire macrofaagactiviteit in gezonde weefsels dempen, zijn tot nu toe niet volledig begrepen.
Door celkweekexperimenten in het laboratorium uit te voeren, de ETH-wetenschappers hebben kunnen vaststellen dat macrofagen zowel biochemisch als mechanisch worden gereguleerd. Door macrofagen in poriënachtige inkepingen te plaatsen, ze zouden de verspreiding van individuele cellen kunnen beperken.
Deze experimenten stelden de onderzoekers ook in staat om onderliggende moleculaire mechanismen te ontsluiten. De functie van een macrofaag is gebonden aan zijn grootte:als hij wordt geactiveerd, het groeit door zijn cytoskelet uit te breiden. Hierdoor komen factoren vrij die de activiteit van de genen beïnvloeden. De macrofaag, echter, kan niet groeien als het wordt opgesloten door externe barrières.
Ziektes begrijpen en implantaten verbeteren
De ontdekking dat ruimtelijke factoren de activering van macrofagen sturen, heeft grote implicaties voor het begrip van verschillende ziekten. "Veel leeftijdsgerelateerde ziekten zijn geassocieerd met de latente productie van pro-inflammatoire cytokines zoals geproduceerd door onvoldoende gecontroleerde macrofagen, " zegt Vogel. Dit omvat reumatische aandoeningen, atherosclerose, zwaarlijvigheid, kanker en verschillende auto-immuunziekten.
In aanvulling, de ontdekking zal leiden tot nieuwe ideeën over het structureren van de oppervlakken van implantaten om ontstekingen te verminderen. "We laten zien dat de structuur van een materiaaloppervlak de macrofaagrespons beïnvloedt, " zegt Vogel. De volgende stap zou kunnen zijn om te kijken of, bijvoorbeeld, patiënten die implantaten met poreuze oppervlakken krijgen, vormen er minder littekenweefsel omheen, zoals reeds gesuggereerd door enkele eerdere waarnemingen.
Hoofdlijnen
- Marmoset-baby's krijgen een boost van attente vaders
- Symbiose en celevolutie:Lynn Margulis en de oorsprong van eukaryoten
- Waarom krijgen demonen de schuld van slaapverlamming?
- Een buitengewoon grotdier gevonden in Oost-Turkmenistan
- Apenstudie toont een pad naar het monitoren van bedreigde diersoorten
- Embryonale ontwikkeling van een kikker
- Centriolen:je kunt cellen niet verdelen zonder ze
- Indonesië's selfiesnagende aap uitgeroepen tot Persoon van het Jaar
- Hibernerende ribosomen helpen bacteriën te overleven
- Stoffen gezichtsmaskers die kunnen worden gedesinfecteerd door zonlicht

- Een nieuwe kruiskoppeling vereenvoudigt de synthese van medicijnachtige moleculen

- Gebruik maken van de slagvastheid van 's werelds hardste beton voor rampenpreventie
- Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden

- Het dieet van zijderupsen veranderen om sterkere zijde te spinnen

 Schoolproject: Hoe maak je een vulkaan die de as blaast
Schoolproject: Hoe maak je een vulkaan die de as blaast  Google had Zero-Day redenen om over updates te schreeuwen
Google had Zero-Day redenen om over updates te schreeuwen Onderzoekers ontwikkelen nieuwe methode om nanodevices te controleren
Onderzoekers ontwikkelen nieuwe methode om nanodevices te controleren Student test HoloLens voor NASA, krijgt een nadere blik op het oppervlak van Mars
Student test HoloLens voor NASA, krijgt een nadere blik op het oppervlak van Mars Major State of the Planet-rapport voorafgaand aan de eerste Nobelprijstop
Major State of the Planet-rapport voorafgaand aan de eerste Nobelprijstop Hoe RPM naar lineaire snelheid wordt geconverteerd
Hoe RPM naar lineaire snelheid wordt geconverteerd Overstromingsrisico's:Nauwkeurigere gegevens door COVID-19
Overstromingsrisico's:Nauwkeurigere gegevens door COVID-19 Nieuwe 3D-röntgentechniek onthult geheimen van binnenuit botten
Nieuwe 3D-röntgentechniek onthult geheimen van binnenuit botten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


