Wetenschap
Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert
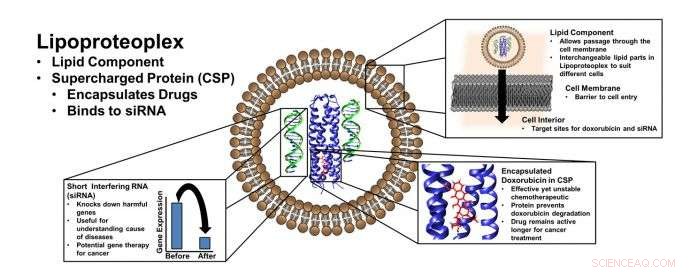
Lipoproteoplex gebruikt een lipide "container" voor transfectie - het transport van materiaal langs een celmembraan - en een gemakkelijk te maken eiwitcapsule die zowel kleine moleculen chemotherapeutische medicijnen als genetische technologie kan binden, zoals kort interfererend RNA (siRNA), dat genen kan "stilzetten" die ziektetoestanden voortplanten. Krediet:NYU Tandon School of Engineering
Clinici hebben tegenwoordig een arsenaal van meer dan 200 medicijnen tot hun beschikking voor de behandeling van een reeks kankers - alleen al tussen 2011 en 2016 werden 68 medicijnen goedgekeurd. Maar veel chemotherapeutische middelen vormen een hardnekkige uitdaging:ze veroorzaken ernstige bijwerkingen omdat ze naast kankercellen ook gezonde cellen doden; sommige vormen van kanker ontwikkelen resistentie tegen medicijnen; en veel van dergelijke chemotherapieën, slecht oplosbaar in water, lage biologische beschikbaarheid aantonen, resulterend in suboptimale medicijnafgifte aan kankercellen.
Een mogelijke oplossing ligt in de synergetische combinatie van een chemotherapeutisch medicijn met gemanipuleerd genetisch materiaal dat is ontworpen om de kwaadaardige genen te neutraliseren die resistentie tegen dat medicijn verlenen, onder andere functies.
Hoewel er talloze voorbeelden zijn van synthetische voertuigen voor het afleveren van twee genen en medicijnen, nieuwe hybride materialen die in het laboratorium van de NYU Tandon School of Engineering zijn ontwikkeld, maken gebruik van gemakkelijk aanpasbare eiwitten om een chemische een-tweetje te leveren:ze combineren een lipide "container" voor transfectie - het transport van lading langs een celmembraan - en een gemakkelijk om een eiwitcapsule te maken die zowel kleine chemotherapeutische moleculen als nucleïnezuren kan binden.
Ontwikkeld door een team onder leiding van NYU Tandon Associate Professor of Chemical and Biomolecular Engineering Jin Kim Montclare - die ook dienst doet als Affiliate Professor of Chemistry aan NYU's College of Arts and Sciences, en een aangesloten hoogleraar biomaterialen aan het NYU College of Dentistry, en tevens verbonden aan SUNY Downstate als hoogleraar biochemie - het hybride lipide-eiwitmateriaal, een lipoproteoplex genoemd, omvat zowel een opgerold supercharged eiwitmacromolecuul als een in de handel verkrijgbaar transfectiemiddel genaamd Lipofectamine 2000.
Omdat de onderzoekers het eiwitmacromolecuul ontwikkelden met uitgebreide positieve ladingen op het oppervlak en een hydrofobe kern, het kan gemakkelijk worden versierd met negatief geladen kort interfererend RNA (siRNA) - een krachtig hulpmiddel voor het onderdrukken van genen die resistentie tegen geneesmiddelen oproepen en ziektetoestanden verspreiden - terwijl het ook dient als een efficiënt, en toxiciteit verminderend, carryall voor het hydrofobe chemotherapeutische middel doxorubicine.
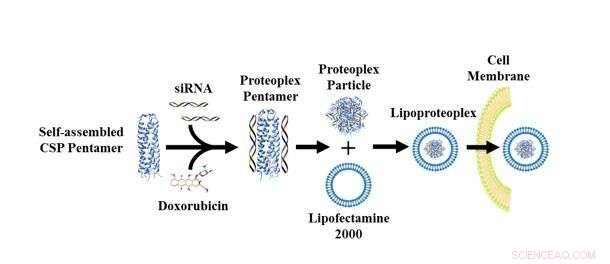
Lipoproteoplex stelt onderzoekers in staat om een supercharged eiwit- of lipidecomponent en een willekeurig aantal siRNA uit te wisselen om een specifieke cellijn en type medicijn aan te pakken. Krediet:NYU Tandon School of Engineering
In onderzoek gepubliceerd in Biomacromoleculen , een tijdschrift van de American Chemical Society, het team beschrijft hoe de lipoproteoplex die werd blootgesteld aan monsters van de MCF-7-borstkankercellijn meer doxorubicine aan de doelcellen afleverde dan Lipofectamine 2000 alleen, resulterend in een aanzienlijke afname van de levensvatbaarheid van MCF-7-cellen. Ze toonden ook aan dat het hybride macromolecuul zeer succesvol was bij siRNA-transfectie, het gen met 60 procent tot zwijgen brengen.
Montclare zei dat een belangrijk voordeel van de nieuwe lipoproteoplex het gemak van modificatie is, een aanwinst voor onderzoekers die cellen bestuderen waarvan het genetisch aangeroepen gedrag in de loop van de tijd verandert en verschilt per cellijn en patiënt. Eerder als een systeem van mix-and-match componenten, de lipoproteoplex stelt onderzoekers in staat om een supercharged eiwit- of lipidecomponent en een willekeurig aantal siRNA uit te wisselen om een specifieke cellijn en type medicijn aan te pakken.
"In tegenstelling tot andere bezigheden bij het produceren van dubbele gen- en medicijnafgiftesystemen, deze benadering vereist geen vervelende chemische syntheseprocedures; in plaats daarvan kunnen we elke variant van het supercharged eiwit biosynthetiseren, " zei ze. "Dit maakt het mogelijk om verschillende siRNA-moleculen en chemotherapeutische medicijnen te vervangen om aan de laboratoriumbehoeften te voldoen."
In recent werk aan op eiwit gebaseerde hybride materialen, Montclare en haar medewerkers combineerden een ontwikkeld supercharged eiwit met het transfectiereagens Fugene. De combinatie vertoonde een achtvoudige verbetering in transfectie-efficiëntie van DNA vergeleken met Fugene alleen, met verwaarloosbare cytotoxiciteit.
Montclare onderzoekt de mechanismen die ervoor zorgen dat deze lipoproteoplexen effectief genen en medicijnen over verschillende cellijnen kunnen afleveren.
 Gluten in tarwe:wat is er veranderd in 120 jaar fokken?
Gluten in tarwe:wat is er veranderd in 120 jaar fokken? Science Projects on Hair Dye
Science Projects on Hair Dye Onderzoek wijst op ethische inkoop van materialen voor moderne technologie
Onderzoek wijst op ethische inkoop van materialen voor moderne technologie Wetenschappers automatiseren de analyse van de elektrolytsamenstelling voor de productie van aluminium
Wetenschappers automatiseren de analyse van de elektrolytsamenstelling voor de productie van aluminium School Science Projects voor junioren
School Science Projects voor junioren
 India verwijdert 27 zeer giftige pesticiden
India verwijdert 27 zeer giftige pesticiden Trump EPA zal naar verwachting de normen voor autogaskilometers terugdraaien
Trump EPA zal naar verwachting de normen voor autogaskilometers terugdraaien Waarom COVID-19 onze steden misschien niet zoveel verandert als we verwachten
Waarom COVID-19 onze steden misschien niet zoveel verandert als we verwachten Storm Elsa trekt over Straat van Florida na bestorming van Cuba
Storm Elsa trekt over Straat van Florida na bestorming van Cuba Onderzoek toont aan hoe stadslandbouw de duurzaamheid van Phoenix kan stimuleren
Onderzoek toont aan hoe stadslandbouw de duurzaamheid van Phoenix kan stimuleren
Hoofdlijnen
- Boomklimmende gekko's die smallere zitstokken gebruiken, hebben langere ledematen dan verwacht
- Wat is apoptose?
- Hoe een PCR-primer te ontwerpen
- CRISPR gebruiken om warmer te maken, minder vette varkens
- Gemengde organisatie van darmbacteriën wordt onthuld door microbioombeeldvormingstechnologie
- Nieuw type stamcellijn geproduceerd biedt uitgebreide mogelijkheden voor onderzoek en behandelingen
- Trucs voor het onthouden van dierenfylum
- Tagged slakken om onderzoekers te helpen de groei van de slakkenpopulatie te volgen
- Nieuwe high-throughput sequencing-technologieën onthullen een wereld van op elkaar inwerkende micro-organismen
 Gesmolten zee-ijs Alaska alarmeert kustbewoners, wetenschappers
Gesmolten zee-ijs Alaska alarmeert kustbewoners, wetenschappers Antarctica stevent af op een klimaatomslagpunt tegen 2060, catastrofaal smelten als de CO2-uitstoot niet snel wordt verminderd?
Antarctica stevent af op een klimaatomslagpunt tegen 2060, catastrofaal smelten als de CO2-uitstoot niet snel wordt verminderd? Wat is voltage in een batterij?
Wat is voltage in een batterij?  De fysica lezen die zich in gegevens verstopt
De fysica lezen die zich in gegevens verstopt Consumenten keren misschien niet terug naar oude productkeuzes zodra de financiën verbeteren
Consumenten keren misschien niet terug naar oude productkeuzes zodra de financiën verbeteren Nieuwe halfgeleider is veelbelovend voor 2D-fysica en elektronica
Nieuwe halfgeleider is veelbelovend voor 2D-fysica en elektronica Nieuwe Raman-methode vangt doelmoleculen actief in kleine openingen
Nieuwe Raman-methode vangt doelmoleculen actief in kleine openingen Adviseurs niet genoeg om een sterk pensioen te garanderen
Adviseurs niet genoeg om een sterk pensioen te garanderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com