
Wetenschap
De asymmetrische synthese van gehalogeneerde verbindingen uit carbonzuren is wereldprimeur
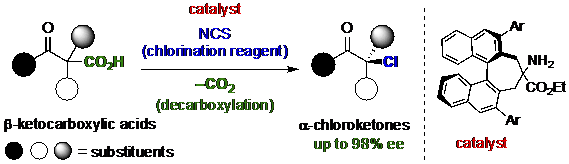
De decarboxylatieve chlorering van β-ketocarbonzuren. Krediet:(c) Toyohashi University of Technology
Toyohashi University of Technology-onderzoekers onder leiding van universitair hoofddocent Shibatomi ontwikkelden een nieuwe katalytische reactie om chloorbevattende organische moleculen te produceren in isomeerzuivere (links- of rechtshandige) vorm
Moleculen hebben geen handen, maar sommige zijn links- of rechtshandig. Veel chemische verbindingen vertonen een eigenschap die chiraliteit wordt genoemd, waar twee versies - bekend als enantiomeren - bestaan voor hetzelfde molecuul. Hoewel hun atomen in precies dezelfde volgorde zijn verbonden, de twee enantiomeren zijn verschillende spiegelbeelden, als een paar handen.
Enantiomeren kunnen heel verschillende eigenschappen hebben. Bijvoorbeeld, alleen de rechtshandige vorm van glucose geeft je energie - de linkshandige isomeer kan niet worden gemetaboliseerd, ook al smaakt het hetzelfde. Veel geneesmiddelen zijn ook chiraal, en vaak heeft slechts één enantiomeer een medicinaal gebruik. Daarom, scheikundigen die aan complexe moleculen werken, hebben verschillende trucs ontwikkeld om de zuiverheid van isomeren te garanderen. Echter, voor sommige reacties blijft dit een uitdaging.
Nutsvoorzieningen, het onderzoeksteam heeft een reactie ontwikkeld om een belangrijke klasse verbindingen in zuivere links- of rechtshandige vorm te produceren. Organohalogeniden zijn moleculen waarin een halogeen, zoals chloor, is gebonden aan koolstof. Velen zijn te vinden in de natuur, of gebruikt in de geneeskunde. Ze kunnen worden geproduceerd uit een andere familie van verbindingen, carbonzuren, door simpelweg een zuur te vervangen door een halogeen. Helaas, als de doelverbinding chiraal is, deze substitutie produceert links- en rechtshandige isomeren in gelijke hoeveelheden.
Het onderzoeksteam van de Toyohashi University of Technology loste dit probleem op door de reactie te katalyseren met een katalysator die zelf chiraal is. Vandaag de dag, Katalysatoren zijn er in een breed scala aan vormen en maten, die vaak wedijveren met de complexiteit van het eigenlijke doelmolecuul. "We hebben een breed scala aan chirale katalysatoren gescreend, zoals Lewiszuur, Bronsted zuur, en Lewis-base-katalysatoren, " hoofdauteur van de studie Kazutaka Shibatomi zegt. "Eindelijk, we vonden een amine dat ons organohalogeniden gaf met een enantiomere zuiverheid tot 98% - ook al was ons uitgangsmateriaal een 50/50 mengsel."
De gechloreerde producten, bekend als chloorketonen, zijn bouwstenen voor belangrijkere chirale moleculen zoals geneesmiddelen. Omdat chloor slechts zwak aan koolstof gebonden is, het kan gemakkelijk worden vervangen door een ander atoom om een nieuw molecuul te maken. Met behulp van een van de vele verbindingen die door hun nieuwe reactie in enantiomere zuiverheid zijn geproduceerd, het onderzoeksteam synthetiseerde Cathinone, een natuurlijk stimulerend middel.
"De vervanging verloopt op een eenvoudige, klassieke manier, Associate Prof. Shibatomi zegt. "Terwijl chloor het molecuul aan de ene kant verlaat, de inkomende groep nadert van de andere kant. De chiraliteit van het product hangt gewoon af van de rangschikking van deze atomen, dus als je begint met een zuivere enantiomeer, je behoudt die zuiverheid. Dit zou een hele klasse verbindingen kunnen openen die voorheen een grote uitdaging waren om als pure enantiomeren te produceren."
 "What Are Oxidants?
"What Are Oxidants? Nieuwe chemische methode maakt het gemakkelijker om vervuilende pesticiden uit water te halen
Nieuwe chemische methode maakt het gemakkelijker om vervuilende pesticiden uit water te halen Fidget spinner als centrifuge scheidt bloedplasma
Fidget spinner als centrifuge scheidt bloedplasma Radicale diagnostiek kan miljoenen mensen redden die het risico lopen te overlijden aan bloedverlies
Radicale diagnostiek kan miljoenen mensen redden die het risico lopen te overlijden aan bloedverlies Wat zijn de twee belangrijkste componenten van een atoom?
Wat zijn de twee belangrijkste componenten van een atoom?
 Wat heeft geleid tot meer extreme zomerhitte-evenementen in Noordoost-Azië?
Wat heeft geleid tot meer extreme zomerhitte-evenementen in Noordoost-Azië? Groen geld, CO2-belasting:wat te verwachten op klimaatbijeenkomst in Parijs
Groen geld, CO2-belasting:wat te verwachten op klimaatbijeenkomst in Parijs Klimaatverandering en economische consumptie
Klimaatverandering en economische consumptie De sluiting maakt de lucht in New York vrij, maar raak niet te opgewonden, geochemicus zegt:
De sluiting maakt de lucht in New York vrij, maar raak niet te opgewonden, geochemicus zegt: Klimaat in een zoetwaterbiomeer
Klimaat in een zoetwaterbiomeer
Hoofdlijnen
- Boomklimmende gekko's die smallere zitstokken gebruiken, hebben langere ledematen dan verwacht
- Verschrikkelijke sneeuwman? Nee - studie koppelt DNA-monsters van vermeende Yeti's aan Aziatische beren
- Hoe worden restrictie-enzymen gebruikt in de biotechnologie?
- Hoe is zuurstof belangrijk voor de afgifte van energie in de celademhaling?
- Een buitengewoon grotdier gevonden in Oost-Turkmenistan
- Nieuwe transdisciplinaire studie onthult microben die op een dag een grote druivenziekte kunnen afschrikken
- Structuur van het spierstelsel
- Ver van harpoenen, walvissen schitteren in de boom van ecotoerisme in IJsland
- Conserveringsonderzoek gebruikt kleine loopbanden om het uithoudingsvermogen van de zeeschildpadden te testen
- Onthulling van de regels achter de constructie van virussteigers
- Welke dranken barsten van het umami-potentieel?

- Wetenschappers ontwerpen een betere methode om moleculen te bouwen die medicijnen zouden kunnen zijn - in de helft van de stappen
- Wetenschap op het raakvlak:bio-geïnspireerde materialen onthullen nuttige eigenschappen

- Een duurzamere manier om metalen te raffineren

 Continue bodemvruchtbaarheidsmonitor kan de landbouw ten goede komen
Continue bodemvruchtbaarheidsmonitor kan de landbouw ten goede komen Astronomen leggen sterrenwinden in ongekend detail vast
Astronomen leggen sterrenwinden in ongekend detail vast Team bereikt chemische reacties met twee elektronen met behulp van lichtenergie, goud
Team bereikt chemische reacties met twee elektronen met behulp van lichtenergie, goud Afbeelding:visualisatie van de voorgestelde tempel bovenop Shackleton Crater
Afbeelding:visualisatie van de voorgestelde tempel bovenop Shackleton Crater Afbeelding:Gigantische magnetische touwen in een halo van sterrenstelsels
Afbeelding:Gigantische magnetische touwen in een halo van sterrenstelsels Voor een overstroomd Midwesten, klimaatvoorspellingen bieden weinig troost
Voor een overstroomd Midwesten, klimaatvoorspellingen bieden weinig troost De rol van microben in afvalrecycling
De rol van microben in afvalrecycling  Grootschalige geïntegreerde schakelingen geproduceerd in de drukpers
Grootschalige geïntegreerde schakelingen geproduceerd in de drukpers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

