
Wetenschap
Hoe een smalspectrumantibioticum zich richt op C. difficile
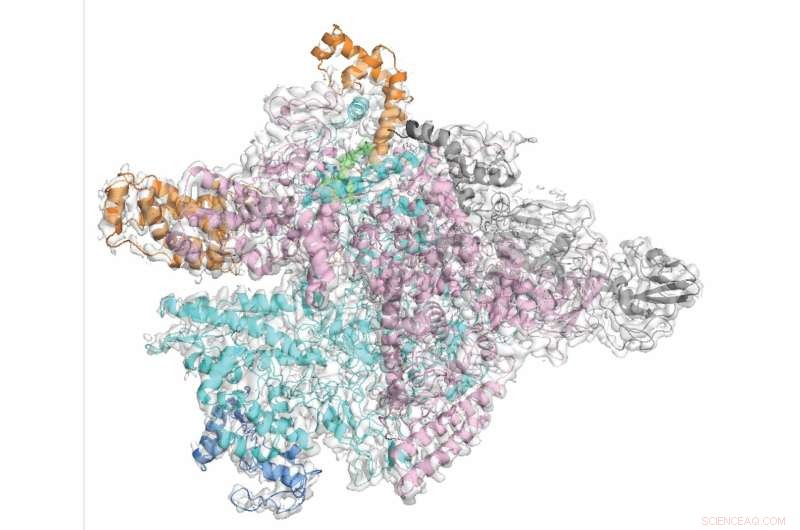
De onderzoekers toonden op moleculair niveau aan hoe fidaxomicine zich selectief richt op C. diff terwijl de onschuldige bacteriële omstanders worden gespaard. Krediet:de Rockefeller-universiteit
De meeste antibiotica zijn tweesnijdende zwaarden. Naast het doden van de ziekteverwekker waarvoor ze zijn voorgeschreven, decimeren ze ook nuttige bacteriën en veranderen ze de samenstelling van het darmmicrobioom. Als gevolg hiervan worden patiënten vatbaarder voor herinfectie en is de kans groter dat er resistente stammen ontstaan.
Het antwoord op dit probleem zou kunnen zijn smalspectrumantibiotica die slechts één of enkele soorten bacteriën doden, waardoor het risico op nevenschade wordt geminimaliseerd. In een recent onderzoek hebben Rockefeller-wetenschappers een dergelijk antibioticum, fidaxomicine, onder de loep genomen, dat wordt gebruikt voor de behandeling van Clostridium difficile, of C. diff, een van de meest voorkomende zorginfecties. De onderzoekers toonden op moleculair niveau aan hoe fidaxomicine zich selectief richt op C. diff, terwijl de onschuldige bacteriële omstanders worden gespaard.
De bevindingen, gedetailleerd in Natuur , zou wetenschappers kunnen helpen in de race om nieuwe smalspectrumantibiotica te ontwikkelen tegen andere pathogenen.
"Ik wil dat mensen, wetenschappers en artsen anders over antibiotica denken", zegt Elizabeth Campbell, universitair hoofddocent onderzoek bij Rockefeller. "Aangezien ons microbioom cruciaal is voor de gezondheid, spelen benaderingen met een smal spectrum een belangrijke rol bij de behandeling van bacteriële infecties in de toekomst."
Enigmatisch selectief
C. diff is een toxine-producerende bacterie die de dikke darm kan doen ontsteken en ernstige diarree kan veroorzaken. Het infecteert ongeveer een half miljoen mensen in de Verenigde Staten, meestal in een ziekenhuisomgeving, en ongeveer één op de elf van de 65-plussers sterft binnen een maand.
Jarenlang hebben artsen breedspectrumantibiotica gebruikt om C. diff te behandelen. Fidaxomicine is een relatief nieuw alternatief dat in 2011 door de FDA is goedgekeurd.
Net als verschillende andere antibiotica, waaronder het tuberculose-medicijn rifampicine, richt fidaxomicine zich op een enzym genaamd RNA-polymerase (RNAP), dat de bacterie gebruikt om zijn DNA-code in RNA te transcriberen. Om precies te begrijpen waarom fidaxomicine RNAP selectief remt in C. diff en niet in de meeste andere bacteriën, werkte Campbell samen met biochemicus Robert Landick van de Universiteit van Wisconsin-Madison om C. diff RNAP te visualiseren met behulp van cryo-elektronenmicroscopie, een krachtige beeldvormingstechniek die kan de 3D-vorm van moleculen onthullen en het medicijnmolecuul en zijn doelwit in actie vastleggen. "Hoewel de algemene architectuur van RNAP in verschillende bacteriën vergelijkbaar is, zijn er nog steeds aanzienlijke verschillen", zegt Campbell.
RNAP bespioneren
Een grote uitdaging was echter om eerst grote hoeveelheden C. diff te produceren, een anaërobe kiem die niet groeit in aanwezigheid van zuurstof. De eerste auteur van de studie, Xinyun Cao, van het Landick Lab, heeft twee jaar lang een systeem ontwikkeld om C. diff RNAP gemakkelijker te produceren met behulp van E. Coli, een gemakkelijk groeiende bacterie die vaak in het laboratorium wordt gebruikt.
Met behulp van dit materiaal genereerde co-eerste auteur Hande Boyaci, een postdoc in Campbell's team, afbeeldingen van C. diff RNAP vergrendeld met fidaxomicine met een bijna-atomaire resolutie. Ingeklemd in een scharnier tussen twee subeenheden van RNAP, opent fidaxomicine de tang van het enzym, waardoor het niet in genetisch materiaal kan grijpen en het transcriptieproces kan starten.
Bij het nauwkeurig onderzoeken van de contactpunten tussen RNAP en fidaxomicine, identificeerden de onderzoekers één aminozuur op het RNAP dat bindt aan fidaxomicine, maar afwezig is in de belangrijkste groepen darmmicroben die worden gespaard door fidaxomicine. Een genetisch gewijzigde versie van C. diff die dit aminozuur miste, werd niet gestoord door fidaxomicine, net als andere commensale bacteriën in de darm. Omgekeerd werden bacteriën die het aan hun RNAP hadden toegevoegd gevoelig voor fidaxomicine.
De bevindingen suggereren dat dit ene aminozuur van de 4.000 aminozuren van deze robuuste en essentiële transcriptiemachine de achilleshiel is, die verantwoordelijk is voor het doden van de bacteriën door fidaxomicine.
De benadering die in deze studie wordt gebruikt, stelt een routekaart voor om nieuwe en veiligere antibiotica te ontwikkelen, zeggen de onderzoekers. Door de RNAP-structuur van diverse bacteriën verder op te helderen, kunnen wetenschappers antibiotica ontwerpen die zich selectiever en effectiever op elke ziekteverwekker richten.
 Boterachtige smeersels gezonder maken
Boterachtige smeersels gezonder maken Geen trial-and-error meer bij het kiezen van een elektrolyt voor metaal-luchtbatterijen
Geen trial-and-error meer bij het kiezen van een elektrolyt voor metaal-luchtbatterijen Welke elementen maken glucose
Welke elementen maken glucose  Elektrochemische reactie stimuleert nieuwe medicijnontdekkingen
Elektrochemische reactie stimuleert nieuwe medicijnontdekkingen Proton vaste oxide elektrolytische cel vergemakkelijkt niet-geoxideerde dehydrogenering van ethaan
Proton vaste oxide elektrolytische cel vergemakkelijkt niet-geoxideerde dehydrogenering van ethaan
Hoofdlijnen
- Hoe een DNA-monster wordt verzameld en voorbereid voor onderzoek
- Kan slapen met een hersenschudding je doden?
- Hoe het uitsterven van de dinosauriërs de evolutie van planten veranderde
- Stamcelvaccins: de nieuwe grens in kankertherapie?
- De vier eigenschappen van spiercellen
- Hoe spreken felle kleuren kinderen aan?
- Het grootste deel van het graasland voor rendieren staat onder cumulatieve druk
- Hoe verbeteren microscopen ons leven vandaag?
- Leef snel, sterf jong:signaaldetectietheorie bijwerken
- Hoe telomeren werken
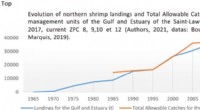
- Hoe kan een op coöperaties gebaseerde organisatie van inheemse visserij de veerkracht van afnemende bestanden bevorderen?
- Kan Nieuw-Zeeland de nationale beschermingsinspanningen ter bestrijding van plaagzoogdieren coördineren?

- Te veel zon is niet goed - voor mensen of planten

- Stamcellen die vetweefsel genereren, hebben een circadiane klok

 Nucleïnezuren: structuur, functie, typen en voorbeelden
Nucleïnezuren: structuur, functie, typen en voorbeelden  Eenvoudig proces voor tweezijdige nanomaterialen kan helpen bij energie, informatietechnologie
Eenvoudig proces voor tweezijdige nanomaterialen kan helpen bij energie, informatietechnologie Een multi-representatieve convolutionele neurale netwerkarchitectuur voor tekstclassificatie
Een multi-representatieve convolutionele neurale netwerkarchitectuur voor tekstclassificatie Japan begint kosten in rekening te brengen voor plastic zakken
Japan begint kosten in rekening te brengen voor plastic zakken Studie laat zien hoe mens en natuur significante veranderingen teweegbrengen in de gezondheid van mondiale rivieren
Studie laat zien hoe mens en natuur significante veranderingen teweegbrengen in de gezondheid van mondiale rivieren Zelfrijdende platforms van Waymo om Google-vracht te vervoeren
Zelfrijdende platforms van Waymo om Google-vracht te vervoeren Jura-dinosaurus met vogelschild was een van de eersten die in kuddes leefde
Jura-dinosaurus met vogelschild was een van de eersten die in kuddes leefde Surface defect engineering van nanodraadarrays naar efficiënte stikstofreductie voor ammoniaksynthese
Surface defect engineering van nanodraadarrays naar efficiënte stikstofreductie voor ammoniaksynthese
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

