
Wetenschap
Het geheim van een langere levensduur? Genregulatie houdt een aanwijzing in
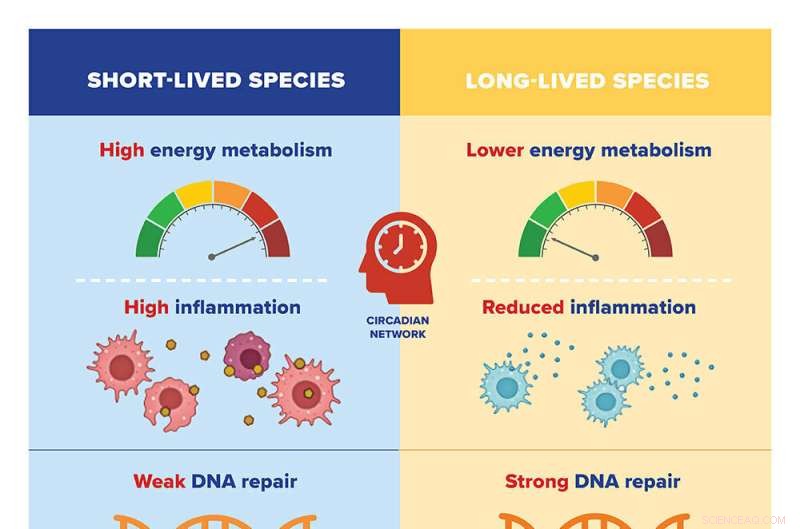
Bij het vergelijken van de genexpressiepatronen van 26 soorten met verschillende levensduur, ontdekten Rochester-biologen Vera Gorbunova en Andrei Seluanov dat de kenmerken van de verschillende genen werden gecontroleerd door circadiane of pluripotentienetwerken. Credit:illustratie Universiteit van Rochester / Julia Joshpe
Natuurlijke selectie heeft zoogdieren voortgebracht die in dramatisch verschillende snelheden verouderen. Neem bijvoorbeeld naakte molratten en muizen; de eerste kan tot 41 jaar oud worden, bijna tien keer zo lang als knaagdieren van vergelijkbare grootte zoals muizen.
Wat zorgt voor een langere levensduur? Volgens nieuw onderzoek van biologen van de Universiteit van Rochester ligt een belangrijk stukje van de puzzel in de mechanismen die genexpressie reguleren.
In een paper gepubliceerd in Cell Metabolism , de onderzoekers, waaronder Vera Gorbunova, de Doris Johns Cherry-hoogleraar biologie en geneeskunde; Andrei Seluanov, hoogleraar biologie en geneeskunde; en Jinlong Lu, een postdoctoraal onderzoeksmedewerker in het laboratorium van Gorbunova en de eerste auteur van het artikel, onderzocht genen die verband houden met de levensduur. Hun onderzoek bracht specifieke kenmerken van deze genen aan het licht en onthulde dat twee regulerende systemen die genexpressie controleren - circadiane en pluripotentienetwerken - van cruciaal belang zijn voor een lang leven. De bevindingen hebben implicaties voor zowel het begrip van hoe de levensduur evolueert als voor het bieden van nieuwe doelen om veroudering en aan leeftijd gerelateerde ziekten te bestrijden.
Levensduurgenen vergelijken
De onderzoekers vergeleken de genexpressiepatronen van 26 zoogdiersoorten met verschillende maximale levensduur, van twee jaar (spitsmuizen) tot 41 jaar (naakte molratten). Ze identificeerden duizenden genen die verband houden met de maximale levensduur van een soort en die positief of negatief waren gecorreleerd met een lang leven.
Ze ontdekten dat langlevende soorten vaak een lage expressie hebben van genen die betrokken zijn bij energiemetabolisme en ontsteking; en hoge expressie van genen die betrokken zijn bij DNA-herstel, RNA-transport en organisatie van cellulair skelet (of microtubuli). Eerder onderzoek door Gorbunova en Seluanov heeft aangetoond dat kenmerken zoals efficiënter DNA-herstel en een zwakkere ontstekingsreactie kenmerkend zijn voor zoogdieren met een lange levensduur.
Het tegenovergestelde gold voor kortlevende soorten, die de neiging hadden om een hoge expressie te hebben van genen die betrokken zijn bij energiemetabolisme en ontsteking en een lage expressie van genen die betrokken zijn bij DNA-herstel, RNA-transport en de organisatie van microtubuli.
Twee pijlers van een lang leven
Toen de onderzoekers de mechanismen analyseerden die de expressie van deze genen reguleren, ontdekten ze dat er twee belangrijke systemen in het spel waren. De negatieve levensduurgenen - die betrokken zijn bij het energiemetabolisme en ontstekingen - worden gecontroleerd door circadiane netwerken. Dat wil zeggen, hun expressie is beperkt tot een bepaald tijdstip van de dag, wat kan helpen de algehele expressie van de genen in langlevende soorten te beperken.
Dit betekent dat we op zijn minst enige controle kunnen uitoefenen over de negatieve levensduurgenen.
"Om langer te leven, moeten we een gezond slaapschema aanhouden en 's nachts blootstelling aan licht vermijden, omdat dit de expressie van de negatieve levensduurgenen kan verhogen", zegt Gorbunova.
Aan de andere kant worden positieve levensduurgenen - die betrokken zijn bij DNA-herstel, RNA-transport en microtubuli - gecontroleerd door wat het pluripotentienetwerk wordt genoemd. Het pluripotentienetwerk is betrokken bij het herprogrammeren van somatische cellen - alle cellen die geen reproductieve cellen zijn - in embryonale cellen, die gemakkelijker kunnen verjongen en regenereren, door DNA opnieuw te verpakken dat gedesorganiseerd raakt naarmate we ouder worden.
"We ontdekten dat evolutie het pluripotentienetwerk heeft geactiveerd om een langere levensduur te bereiken", zegt Gorbunova.
Het pluripotentienetwerk en de relatie met positieve levensduurgenen is daarom "een belangrijke bevinding om te begrijpen hoe de levensduur evolueert", zegt Seluanov. "Bovendien kan het de weg vrijmaken voor nieuwe anti-verouderingsinterventies die de belangrijkste positieve levensduurgenen activeren. We zouden verwachten dat succesvolle anti-verouderingsinterventies de expressie van de positieve levensduurgenen zouden verhogen en de expressie van negatieve levensduurgenen zouden verminderen."
 Zika-viruseiwit in kaart gebracht om het zoeken naar genezing te versnellen
Zika-viruseiwit in kaart gebracht om het zoeken naar genezing te versnellen Vliegen injecteren met slakkengif kan ons helpen moleculen te ontdekken voor het ontwikkelen van nieuwe medicijnen
Vliegen injecteren met slakkengif kan ons helpen moleculen te ontdekken voor het ontwikkelen van nieuwe medicijnen Kevers zorgen voor ontwikkeling van kleurveranderende nanodeeltjes voor commercieel gebruik
Kevers zorgen voor ontwikkeling van kleurveranderende nanodeeltjes voor commercieel gebruik Ingenieurs maken microfluïdica modulair met behulp van de populaire in elkaar grijpende blokken
Ingenieurs maken microfluïdica modulair met behulp van de populaire in elkaar grijpende blokken Een speciale elementaire magie
Een speciale elementaire magie
 Westerse rivieren krijgen te maken met knijpen als een ander droog jaar vorm krijgt
Westerse rivieren krijgen te maken met knijpen als een ander droog jaar vorm krijgt 5. 4. 3. 2. 1. 1... Een extra seconde om 2016 te zien
5. 4. 3. 2. 1. 1... Een extra seconde om 2016 te zien Aardbevingen in Raton Basin gekoppeld aan injecties van olie en gasvloeistof
Aardbevingen in Raton Basin gekoppeld aan injecties van olie en gasvloeistof Miljoenen protesteren in door jongeren geleide wereldwijde klimaatstaking
Miljoenen protesteren in door jongeren geleide wereldwijde klimaatstaking Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie
Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie
Hoofdlijnen
- Welke organellen zijn membraansusjes die worden gebruikt om moleculen te transporteren?
- Het bloedstamcelonderzoek dat de geneeskunde van de toekomst zou kunnen veranderen
- Slimme app gebruikt smartphonecamera om plantensoorten te identificeren
- Hoe celorganellen samenwerken
- "The Theory of Biogenesis
- Wat zijn de stappen in de meiose die de variabiliteit verhogen?
- Wat gebeurt er op het chromosomale niveau als een resultaat van bevruchting?
- Kikkers onthullen mechanisme dat de levensvatbaarheid van hybriden bepaalt
- Het verschil tussen kwalitatieve en kwantitatieve eigenschappen in de genetica
- In Australië zijn kaketoes en mensen in een wapenwedloop om toegang tot afval

- Hoe heet is te heet? Hier leest u hoe u kunt zien of uw hond last heeft van de zomerhitte

- Wereldwijd belang van honingbijen voor natuurlijke habitats vastgelegd in nieuw rapport

- Grote plantendiversiteit komt vaak voor in de kleinste gebieden

- Hoe de bescherming van de gezondheid van planten essentieel is voor toekomstige welvaart en duurzaamheid

 Uitbreiding van de VCSEL-golflengtedekking naar het midden-infrarood
Uitbreiding van de VCSEL-golflengtedekking naar het midden-infrarood Onderzoekers gebruiken satellietbeelden om het grondwatergebruik in de centrale vallei van Californië in kaart te brengen
Onderzoekers gebruiken satellietbeelden om het grondwatergebruik in de centrale vallei van Californië in kaart te brengen Hoe een stap voor stap geometrie te doen?
Hoe een stap voor stap geometrie te doen?  Welke elementen vormen de samengestelde kooldioxide?
Welke elementen vormen de samengestelde kooldioxide?  Horzels lokken:wetenschappers ontsluiten seksferomoon van berucht honingbij-roofdier
Horzels lokken:wetenschappers ontsluiten seksferomoon van berucht honingbij-roofdier Wortelexsudaten beïnvloeden de bodemstabiliteit, waterafstotendheid
Wortelexsudaten beïnvloeden de bodemstabiliteit, waterafstotendheid Onderzoek toont aan dat vroege veldervaringen voor docenten in opleiding een pluspunt zijn, zelfs online
Onderzoek toont aan dat vroege veldervaringen voor docenten in opleiding een pluspunt zijn, zelfs online Italië beboet Ryanair voor massale annulering van vluchten
Italië beboet Ryanair voor massale annulering van vluchten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

