
Wetenschap
Nieuwe studie stelt wetenschappers in staat om therapieën te testen voor zeldzame neurodegeneratieve ziekte die jonge kinderen treft
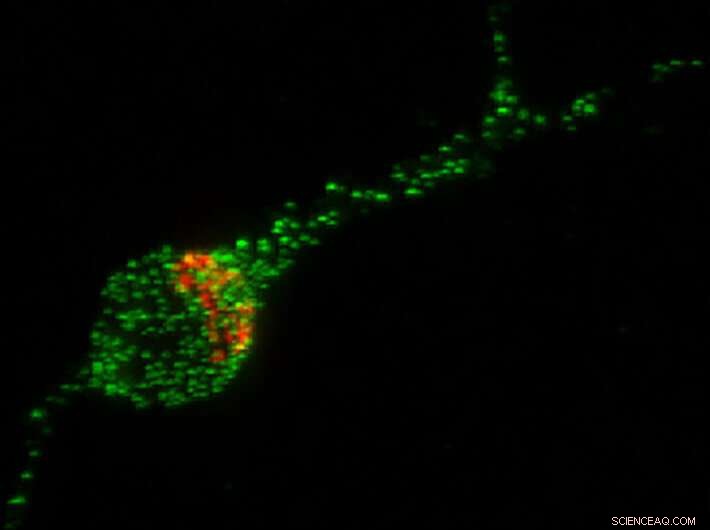
In deze afbeelding van een van een menselijke STEM-cel afgeleide neuron, wordt het Trk-gefuseerde gen-eiwit (TFG) in het groen weergegeven en het Golgi-apparaat, het organel dat helpt bij het verpakken van eiwitten voor transport naar de rest van het lichaam, wordt in het rood weergegeven. Krediet:Universiteit van Wisconsin-Madison
Voor het eerst kunnen wetenschappers therapieën testen voor een groep zeldzame neurodegeneratieve ziekten die zuigelingen en jonge kinderen treffen, dankzij een nieuw onderzoeksmodel dat is gecreëerd door wetenschappers van de Universiteit van Wisconsin-Madison. Hun resultaten zijn gepubliceerd in de Proceedings of the National Academy of Sciences .
Erfelijke spastische paraplegie (HSP's) is een groep neurodegeneratieve ziekten die wordt veroorzaakt door genetische mutaties. Ze zorgen ervoor dat tienduizenden kinderen een verhoogde spierspanning in hun onderste ledematen ontwikkelen, waardoor hun benen zwak worden en uiteindelijk hun vermogen om te kruipen of te lopen wordt aangetast.
"Kinderen vanaf zes maanden die deze mutaties hebben, beginnen tekenen van ziekte te vertonen", zegt Anjon Audhya, een professor in de afdeling Biomoleculaire Chemie van UW-Madison. "Tussen twee en vijf jaar worden deze kinderen rolstoelgebonden en zullen ze helaas nooit kunnen lopen."
Audhya legt uit dat veel wetenschappers geen onderzoek hebben gedaan naar spastische dwarslaesie omdat er geen goed model was om de oorsprong van de ziekte te bestuderen of therapieën te testen. Eerdere muismodellen hebben niet gewerkt omdat de neuronale paden die bewegingsgerelateerde informatie door het hele lichaam vervoeren te veel lijken te verschillen van die bij mensen, en onderzoekers hebben nog geen klinische proeven bij mensen uitgevoerd.
Audhya werkte met een interdisciplinair team van UW-Madison-onderzoekers om een specifieke mutatie te bestuderen die HSP bij jonge kinderen veroorzaakt. Vervolgens gebruikten ze wat ze hadden geleerd om een beter model te maken:bij ratten.
De mutatie die de onderzoekers kozen, werkt op een eiwit dat Trk-fused gen of TFG wordt genoemd. Gezonde TFG-eiwitten werken in zenuwcellen, of neuronen, om andere eiwitten van het ene deel van de cel naar het andere te vervoeren. Het is de taak van een neuron om berichten in de vorm van elektrische signalen tussen de hersenen en de rest van het lichaam te vervoeren.
De eiwitten die voor hun transport afhankelijk zijn van TFG, houden deze neuronale paden gezond en helpen te beheren welke elektrische signalen de hersenen naar het lichaam sturen en welke signalen moeten worden geremd. Door de juiste stimulatieniveaus in evenwicht te brengen, kunnen neuronen bewegingen sturen, zoals het samentrekken van de beenspieren die bij het lopen betrokken zijn.
Bij jonge kinderen met een mutatie op hun TFG-gen bewegen neuronale eiwitten niet efficiënt door hun zenuwcellen. Audhya zegt dat dit een onbalans van elektrische stimulatie kan veroorzaken, waardoor een overvloed aan elektrische signalen naar de onderste ledematen kan worden gestuurd, wat resulteert in een verhoogde spierspanning. Na verloop van tijd leidt de overmatige spierspanning tot een verlies van motorische functie.
"Je kunt je voorstellen dat als je je been heel hard strekt, en je al je energie steekt in het buigen van die spier, het heel moeilijk is om hem te bewegen", zegt Audhya, die ook de senior associate decaan is voor fundamenteel onderzoek, biotechnologie en graduate studies in de UW School of Medicine and Public Health.
Op zoek naar een werkbaar model wendden de onderzoekers zich tot ratten om deze kinderen te helpen. Het team gebruikte CRISPR-technologie voor het bewerken van genen om in rattenembryo's de mutaties te creëren die tot HSP leiden. Hierdoor konden ze het verloop van de ziekte vanaf de vroege ontwikkeling bestuderen en de progressie van de symptomen na de geboorte volgen.
Niet alleen zijn de neuronale paden van ratten dichter bij die van mensen, maar de onderzoekers zagen ook dat de symptomen zich bij ratten op dezelfde manier ontwikkelden als die bij kinderen met HSP. Het gebeurde ook op een tijdschaal die snel genoeg was dat wetenschappers in staat zouden moeten zijn om de levensvatbaarheid van potentiële therapieën gemakkelijk te testen.
"Oefening is de enige therapie die voor deze patiënten bestaat, en dat is echt onbevredigend", zegt Audhya. "Ik denk dat we een grote sprong voorwaarts hebben gemaakt door alleen een model te hebben waarmee je verschillende hypothesen kunt testen. Dat is groot, vanuit mijn perspectief."
De ingewikkelde details die betrokken zijn bij biomoleculaire chemie kunnen voor sommigen alledaags lijken, maar fundamentele wetenschap als deze fascineert Audhya. Pas toen hij in contact kwam met patiënten met HSP, begreep hij volledig de potentiële impact die zijn werk zou kunnen hebben.
"Dit zijn populaties die achtergesteld zijn. Een farmaceutisch bedrijf zal waarschijnlijk geen enorme middelen uitgeven voor een getroffen populatie die zo klein is. In plaats daarvan gaan ze zich concentreren op ziekten zoals Alzheimer en Parkinson", zegt hij. "Dus ik voelde dat hier een ziekte is die algemeen over het hoofd wordt gezien, waarin te weinig geïnvesteerd wordt, en dit is een gebied waar we een impact kunnen hebben."
Audhya zei dat hij hoopt dat dit nieuwe model meer wetenschappers zal inspireren om HSP's te bestuderen om het begrip van de ontwikkeling van de ziekte te verbeteren en om uiteindelijk de toegang tot therapieën te verbeteren die kinderen zullen helpen om ermee te leven. + Verder verkennen
Genmutaties van patiënten met slopende aanvallen en bewegingsstoornissen gecreëerd bij muizen
 Bijdrage van de biologische pomp aan het stikstoftekort in de Stille Oceaan over het hoofd gezien
Bijdrage van de biologische pomp aan het stikstoftekort in de Stille Oceaan over het hoofd gezien Nieuw-Zeeland lanceert plan om de gezondheid van meren en rivieren nieuw leven in te blazen
Nieuw-Zeeland lanceert plan om de gezondheid van meren en rivieren nieuw leven in te blazen Sporen van antidepressiva en pijnstillers gevonden in schaaldieren
Sporen van antidepressiva en pijnstillers gevonden in schaaldieren Rockfalls, gapende spleten maken de Mont Blanc voor velen buiten bereik
Rockfalls, gapende spleten maken de Mont Blanc voor velen buiten bereik Nieuw bewijs dat een buitenaardse botsing 12, 800 jaar geleden veroorzaakte een abrupte klimaatverandering voor de aarde
Nieuw bewijs dat een buitenaardse botsing 12, 800 jaar geleden veroorzaakte een abrupte klimaatverandering voor de aarde
Hoofdlijnen
- Vleugelafdrukken kunnen individuele vleermuizen net zo effectief identificeren als vingerafdrukken mensen identificeren
- Proactieve reacties zijn het meest effectief voor de bestrijding van zeeziekte, blijkt uit onderzoek
- Nieuwe tool kan helpen de kwaliteit te behouden tijdens de kaasproductie
- Studie beantwoordt een al lang bestaand mysterie over slangenpredatie
- Nieuw zenuwdegeneratiemolecuul geïdentificeerd
- Honden zijn overleden na het likken van een gewone chemotherapiecrème, waarschuwt de FDA
- Studie verbindt de BMI van het ontbindende lichaam met omringende bodemmicroben
- Het weer in november is een lastige tijd voor schildpadden
- Antibiotica in actie zien in een pathogene bacterie
- Kleine rode dieren schieten in het donker onder het ijs van een bevroren meer in Quebec
- Prehistorische vrouwen waren sterker dan de elite vrouwelijke atleten van vandaag

- leeuwen, chimpansees, haaien krijgen extra bescherming onder VN-verdrag

- Als gevaarlijke gifstoffen fundamentele biologie onderwijzen
- Insecten hebben moeite om zich aan extreme temperaturen aan te passen, waardoor ze kwetsbaar zijn voor klimaatverandering, zo blijkt uit onderzoek
 Gigantische stervlekken waarschijnlijk oorzaak van dimmen van Betelgeuze
Gigantische stervlekken waarschijnlijk oorzaak van dimmen van Betelgeuze Amerikaans, Russen meren aan bij International Space Station
Amerikaans, Russen meren aan bij International Space Station De ontvoering van de heuvel
De ontvoering van de heuvel  Verbetering van de luchtkwaliteit in de Greater Bay Area van China
Verbetering van de luchtkwaliteit in de Greater Bay Area van China Afrikaanse landen kunnen niet industrialiseren? Ja, ze kunnen
Afrikaanse landen kunnen niet industrialiseren? Ja, ze kunnen Van marginale landbouwgronden winst maken voor boeren en ecosystemen
Van marginale landbouwgronden winst maken voor boeren en ecosystemen Liberaal of conservatief? De politieke voorkeuren van CEO's vertekenen de logica van bedrijven bij het structureren van initiële loonpakketten, studie toont
Liberaal of conservatief? De politieke voorkeuren van CEO's vertekenen de logica van bedrijven bij het structureren van initiële loonpakketten, studie toont Welke rol spelen schimmels in voedselketens?
Welke rol spelen schimmels in voedselketens?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

