
Wetenschap
Roofzuchtige bacteriën - de zoektocht naar een nieuwe klasse antibiotica
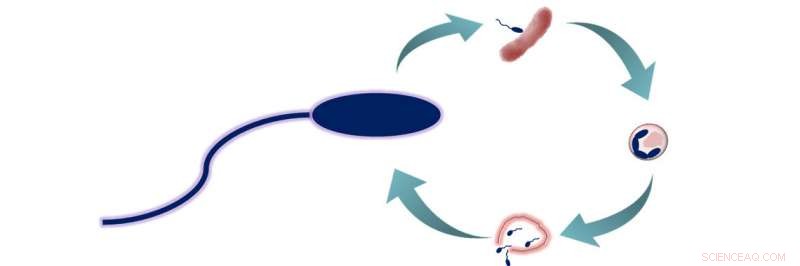
B. bacteriovorus predatiecyclus. B. bacteriovorus kent twee levensfasen:1) zoeken naar prooi, en 2) het betreden van de prooi en het voeren. Tijdens deze tweede fase de bacteriën consumeren hun prooi van binnenuit, waardoor ze kunnen groeien en verlengen voordat ze worden gescheiden in 3 tot 6 nieuwe B. bacteriovorus-cellen. Deze cellen ontsnappen dan aan de nu dode prooi en beginnen aan een nieuwe levenscyclus. Krediet:American Chemical Society
in 2016, de Wereldgezondheidsorganisatie noemde antibioticaresistentie als "een van de grootste bedreigingen voor de wereldwijde gezondheid, voedselveiligheid, en ontwikkeling vandaag." De aankondiging noemde een groeiende lijst van infecties, zoals tuberculose en gonorroe, die elk jaar moeilijker te behandelen zijn naarmate de resistentie tegen de huidige antibioticabehandelingen toeneemt. Toch zijn antibiotica essentieel - zonder hen, het menselijk ras zou worden geplaagd door aanhoudende infecties. Dus wat is de oplossing om continue behandeling te garanderen en tegelijkertijd de alarmerende toename van resistentie aan te pakken?
Een mogelijke oplossing ligt in een uniek type roofbacteriën die zich voedt met andere bacteriën, zoals die welke ziekten veroorzaken. Nagesynchroniseerd met "levende antibiotica, " deze groep vleesetende fauna heeft de aandacht van onderzoekers getrokken, waaronder die van de Okinawa Institute of Science and Technology Graduate University (OIST). In een onlangs gepubliceerd artikel in ACS synthetische biologie , OIST-onderzoekers hebben de eerste stappen gezet in de richting van genetische manipulatie van zo'n kleine kannibaal, B. bacteriovorus. Ze hebben hulpmiddelen geïdentificeerd die de manipulatie van genen mogelijk maken die het roofzuchtige gedrag van deze bacterie beïnvloeden.
"In de toekomst, we willen de predatie van de bacteriën beheersen - de timing en mate van predatie, " legt Dr. Mohammed Dwidar uit van de Nucleic Acid Chemistry and Engineering Unit en eerste auteur van het artikel. "[Momenteel] ontbreekt het ons aan de elementaire technische hulpmiddelen om dit te doen."
B. bacteriovorus is onschadelijk voor mensen maar dodelijk voor zijn prooi - Gram-negatieve bacteriën - waaronder slechteriken zoals E. coli, Salmonella, Legionella, en anderen. Als zodanig, in staat zijn om het onder controle te krijgen, zou mogelijk veel verschillende soorten infecties kunnen behandelen. Echter, vanwege zijn ongewone roofzuchtige karakter en andere unieke kenmerken, genetische manipulatie van B. bacteriovorus is beperkt.
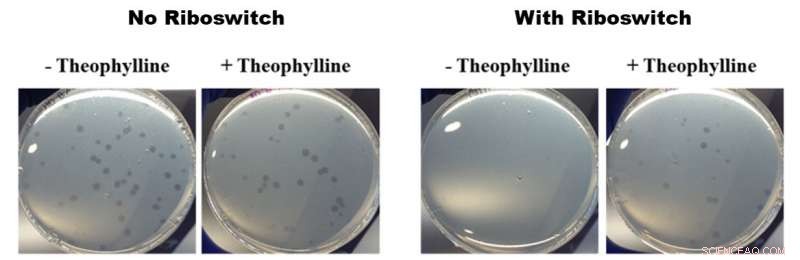
Effecten van door theofylline geactiveerde riboswitches op de groei van B. bacteriovorus. Alle foto's in de afbeelding hierboven tonen petrischalen met B. bacteriovorus en zijn prooi E. coli. De twee foto's aan de linkerkant tonen de groei van B. bacteriovorus in schalen die geen (-) en (+) theofylline bevatten zonder een riboswitch in het genoom. De rechter twee foto's tonen de groei van B. bacteriovorus gemodificeerd met een riboswitch in schalen die geen (-) en (+) theofylline bevatten. De linker foto's laten geen verschil in groei zien en de rechter foto's tonen snellere groei in aanwezigheid van theofylline, wat betekent dat de door theofylline geactiveerde riboswitches een effect hadden op het roofdiergedrag van B. bacteriovorus. Krediet:American Chemical Society
De OIST-onderzoekers gebruikten riboswitches, die genexpressie-controlerende instrumenten zijn waarvan bekend is dat ze goed functioneren in andere bacteriën, om de uitdaging aan te gaan om de predatie van B. bacteriovorus te begrijpen en te manipuleren. De manier waarop een gen tot expressie wordt gebracht, volgt een specifieke route:DNA wordt via transcriptie omgezet in RNA, RNA wordt via translatie omgezet in eiwitten, en dan voeren de eiwitten verschillende functies uit. De riboswitch komt binnen in de translatiefase. Door een riboswitch aan het begin van een RNA-streng te plaatsen, en dan "activeren" met een chemische stof, de riboswitch kan het RNA starten of stoppen om te worden vertaald in een eiwit.
Voor hun studie de OIST-onderzoekers plaatsten een riboswitch in een van de genen die belangrijk werden geacht voor het roofzuchtige gedrag van B. bacteriovorus:flagellaire sigmafactor fliA. Vervolgens activeerden ze het met de chemische theofylline. Na het plaatsen van de gemodificeerde bacteriën in petrischalen samen met een heerlijke E. coli prooi, de gemodificeerde B. bacteriovorus leek zich sneller te vermenigvuldigen in aanwezigheid van theofylline dan in afwezigheid ervan. Deze snellere vermenigvuldiging impliceert dat B. bacteriovorus zijn prooi sneller at, en dus sneller vermenigvuldigen. Dit toont op zijn beurt aan dat de roofzuchtige levenscyclus kan worden gecontroleerd door theofylline.
Naast het einddoel "levend antibioticum", er zijn veel meer potentiële toepassingen voor gemakkelijk manipuleerbare B. bacteriovorus-cellen. "Mensen willen biologisch voedsel zonder chemicaliën, Dr. Dwidar legt uit. "De roofbacteriën kunnen voor sommige plantenziekten een potentieel veilig alternatief zijn voor antibacteriële middelen. We kunnen het ook gebruiken voor de industrie, bijvoorbeeld, in waterzuiveringsinstallaties."
"In de toekomst, je zou deze bacteriën op vers voedsel kunnen spuiten ter bescherming tegen voedselvergiftiging, "Professor Yohei Yokobayashi, die ook bij het onderzoek betrokken was, voegt toe.
Met de resultaten van de OIST-onderzoekers in de hand, de volgende stap is om meer te weten te komen over B. bacteriovorus en de hulpmiddelen die zijn gedrag kunnen beheersen om op een dag zijn volledige antibioticumpotentieel te realiseren.
 Onderzoekers vinden een manier om farmacoterrorisme te bestrijden
Onderzoekers vinden een manier om farmacoterrorisme te bestrijden Het wijzigen van de genen van zijderupsen om de toevoeging van nuttige eiwitten aan de zijdeproductie te veroorzaken
Het wijzigen van de genen van zijderupsen om de toevoeging van nuttige eiwitten aan de zijdeproductie te veroorzaken Nieuwe aanpak bepaalt optimale materiaalontwerpen met minimale gegevens
Nieuwe aanpak bepaalt optimale materiaalontwerpen met minimale gegevens Neutronen inspecteren zouthoudende materialen om de opslag van afval op de lange termijn te verbeteren
Neutronen inspecteren zouthoudende materialen om de opslag van afval op de lange termijn te verbeteren Hoe te berekenen Mollen van Liters
Hoe te berekenen Mollen van Liters
Hoofdlijnen
- Reuzenzeebaars heeft meer waarde als levend, onderzeese wonderen ademen dan als commerciële vangst
- Waar bevinden zich lipiden in het lichaam?
- Maïsplaag maakt gebruik van plantafweerstoffen om zichzelf te beschermen
- Waar zijn stamcellen gevonden?
- Zilte zwembadbacteriën kunnen opruimen en opstarten
- Twee muziekbloemlezingen nu voor eeuwig opgeslagen in DNA
- Antibiotica kunnen het vermogen van immuuncellen om bacteriën te doden verminderen
- Hoe snel is een knipoog?
- Biologen ontdekten de paden van groepen van de lophopoor
- Mieren in het bladerdak van het Amazone-regenwoud hebben veel meer bacteriën in hun ingewanden dan grondbewoners

- Herziening van historische voorraadroutes kan zeldzame stukken inheemse planten en dieren in gevaar brengen

- Goed excuus,

- Onderzoekers onthullen een faalveilige structuur van een enzym dat verband houdt met de ziekte van Alzheimer, kanker
- Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin

 Nieuwe opvouwbare drone vliegt door nauwe gaten in reddingsmissies
Nieuwe opvouwbare drone vliegt door nauwe gaten in reddingsmissies De Verenigde Staten lopen het risico van een gewapende opstand tegen de politie, onderzoeker zegt:
De Verenigde Staten lopen het risico van een gewapende opstand tegen de politie, onderzoeker zegt: Overbevolking en betaalbaarheidsstress:de COVID-19-hotspots van Melbourne zijn ook hotspots voor crises
Overbevolking en betaalbaarheidsstress:de COVID-19-hotspots van Melbourne zijn ook hotspots voor crises Amazon heeft de Amerikaanse detailhandel vernietigd, Mnuchin zegt
Amazon heeft de Amerikaanse detailhandel vernietigd, Mnuchin zegt Trump belooft Chinese telecombanen veilig te stellen (update)
Trump belooft Chinese telecombanen veilig te stellen (update) Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie
Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie Zal Nissans nieuwe zelfrijdende stoel een gouden eeuw van luiheid inluiden?
Zal Nissans nieuwe zelfrijdende stoel een gouden eeuw van luiheid inluiden?  Heeft een veelvoorkomende kinderziekte de Neanderthalers ten val gebracht?
Heeft een veelvoorkomende kinderziekte de Neanderthalers ten val gebracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

