
Wetenschap
Nieuwe technologie zorgt ervoor dat moleculen veilig cellen kunnen binnendringen
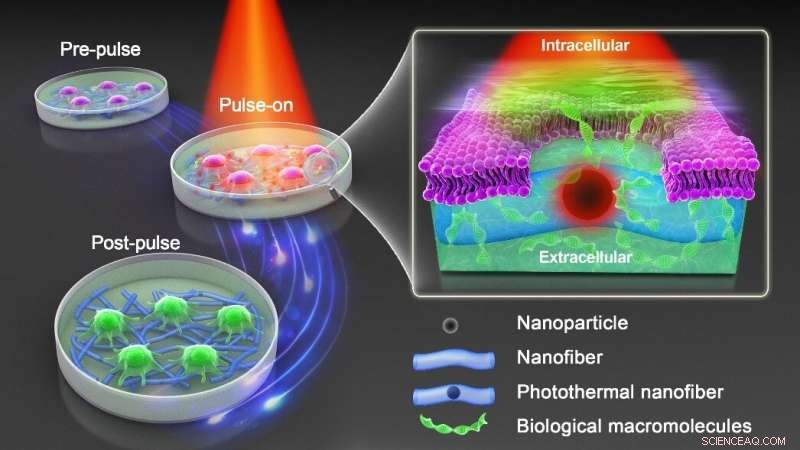
Grafisch abstract. Krediet:DOI:10.1038/s41565-021-00976-3
Professor Kevin Braeckmans van de Universiteit Gent richtte zich de laatste 10 jaar op een methode voor veilige engineering van therapeutische cellen met fotothermische nanovezels. Tegenwoordig is Natuurnanotechnologie geeft inzicht in hoe deze biocompatibele fotothermische nanovezels werden ontwikkeld, en hoe, na laserbestraling, cellen die in contact komen met die nanovezels permeabel worden en getransfecteerd kunnen worden met een verscheidenheid aan effectormoleculen, waaronder CRISPR/Cas9 ribonucleoproteïnecomplexen en siRNA. Professor Braeckmans en zijn team toonden aan dat cellen, zoals embryonale stamcellen en menselijke T-cellen, getransfecteerd met dergelijke nanovezels, in uitstekende gezondheid verkeren en hun therapeutische functionaliteit behouden.
Nieuwe basis voor celgebaseerde therapieën
Celgebaseerde therapieën vormen een nieuwere vorm van behandeling waarbij genetisch gemodificeerde cellen in de patiënt worden geïnjecteerd om ziekten te voorkomen of te behandelen. Een bekend voorbeeld is het gebruik van de eigen immuuncellen van een kankerpatiënt die geïsoleerd, genetisch gemodificeerd en uitgebreid kunnen worden in een laboratoriumomgeving en opnieuw in de patiënt kunnen worden geïnfuseerd om de tumorcellen aan te vallen. Genetische modificatie van cellen is afhankelijk van intracellulaire toedieningstechnologieën die vaak moeite hebben met het verkrijgen van voldoende efficiëntie terwijl ze een minimale impact hebben op de gezondheid en het functioneren van de cel.
Met nanodeeltjes gesensibiliseerde fotoporatie is in dit opzicht bijzonder veelbelovend, omdat het doorgaans een hoge efficiëntie, hoge doorvoer en lage toxiciteit biedt. Het is gebaseerd op het gebruik van op licht reagerende nanodeeltjes, zoals gouden nanodeeltjes (NP's), die explosieve nanobellen kunnen vormen bij gepulseerde laserbestraling. Die kleine explosies kunnen kleine poriën in celmembranen veroorzaken, waardoor externe effectormoleculen die in het celmedium zijn aangevuld, de cellen kunnen binnendringen. De vertaling van door nanodeeltjes gesensibiliseerde fotoporatie naar klinische toepassingen wordt echter belemmerd door het feit dat cellen in contact zijn geweest met (niet-afbreekbare) nanodeeltjes, wat toxicologische en regelgevende problemen met zich meebrengt.
Daarom is een nieuwe benadering nodig die het voordeel van door nanodeeltjes gesensibiliseerde fotoporatie behoudt, terwijl direct contact van nanodeeltjes en cellen wordt vermeden. Zoals te zien is in de bovenstaande figuur, hebben professor Braeckmans en zijn team fotothermische ijzeroxide-nanodeeltjes (IONP's) ingebed in biocompatibele polymere nanovezels die werden geproduceerd door elektrospinning. Polycaprolacton (PCL) is een biocompatibel polymeer dat veel wordt gebruikt in biomedische toepassingen, terwijl IONP's kostenefficiënt zijn en een breed lichtabsorptiespectrum hebben.
Ze laten zien dat zowel hechtende als suspensiecellen veilig en efficiënt kunnen worden getransfecteerd met een reeks macromoleculen na bestraling met laserpulsen van nanoseconden. Door elementanalyse uit te voeren via inductief gekoppelde plasma-tandem massaspectrometrie (ICP-MS/MS), bevestigen ze dat IONP's veilig ingebed blijven in de nanovezels na laserbestraling, zodat de behandelde cellen effectief vrij zijn van directe blootstelling aan nanodeeltjes. Numerieke simulaties van warmteoverdracht van met vezels ingebedde IONP's naar nabijgelegen cellen werden uitgevoerd om beter te begrijpen hoe de fluentie van de laserpuls, de IONP-distributie en de aggregatietoestand de doorlaatbaarheid van het celmembraan beïnvloeden.
Experimenteel toonde het team aan dat fotoporatie met fotothermische nanovezels met succes functionele biologische moleculen, waaronder siRNA of CRISP-Cas9 ribonucleoproteïnen (RNP's), kan leveren aan zowel hechtende als suspensiecellen, waaronder menselijke embryonale stamcellen (hESC) en primaire menselijke T-cellen. Als benchmark werd een vergelijking gemaakt met state-of-the-art elektroporatie. Terwijl geëlektroporeerde cellen leden onder veranderingen in hun fenotype en functionaliteit, was dit niet het geval voor gefotoporeerde cellen die hun vermogen om te prolifereren en, in het geval van CAR-T-cellen, tumorcellen te doden, behielden. Ten slotte werd PEN-fotoporatie gebruikt om CAR-T-cellen te transfecteren met siRNA gericht op de PD1-receptor, een bekende immuuncontrolepuntremmer. Met siPD1 behandelde cellen werd bevestigd dat ze in vivo een verbeterd tumordodend vermogen hebben.
Samen laat het zien dat fotoporatie met fotothermische nanovezels een efficiënte en veilige intracellulaire levering van een breed scala aan effectormoleculen in een verscheidenheid aan celtypen mogelijk maakt zonder contact met potentieel giftige fotothermische nanodeeltjes. "Wij geloven dat dit een belangrijke stap is in de richting van het gebruik van fotoporatie voor een veilige en efficiënte productie van gengemodificeerde celtherapieën", zegt professor Braeckmans. + Verder verkennen
Titaniumoxide nanobuisjes vergemakkelijken goedkope laserondersteunde fotoporatie
 Ingenieurs ontdekken waarom gevallen bladeren op treinrails zo glad zijn
Ingenieurs ontdekken waarom gevallen bladeren op treinrails zo glad zijn Nieuwe katalysatoren verbeteren de efficiëntie van de ureumsynthese bij omgevingsomstandigheden
Nieuwe katalysatoren verbeteren de efficiëntie van de ureumsynthese bij omgevingsomstandigheden Zwavelzuur- en chloorbleekreactie
Zwavelzuur- en chloorbleekreactie  Magnetische behandeling kan helpen bij het verwijderen van de smaak van wijnen
Magnetische behandeling kan helpen bij het verwijderen van de smaak van wijnen Hete OLED's kunnen terugschakelen
Hete OLED's kunnen terugschakelen
Hoofdlijnen
- Maleisië omarmt het werk van Melanies aan de illegale handel in wilde dieren
- Een natte winter kan de invasieve soorten van San Francisco Bay opschudden
- Zouden herten aanwijzingen kunnen bevatten over het verband tussen malariaresistentie en sikkelcel?
- Waarom zijn sommige mensen muggenmagneten en anderen niet? Entomoloog wijst op stofwisseling, lichaamsgeur en mindset
- Bezuinigingen op het behoud brengen de Amazone-dieren in Brazilië in gevaar
- De opname van koolstof in bossen wordt aangetast door klimaatverandering, suggereert onderzoek naar bladtemperatuur
- Mammoetprojecten om Noorse viskwekerijen milieuvriendelijk te maken
- Moderne genomica gebruiken om krokodillenschubben in vogelachtige veren te veranderen
- Voordelen en nadelen van Hydrostatic Skeleton
- Nare nano-injectoren vormen een nieuw doelwit voor antibioticaonderzoek
- Onderzoekers brengen getheoretiseerd geleidingsmechanisme tot leven

- Platte lens om over een continue bandbreedte te werken, maakt nieuwe controle over licht mogelijk

- Op weg naar het doorbreken van de terahertz-barrière voor grafeen-nano-elektronica

- Door Kirigami geïnspireerde techniek manipuleert licht op nanoschaal

 Kledingontwikkelingssoftware:computermodel berekent warmteafvoer onder kleding
Kledingontwikkelingssoftware:computermodel berekent warmteafvoer onder kleding Conserveringskosten kunnen hoger zijn dan verwacht
Conserveringskosten kunnen hoger zijn dan verwacht Studie:Vaderschapsverlof voor kansarme vader resulteert in sterke familierelaties
Studie:Vaderschapsverlof voor kansarme vader resulteert in sterke familierelaties HRM is een voorspeller voor de veerkracht van bedrijven na ontslagen
HRM is een voorspeller voor de veerkracht van bedrijven na ontslagen Vrouwen keren wereldwijd het tij in het klimaatbeleid en kunnen een nieuw tijdperk inluiden voor Australië
Vrouwen keren wereldwijd het tij in het klimaatbeleid en kunnen een nieuw tijdperk inluiden voor Australië Twitter-berichten onthullen polarisatie in het Congres over COVID-19
Twitter-berichten onthullen polarisatie in het Congres over COVID-19 Afbeelding:Saturnus grote storm van 2011
Afbeelding:Saturnus grote storm van 2011 Studie onthult nieuwe aanwijzingen over dodelijkste lawine van Mount Everest
Studie onthult nieuwe aanwijzingen over dodelijkste lawine van Mount Everest
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

