
Wetenschap
Hartaanval op een chip:wetenschappers modelleren omstandigheden van ischemie op een microfluïdisch apparaat

Het microfluïdische apparaat dat HL-1-hartcellen bevat, is in staat om omstandigheden te modelleren die worden waargenomen tijdens een hartaanval, inclusief een verlaging van het zuurstofgehalte. Krediet:Tufts University
Onderzoekers onder leiding van biomedische ingenieurs van Tufts University hebben een microfluïdische chip uitgevonden die hartcellen bevat die in staat is hypoxische aandoeningen na een hartaanval na te bootsen, met name wanneer een slagader in het hart wordt geblokkeerd en vervolgens na de behandeling wordt gedeblokkeerd. De chip bevat gemultiplexte arrays van elektronische sensoren die buiten en in de cellen zijn geplaatst en die de stijging en daling van de spanning over individuele celmembranen kunnen detecteren, evenals spanningsgolven die over de cellaag bewegen, die ervoor zorgen dat de cellen samen in de chip kloppen, net zoals ze dat in het hart doen. Na het verlagen van het zuurstofgehalte in de vloeistof in het apparaat, de sensoren detecteren een eerste periode van tachycardie (versnelde hartslag), gevolgd door een verlaging van de hartslag en uiteindelijk aritmie die lijkt op een hartstilstand.
Het onderzoek, gepubliceerd in Nano-letters , is een belangrijke vooruitgang in de richting van het begrijpen van de elektrofysiologische reacties op cellulair niveau op ischemische hartaanvallen, en kan worden toegepast op toekomstige ontwikkeling van geneesmiddelen. Het papier werd door de American Chemical Society geselecteerd als Editors' Choice, en is beschikbaar met open toegang.
Hart- en vaatziekten (HVZ) blijven wereldwijd de belangrijkste doodsoorzaak, bij de meeste patiënten die lijden aan cardiale ischemie, die optreedt wanneer een slagader die het hart van bloed voorziet, gedeeltelijk of volledig wordt geblokkeerd. Als ischemie gedurende een langere periode optreedt, het hartweefsel heeft geen zuurstof meer (een aandoening die "hypoxie" wordt genoemd), en kan leiden tot weefselsterfte, of myocardinfarct. De veranderingen in hartcellen en weefsels veroorzaakt door hypoxie omvatten veranderingen in spanningspotentiaal over het celmembraan, vrijkomen van neurotransmitters, verschuivingen in genexpressie, veranderde metabolische functies, en activering of deactivering van ionkanalen.
De biosensortechnologie die in de microfluïdische chip wordt gebruikt, combineert multi-elektrode-arrays die extracellulaire uitlezingen van spanningspatronen kunnen bieden, met nanopillar-sondes die het membraan binnendringen om uitlezingen van spanningsniveaus (actiepotentialen) in elke cel te nemen. Met minuscule kanaaltjes in de chip kunnen de onderzoekers de vloeistof die over de cellen stroomt continu en nauwkeurig aanpassen, het verlagen van de zuurstofniveaus tot ongeveer 1-4 procent om hypoxie na te bootsen of het verhogen van zuurstof tot 21 procent om normale omstandigheden te modelleren. De veranderende omstandigheden zijn bedoeld om te modelleren wat er met cellen in het hart gebeurt wanneer een slagader wordt geblokkeerd, en vervolgens heropend door behandeling.
"Heart-on-a-chip-modellen zijn een krachtig hulpmiddel om ziekten te modelleren, maar de huidige instrumenten om elektrofysiologie in die systemen te bestuderen, ontbreken enigszins, omdat ze ofwel moeilijk te multiplexen zijn of uiteindelijk schade aan de cellen veroorzaken, " zei Brian Timko, assistent-professor biomedische technologie aan de Tufts University School of Engineering, en corresponderend auteur van de studie. "Signaleringsroutes tussen moleculen en uiteindelijk elektrofysiologie treden snel op tijdens hypoxie, en ons apparaat kan veel van deze informatie tegelijkertijd in realtime vastleggen voor een groot aantal cellen."
Wanneer getest, de extracellulaire elektrode-arrays zorgden voor een tweedimensionale kaart van spanningsgolven die over de laag hartcellen gingen, en onthulde een voorspelbaar golfpatroon onder normale (21 procent) zuurstofniveaus. In tegenstelling tot, de onderzoekers observeerden grillige en langzamere golfpatronen wanneer de zuurstof werd teruggebracht tot 1 procent.
De intracellulaire nanosondesensoren gaven een opmerkelijk nauwkeurig beeld van actiepotentialen in elke cel. Deze sensoren waren gerangschikt als een reeks kleine naalden met platina-tip waarop de cellen rusten, als een spijkerbed. Wanneer gestimuleerd met een elektrisch veld, de naalden prikken door het celmembraan, waar ze kunnen beginnen met het nemen van metingen met een resolutie van één cel. Beide soorten apparaten zijn gemaakt met behulp van fotolithografie - de technologie die wordt gebruikt om geïntegreerde schakelingen te maken - waarmee onderzoekers apparaatarrays met zeer reproduceerbare eigenschappen konden bereiken.
De extracellulaire en intracellulaire sensoren geven samen informatie over de elektrofysiologische effecten van een gemodelleerde ischemische aanval, inclusief een "time-lapse" van cellen wanneer ze disfunctioneel worden en vervolgens reageren op de behandeling. Als zodanig, de microfluïdische chip zou de basis kunnen vormen van een high-throughput-platform bij het ontdekken van geneesmiddelen, het identificeren van therapieën die cellen en weefsels helpen de normale functie sneller te herstellen.
"In de toekomst, we kunnen verder kijken dan de effecten van hypoxie en andere factoren overwegen die bijdragen aan acute hartaandoeningen, zoals acidose, nutriëntentekort en afvalophoping, eenvoudig door de samenstelling en stroom van het medium te wijzigen, "zei Timko. "We zouden ook verschillende soorten sensoren kunnen opnemen om specifieke moleculen te detecteren die tot expressie worden gebracht als reactie op spanningen."
 Het vermogen van SIRT6 om de groei van kankercellen te onderdrukken wordt uitgelegd
Het vermogen van SIRT6 om de groei van kankercellen te onderdrukken wordt uitgelegd Hoe een atoom protonen verliest
Hoe een atoom protonen verliest  Wat zit er in deze plant? Het beste geautomatiseerde systeem voor het vinden van potentiële medicijnen
Wat zit er in deze plant? Het beste geautomatiseerde systeem voor het vinden van potentiële medicijnen Eenvoudig te maken onderzoeksprojecten
Eenvoudig te maken onderzoeksprojecten  Nieuw NIST-onderzoek kan de kosten van het maken van stuivers verlagen
Nieuw NIST-onderzoek kan de kosten van het maken van stuivers verlagen
 Koningsgetijden zijn een blik in de toekomst met stijgende zeeën. Voor velen, overstromingen is het nieuwe normaal
Koningsgetijden zijn een blik in de toekomst met stijgende zeeën. Voor velen, overstromingen is het nieuwe normaal Onderzoek moet dodelijke milieurampen met mijnafval voorkomen
Onderzoek moet dodelijke milieurampen met mijnafval voorkomen Welke visie hebben we op de diepzee?
Welke visie hebben we op de diepzee? Oudste meteorietverzameling op aarde gevonden op een van de droogste plekken
Oudste meteorietverzameling op aarde gevonden op een van de droogste plekken Nieuw onderzoek bevestigt dat megabranden niet toenemen:groot, zeer ernstige branden zijn natuurlijk in bossen in het westen van de VS
Nieuw onderzoek bevestigt dat megabranden niet toenemen:groot, zeer ernstige branden zijn natuurlijk in bossen in het westen van de VS
Hoofdlijnen
- Warmer watersignalen veranderen voor Schotse shags
- Wedstrijden om vrouwelijke aandacht maken van mannen betere presteerders - in fruitvliegjes
- Celcyclus Feiten
- Onderzoekers willen weten waarom beluga-walvissen nog niet zijn hersteld
- Onderzoekers ontdekken een nieuwe manier om door virussen veroorzaakte kankers te onderdrukken
- Geslachtsrollen in de oudheid
- Grazende paarden op betere weiden
- Wat zijn enkele kenmerken van DNA?
- Wat zijn twee voorbeelden van reacties Organismen weergeven om de homeostase te onderhouden?
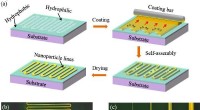
- Elektronische schakelingen geprint met een resolutie van één micron
- Caltech-onderzoekers ontwerpen een nieuw nanomesh-materiaal

- Grote impact, klein element - waterstofenergie op nanoschaal

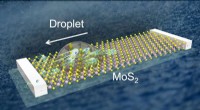
- Beweging van een vloeistofdruppel genereert meer dan 5 volt elektriciteit
- Nieuwe nanostructuren voor efficiënt energietransport over lange afstand

 Kunnen organismen op Mars overleven, en kunnen we ze identificeren?
Kunnen organismen op Mars overleven, en kunnen we ze identificeren? Zoete wetenschap:glucosestroop aan het werk zetten op de oorsprong van de aarde
Zoete wetenschap:glucosestroop aan het werk zetten op de oorsprong van de aarde Studie:automobilisten met een laag inkomen worden gestraft door belastingregels
Studie:automobilisten met een laag inkomen worden gestraft door belastingregels Belangrijke dingen om te weten over NASA's Ingenuity Mars Helicopter
Belangrijke dingen om te weten over NASA's Ingenuity Mars Helicopter Gebruik van geregenereerde asfaltproducten
Gebruik van geregenereerde asfaltproducten Wetenschappers gebruiken satellieten om essentiële ondergrondse watervoorraden te meten
Wetenschappers gebruiken satellieten om essentiële ondergrondse watervoorraden te meten Gemengde breuken vermenigvuldigen en delen
Gemengde breuken vermenigvuldigen en delen  Ingenieurs openen deur naar grote nieuwe bibliotheek met kleine nanodeeltjes
Ingenieurs openen deur naar grote nieuwe bibliotheek met kleine nanodeeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

