
Wetenschap
Onderzoekers verbeteren computermodellering voor het ontwerpen van nanodragers voor medicijnafgifte

Het nieuwe model van de onderzoekers houdt rekening met hoe cytoskeletale pinning de golvingen van het celmembraan beïnvloedt. Krediet:Universiteit van Pennsylvania
Een team van onderzoekers van de Universiteit van Pennsylvania heeft een computermodel ontwikkeld dat zal helpen bij het ontwerp van nanodragers, microscopische structuren die worden gebruikt om medicijnen naar hun doelen in het lichaam te leiden. Het model houdt beter rekening met hoe de oppervlakken van verschillende soorten cellen golven als gevolg van thermische fluctuaties, informerende kenmerken van de nanodragers die hen helpen lang genoeg aan cellen te blijven plakken om hun nuttige lading af te leveren.
De studie werd geleid door Ravi Radhakrishnan, een professor in de afdelingen bio-engineering en chemische en biomoleculaire engineering in Penn's School of Engineering and Applied Science, en Ramakrishnan Natesan, een lid van zijn laboratorium.
Ook bijgedragen aan de studie waren Richard Tourdot, een lid van het Radhakrishnan-lab; David Eckmann, de Horatio C. Wood hoogleraar anesthesiologie en kritieke zorg aan de Perelman School of Medicine van Penn; Portonovo Ayyaswamy, de Asa Whitney hoogleraar Werktuigbouwkunde en Toegepaste Mechanica in Penn Engineering; en Vladimir Muzykantov, een professor in de farmacologie in Penn Medicine.
Het werd gepubliceerd in het tijdschrift Royal Society Open Science .
Nanodragers kunnen worden ontworpen met moleculen aan de buitenkant die alleen binden aan biomarkers die op een bepaald type cel worden aangetroffen. Dit type targeting kan bijwerkingen verminderen, zoals wanneer chemotherapiemedicijnen gezonde cellen vernietigen in plaats van kankercellen, maar de biomechanica van dit bindingsproces is complex.
Eerder werk van enkele van de onderzoekers onthulde een contra-intuïtieve relatie die suggereerde dat het toevoegen van meer doelgerichte moleculen op het oppervlak van de nanodrager niet altijd beter is.
Een nanodrager met meer van die targeting-moleculen kan veel van de overeenkomstige biomarkers tegelijk vinden en eraan binden. Hoewel een dergelijke configuratie stabiel is, het kan het vermogen van de nanodrager om onderscheid te maken tussen gezonde en zieke weefsels verminderen. Het hebben van minder targeting moleculen maakt de nanocarrier selectiever, omdat het moeilijker zal binden aan gezond weefsel waar de overeenkomstige biomarkers niet tot overexpressie worden gebracht.
De nieuwe studie van het team voegt nieuwe dimensies toe aan het model van het samenspel tussen het cellulaire oppervlak en de nanodrager.
"Het celoppervlak zelf is als een caravantent op een winderige dag in een woestijn, " zei Radhakrishnan. "Hoe meer overtollige stof, hoe meer het gefladder van de tent. evenzo, hoe meer overtollig celmembraanoppervlak op de 'tentpalen, ' het cytoskelet van de cel, hoe meer het membraan fladdert als gevolg van thermische beweging."
Het Penn-team ontdekte dat verschillende celtypen verschillende hoeveelheden van dit overtollige membraanoppervlak hebben en dat deze mechanische parameter bepaalt hoe goed nanodragers aan de cel kunnen binden. Rekening houdend met het fladderen van het membraan in hun computermodellen, naast de hoeveelheid targeting moleculen op de nanocarrier en biomarkers op het celoppervlak, heeft het belang benadrukt van deze mechanische aspecten in hoe efficiënt nanodragers hun nuttige lading kunnen afleveren.
"Deze ontwerpcriteria, "Radhakrishnan zei, "kan worden gebruikt bij het op maat ontwerpen van nanodragers voor een bepaalde patiënt of patiëntcohort, vandaar een belangrijke weg vooruit voor het ontwerp van nanocarriers op maat in het tijdperk van gepersonaliseerde geneeskunde."
 Heeft de opwarming van het Noordpoolgebied invloed op het extreme weer in het VK?
Heeft de opwarming van het Noordpoolgebied invloed op het extreme weer in het VK? Langzame aardbevingen in Cascadia zijn voorspelbaar
Langzame aardbevingen in Cascadia zijn voorspelbaar Historische erfenissen beïnvloeden de overleving van klimaatverandering in het Caribisch gebied
Historische erfenissen beïnvloeden de overleving van klimaatverandering in het Caribisch gebied Zebra Life Cycle
Zebra Life Cycle Een verborgen diversiteit van microscopisch kleine dierfossielen van een half miljard jaar oud
Een verborgen diversiteit van microscopisch kleine dierfossielen van een half miljard jaar oud
Hoofdlijnen
- "What Does Heterozygous Mean?
- Tijgers klampen zich vast aan overleving in steeds meer gefragmenteerde bossen op Sumatras
- Waarom blozen mensen?
- Koolwaterstofafbrekende schimmel geeft zijn geheimen prijs
- De genetische handtekening van de zeeschelp lezen
- Hoe verschillende mierensoorten in hetzelfde territorium naast elkaar bestaan
- Codominantie: definitie, toelichting en voorbeeld
- Is alle pijn mentaal?
- Minder herkauwen, meer vergroening van de brandstof
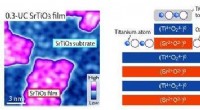
- Identificatie van een complex groeiproces van dunne films van strontiumtitanaat
- Een telefoon die binnen enkele seconden oplaadt? Wetenschappers brengen het dichter bij de realiteit

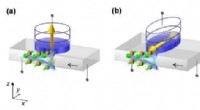
- Een magnetisch geheugenapparaat met nieuwe structuur ontwikkeld
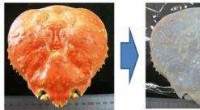
- Japanse onderzoekers maken een krabschaal transparant
- Nanoantennes helpen detectoren meer warmte te zien, minder lawaai

 Er zijn ook microplastics in de buurt van de top van de Mount Everest
Er zijn ook microplastics in de buurt van de top van de Mount Everest Verkeerde uitspraak:waarom je moet stoppen met het corrigeren van fouten van mensen
Verkeerde uitspraak:waarom je moet stoppen met het corrigeren van fouten van mensen Een lijst met dieren in een estuarium
Een lijst met dieren in een estuarium Groeiende HCA-kristallen
Groeiende HCA-kristallen Zelfgemaakt Bobcat-aas
Zelfgemaakt Bobcat-aas  Een mechanische trigger voor toxische tumortherapie
Een mechanische trigger voor toxische tumortherapie Door zelfassemblage geïnduceerde luminescentie van Eu3+-complexen voor bioimaging-toepassing
Door zelfassemblage geïnduceerde luminescentie van Eu3+-complexen voor bioimaging-toepassing Het complexe verband tussen bevolkingsafname en een opwarmende planeet
Het complexe verband tussen bevolkingsafname en een opwarmende planeet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

