Wetenschap
Behandeling met gouden nanodeeltjes van Trojaans paard kan hersentumoren verslaan
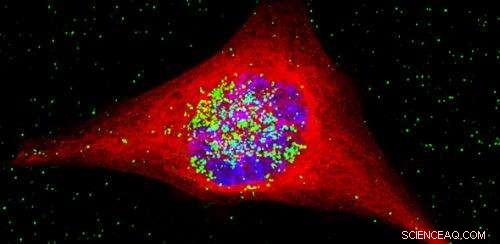
Een kankercel die de nanodeeltjes bevat. De nanodeeltjes zijn groen gekleurd, en zijn de kern binnengegaan, dat is het gebied in blauw. Krediet:M. Welland
Een "Trojaans paard"-behandeling voor een agressieve vorm van hersenkanker, waarbij kleine nanodeeltjes van goud worden gebruikt om tumorcellen te doden, is met succes getest door wetenschappers.
De baanbrekende techniek zou uiteindelijk kunnen worden gebruikt voor de behandeling van glioblastoma multiforme, wat de meest voorkomende en agressieve hersentumor is bij volwassenen, en notoir moeilijk te behandelen. Veel patiënten overlijden binnen enkele maanden na de diagnose, en slechts zes op de 100 patiënten met de aandoening zijn na vijf jaar in leven.
Het onderzoek omvatte technische nanostructuren die zowel goud als cisplatine bevatten, een conventioneel medicijn voor chemotherapie. Deze werden vrijgegeven in tumorcellen die waren genomen van glioblastoompatiënten en in het laboratorium waren gekweekt.
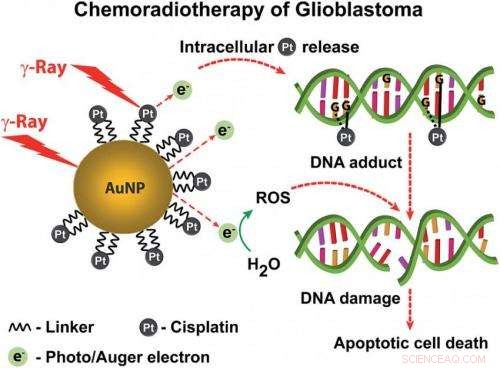
Eenmaal binnen, deze "nanosferen" werden blootgesteld aan radiotherapie. Dit zorgde ervoor dat het goud elektronen vrijmaakte die het DNA van de kankercel en de algehele structuur ervan beschadigden. waardoor de impact van het chemotherapiemedicijn wordt versterkt.
Het proces was zo effectief dat 20 dagen later, de celkweek toonde geen bewijs van enige opleving, wat suggereert dat de tumorcellen waren vernietigd.
Hoewel er nog meer werk moet worden verzet voordat dezelfde technologie kan worden gebruikt om mensen met glioblastoom te behandelen, de resultaten bieden een veelbelovende basis voor toekomstige therapieën. belangrijk, het onderzoek is uitgevoerd op cellijnen die rechtstreeks zijn afgeleid van glioblastoompatiënten, het team in staat stellen om de aanpak van evoluerende, geneesmiddelresistente tumoren.
Het onderzoek werd geleid door Mark Welland, hoogleraar nanotechnologie en een fellow van St John's College, Universiteit van Cambridge, en dr. Colin Watts, een klinisch wetenschapper en honorair adviseur neurochirurg bij de afdeling Klinische Neurowetenschappen. Hun werk wordt gerapporteerd in het tijdschrift Royal Society of Chemistry, nanoschaal .
"De gecombineerde therapie die we hebben bedacht, blijkt ongelooflijk effectief te zijn in de levende celcultuur, Professor Welland zei. "Dit is geen geneesmiddel, maar het laat wel zien wat nanotechnologie kan bereiken bij het bestrijden van deze agressieve vormen van kanker. Door deze strategie te combineren met materialen die kankercellen targeten, we zouden in de toekomst een therapie voor glioblastoom en andere uitdagende kankers moeten kunnen ontwikkelen."
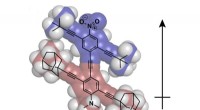
Een diagram dat de samenstelling van de nanosfeer laat zien. Krediet:M. Welland
Daten, glioblastoma multiforme (GBM) is zeer resistent gebleken tegen behandelingen. Een reden hiervoor is dat de tumorcellen de omliggende, gezond hersenweefsel, waardoor de operatieve verwijdering van de tumor vrijwel onmogelijk is.
Op zichzelf gebruikt, chemotherapie medicijnen kunnen een dip veroorzaken in de snelheid waarmee de tumor zich verspreidt. Vaak, echter, dit is tijdelijk, als de celpopulatie dan herstelt.
"We moeten de kankercellen direct kunnen raken met meer dan één behandeling tegelijk", zei Dr. Watts. "Dit is belangrijk omdat sommige kankercellen resistenter zijn tegen het ene type behandeling dan het andere. Nanotechnologie biedt de mogelijkheid om de kankercellen deze 'dubbele klap' te geven en in de toekomst nieuwe behandelingsopties te openen."
In een poging om tumoren uitgebreider te verslaan, wetenschappers doen al geruime tijd onderzoek naar manieren waarop gouden nanodeeltjes in behandelingen kunnen worden gebruikt. Goud is een goedaardig materiaal dat op zichzelf geen bedreiging vormt voor de patiënt, en de grootte en vorm van de deeltjes kan zeer nauwkeurig worden gecontroleerd.
Bij blootstelling aan radiotherapie, de deeltjes zenden een soort laagenergetisch elektron uit, bekend als Auger-elektronen, in staat om het DNA van de zieke cel en andere intracellulaire moleculen te beschadigen. Deze lage energie-emissie betekent dat ze alleen effect hebben op korte afstand, zodat ze geen ernstige schade aanrichten aan gezonde cellen in de buurt.
In de nieuwe studie de onderzoekers wikkelden eerst gouden nanodeeltjes in een positief geladen polymeer, polyethyleenimine. Dit interageerde met eiwitten op het celoppervlak die proteoglycanen worden genoemd, wat ertoe leidde dat de nanodeeltjes door de cel werden opgenomen.
Eenmaal daar, het was mogelijk om het te prikkelen met behulp van standaard radiotherapie, die veel GBM-patiënten als vanzelfsprekend ondergaan. Hierdoor kwamen de elektronen vrij om het cel-DNA aan te vallen.
Terwijl gouden nanosferen, zonder enig begeleidend medicijn, bleken aanzienlijke celschade te veroorzaken, therapieresistente celpopulaties herstelden uiteindelijk enkele dagen na de radiotherapie. Als resultaat, de onderzoekers ontwikkelden vervolgens een tweede nanostructuur die was overgoten met cisplatine.
Het chemotherapeutische effect van cisplatine in combinatie met het radiosensibiliserende effect van gouden nanodeeltjes resulteerde in een verbeterde synergie die een effectievere cellulaire schade mogelijk maakte. Daaropvolgende testen toonden aan dat de behandeling de zichtbare celpopulatie met een factor 100 duizend had verminderd, vergeleken met een onbehandelde celcultuur, binnen een tijdsbestek van slechts 20 dagen. Er is geen populatievernieuwing geconstateerd.
De onderzoekers zijn van mening dat vergelijkbare modellen uiteindelijk kunnen worden gebruikt om andere soorten uitdagende kankers te behandelen. Eerst, echter, de methode zelf moet worden omgezet in een toepasbare behandeling voor GBM-patiënten. Dit proces, dat de focus zal zijn van veel van het komende onderzoek van de groep, zal noodzakelijkerwijs uitgebreide proeven met zich meebrengen. Er moet nog gewerkt worden, te, bij het bepalen hoe de behandeling het beste kan worden uitgevoerd en op andere gebieden, zoals het aanpassen van de grootte en oppervlaktechemie van het nanomedicijn, zodat het lichaam het veilig kan huisvesten.
Sonali Setua, een promovendus die aan het project heeft meegewerkt, zei:"Het was enorm bevredigend om zo'n uitdagend doel na te jagen en om deze agressieve kankercellen te kunnen targeten en vernietigen. Deze bevinding heeft een enorm potentieel om in de nabije toekomst in een klinische proef te worden getest en ontwikkeld tot een nieuwe behandeling om te overwinnen therapeutische resistentie van glioblastoom."
Welland voegde eraan toe dat de betekenis van de resultaten van de groep tot nu toe deels te danken was aan de directe samenwerking tussen nanowetenschappers en clinici. “Het maakte een enorm verschil, omdat we door samen te werken met chirurgen ervoor konden zorgen dat de nanowetenschap klinisch relevant was, " zei hij. "Dat optimaliseert onze kansen om dit verder te brengen dan het laboratoriumstadium, en daadwerkelijk een klinische impact hebben."
 IJsvorming op oppervlakken versterkt via een niet-klassiek kiemvormingsproces
IJsvorming op oppervlakken versterkt via een niet-klassiek kiemvormingsproces Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren
Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren Nieuwe methode kan leiden tot betere in vivo medicijnafgifte
Nieuwe methode kan leiden tot betere in vivo medicijnafgifte Glanzende moleculen maken onderscheid tussen eiwitten in de hersenen
Glanzende moleculen maken onderscheid tussen eiwitten in de hersenen Een hoogwaardige nanopoederfaciliteit voor 3D-printen van metaal
Een hoogwaardige nanopoederfaciliteit voor 3D-printen van metaal
 Australische Black Summer-bosbranden produceerden bijna twee keer zoveel CO2 als alle Australiërs in een jaar
Australische Black Summer-bosbranden produceerden bijna twee keer zoveel CO2 als alle Australiërs in een jaar Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten
Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten Vrij verkeer kan mensen beschermen tegen milieubedreigingen
Vrij verkeer kan mensen beschermen tegen milieubedreigingen Een nieuwe maatstaf voor rampenbestendigheid voor Australische gemeenschappen
Een nieuwe maatstaf voor rampenbestendigheid voor Australische gemeenschappen Worst-case scenario's voor opwarming van de aarde niet geloofwaardig:studie
Worst-case scenario's voor opwarming van de aarde niet geloofwaardig:studie
Hoofdlijnen
- Hoe de cellen van planten, dieren en eencellige organismen te vergelijken
- Droogte geen dingo's achter het uitsterven van tijgers op het vasteland van Australië:studie
- Panspermia:zorgden buitenaardse zaden ervoor dat het leven op aarde explodeerde?
- De structuur en functie van een cel
- Plasmamembraan: definitie, structuur en functie (met diagram)
- Dodelijke vispathogeen gedetecteerd in Australië
- Is het tijd dat ons begrip van evolutie evolueert?
- Bacteriën hebben tastzin
- Onderzoek naar acceptatie van evolutie voor beter wetenschappelijk onderwijs
 Austrian Airlines zegt alle vluchten vanaf donderdag op te schorten vanwege coronavirus
Austrian Airlines zegt alle vluchten vanaf donderdag op te schorten vanwege coronavirus Bezuinigingen op huurtoeslag leidden tot ruim 75, 000 meer overvolle huishoudens tijdens de pandemie
Bezuinigingen op huurtoeslag leidden tot ruim 75, 000 meer overvolle huishoudens tijdens de pandemie Pandemiegedreven verschuiving naar thuiswerk brengt risico's met zich mee, VN zegt
Pandemiegedreven verschuiving naar thuiswerk brengt risico's met zich mee, VN zegt Gevaarlijke druppeldynamiek begrijpen
Gevaarlijke druppeldynamiek begrijpen Opwarming van de aarde zal verschillende vingerafdrukken achterlaten op wereldwijde subtropische anticyclonen
Opwarming van de aarde zal verschillende vingerafdrukken achterlaten op wereldwijde subtropische anticyclonen Vier poten goed, twee beter:studiesporen hagedis bipedalisme
Vier poten goed, twee beter:studiesporen hagedis bipedalisme 200 jaar oude poep toont aan dat landelijke elites in New England parasitaire infecties hadden
200 jaar oude poep toont aan dat landelijke elites in New England parasitaire infecties hadden Grafeen regelt oppervlaktemagnetisme bij kamertemperatuur
Grafeen regelt oppervlaktemagnetisme bij kamertemperatuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com