
Wetenschap
Kankercellen aanvallen met hydrogel-nanodeeltjes

Hydrogel nanodeeltjes. Een artistieke weergave van hydrogel nanodeeltjes. (Tegoed:Andrew Lyon)
(PhysOrg.com) -- Een van de moeilijkheden bij het bestrijden van kanker is dat medicijnen vaak andere niet-kankercellen treffen, waardoor patiënten ziek worden. Maar wat als onderzoekers kankerbestrijdende deeltjes in alleen de kankercellen zouden kunnen sluipen? Onderzoekers van het Georgia Institute of Technology en het Ovarian Cancer Institute werken eraan om precies dat te doen. In het online tijdschrift BMC kanker ze beschrijven een methode die hydrogels gebruikt - minder dan 100 nanometer groot - om een bepaald type klein interfererend RNA (siRNA) in kankercellen te sluipen. Eenmaal in de cel zet het siRNA de geprogrammeerde celdood aan die het lichaam gebruikt om gemuteerde cellen te doden en traditionele chemotherapie te helpen zijn werk te doen.
Veel kankers worden gekenmerkt door een overvloed aan epidermale groeifactorreceptoren (EGFR). Wanneer het EGFR-niveau in een cel verhoogd is, vertelt het de cel om zich met een hoge snelheid te repliceren. Het vermindert ook apoptose, of geprogrammeerde celdood.
“Met onze techniek remmen we de groei van EGFR, met klein interfererend RNA. En door de groei ervan te remmen, we verhogen de apoptotische functie van de cellen. Als we tegelijkertijd de cel raken met chemotherapie, we moeten de kankercellen effectiever kunnen doden, ', zei John Mcdonald, professor aan de School of Biology van Georgia Tech en hoofdonderzoeker van het Ovarian Cancer Institute.
Klein interfererend RNA is goed in het stoppen van de EGFR-productie, maar eenmaal in de cel heeft siRNA een beperkte levensduur. Door het beschermd te houden in de hydrogel-nanodeeltjes, kunnen ze veilig in de kankercel komen en fungeert het als een beschermende barrière om hen heen. De hydrogel geeft slechts een kleine hoeveelheid siRNA per keer af, ervoor te zorgen dat terwijl sommigen in de kankercel hun werk doen, versterkingen worden veilig in het nanodeeltje gehouden totdat het tijd is om hun werk te doen.
“Het is als een paard van Troje, ” zei L. Andrew Lyon, professor aan de School of Chemistry and Biochemistry aan Georgia Tech. “We hebben het oppervlak van deze hydrogels gedecoreerd met een ligand die de kankercel verleidt om het op te nemen. Eenmaal binnen, de deeltjes hebben een langzame afgifteprofiel dat het siRNA over een tijdschaal van dagen uitlekt, waardoor het een therapeutisch effect heeft.”
Cellen gebruiken het boodschapper-RNA (mRNA) om eiwitten te genereren, die helpen om de cel te laten groeien. Zodra het siRNA de cel binnenkomt, het bindt aan het mRNA en rekruteert eiwitten die het siRNA-mRNA-complex aanvallen. Maar de kankercel is nog niet af; het blijft eiwitten genereren, dus zonder een continue aanvoer van siRNA, de cel herstelt. Door de hydrogel te gebruiken om het siRNA langzaam vrij te geven, kan het een aanhoudende aanval volhouden, zodat het de productie van eiwitten kan blijven onderbreken.
“We hebben aangetoond dat je binnen een paar dagen knock-out kunt gaan, die een klinisch venster zou kunnen bieden om binnen te komen en meerdere behandelingen te doen in een combinatie van chemotherapie, ’ zei Lyon.
“Het feit dat dit systeem het siRNA langzaam afgeeft, zonder de cel de tijd te geven om onmiddellijk te herstellen, geeft ons een veel betere efficiëntie bij het doden van de kankercellen met chemotherapie, ', voegde MacDonald eraan toe.
Eerdere technieken hadden betrekking op het gebruik van antilichamen om de eiwitten neer te halen.
“Maar vaak er kan een mutatie optreden in het beoogde gen, zodat het antilichaam niet langer het effect heeft dat het ooit had, waardoor de kans op herhaling toeneemt, ', aldus MacDonald.
Het team gebruikte hydrogels omdat ze niet giftig zijn, een relatief langzame afgiftesnelheid hebben, en kunnen lang genoeg in het lichaam overleven om hun doel te bereiken.
"Het is een goed gedefinieerde architectuur waarin je de intrinsieke porositeit van dat materiaal gebruikt om dingen in te laden, en aangezien onze deeltjes voor ongeveer 98 vol.% uit water bestaan, er is voldoende intern volume om dingen in te laden, ’ zei Lyon.
Momenteel, het is aangetoond dat de tests werken in vitro , maar het team zal tests starten in vivo binnenkort.
 Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af
Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af Afstembaar emissief organisch platform
Afstembaar emissief organisch platform Onderzoekers ontdekken niet eerder onderzocht kankerenzym
Onderzoekers ontdekken niet eerder onderzocht kankerenzym Organisch afval gebruiken om bodemverontreiniging door zware metalen tegen te gaan
Organisch afval gebruiken om bodemverontreiniging door zware metalen tegen te gaan Hoe werkt een calorimeter?
Hoe werkt een calorimeter?
 Sterkere wind zorgt voor smeltend ijs op West-Antarctisch gebied
Sterkere wind zorgt voor smeltend ijs op West-Antarctisch gebied Klimaatverandering en de ineenstorting van Angkor Wat
Klimaatverandering en de ineenstorting van Angkor Wat Soorten moerasgras
Soorten moerasgras  Waarom het geheime wetenschappelijke voorstel van de EPA de volksgezondheidsexperts alarmeert
Waarom het geheime wetenschappelijke voorstel van de EPA de volksgezondheidsexperts alarmeert Gelatinehoudend zoöplankton levert een belangrijke bijdrage aan het transport van koolstof op zee
Gelatinehoudend zoöplankton levert een belangrijke bijdrage aan het transport van koolstof op zee
Hoofdlijnen
- Nieuwe intermoleculaire oppervlaktekracht onthult actomyosine-aandrijfmechanisme
- Door te bezuinigen op milieu-uitgaven, de overheid snijdt kansen
- Hoe telomeren werken
- Hoe virussen de manier veranderen waarop we naar evolutie kijken
- Pogingen om te vangen, red het bedreigde einde van de bruinvis in Mexico
- Soorten redeneren in geometrie
- Wat zijn de functies van een levercel?
- Wat is de eerste stap in het decoderen van genetische berichten?
- Tijgers klampen zich vast aan overleving in steeds meer gefragmenteerde bossen op Sumatras
- Op zoek naar betere lithium-luchtbatterijen, scheikundigen verhogen de stabiliteit van koolstof

- Nanodeeltjes met een schaalstructuur verbeteren de prestaties van zinkoxide-fotodetectoren

- Betrouwbare kwaliteitscontrole van grafeen en andere 2D-materialen is routinematig mogelijk, onderzoekers zeggen:

- Wetenschappers distilleren koemelk tot nanocapsules voor medicijnafgifte
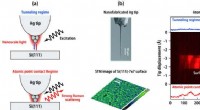
- Ontdekking van enorme Raman-verstrooiing bij contact met atoompunten
 Moge de kracht bij de atoomsonde zijn
Moge de kracht bij de atoomsonde zijn Een nieuw hulpmiddel om de evolutie van sterrenstelsels te bestuderen
Een nieuw hulpmiddel om de evolutie van sterrenstelsels te bestuderen Nieuw onderzoek ontgrendelt eigenschappen voor opslag en computergebruik van kwantuminformatie
Nieuw onderzoek ontgrendelt eigenschappen voor opslag en computergebruik van kwantuminformatie Als je over een aardbeving vloog,
Als je over een aardbeving vloog,  Wetenschappers vinden ontbrekend stuk in voorspellingen van gletsjersmelt
Wetenschappers vinden ontbrekend stuk in voorspellingen van gletsjersmelt Astrofysici 2004-theorie bevestigd:waarom de samenstelling van de zonnen varieert
Astrofysici 2004-theorie bevestigd:waarom de samenstelling van de zonnen varieert Onderzoekers ontwikkelen biologisch afbreekbaar geprint display
Onderzoekers ontwikkelen biologisch afbreekbaar geprint display Een menselijke niche creëren
Een menselijke niche creëren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

