
Wetenschap
Wat is er nodig om een betere batterij te maken?
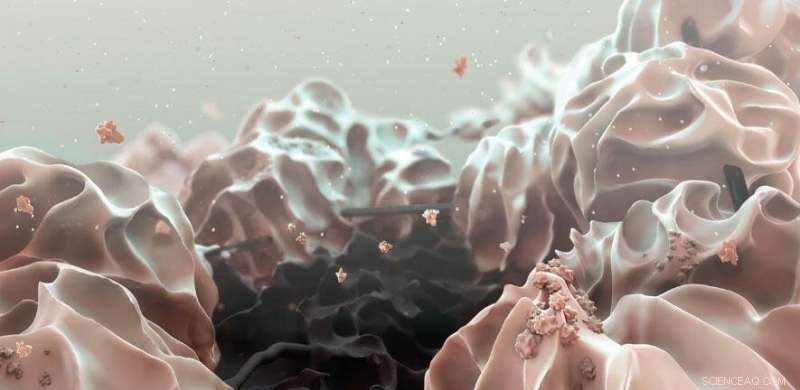
Microscopische weergave in valse kleuren van een gereduceerde grafeenoxide-elektrode (zwart, centrum), die de grote (in de orde van 20 micrometer) lithiumhydroxidedeeltjes (roze) herbergt die zich vormen wanneer een lithium-zuurstofbatterij ontlaadt. Krediet:Valerie Altounian/Wetenschap
Cambridge-onderzoekers werken aan het oplossen van een van de grootste technologische puzzels:hoe batterijen van de volgende generatie te bouwen die een groene revolutie kunnen aandrijven.
Zoals velen van ons, als ik wakker word, pak ik de telefoon op mijn nachtkastje en begin door Twitter te scrollen, Instagram, e-mail- en nieuws-apps. Ik luister naar gestreamde muziek terwijl ik me klaarmaak voor werk en podcasts tijdens mijn woon-werkverkeer. Tegen de tijd dat ik op kantoor kom, mijn telefoon heeft al een boost nodig. Het is nog niet eens 9 uur.
Het is een modern wonder dat we computers in onze zakken hebben die krachtiger zijn dan de computers die de maanlandingen ondersteunden. Maar, ondanks het feit dat de transistors in onze telefoons en laptops elk jaar kleiner en sneller worden, de batterijen die ze van stroom voorzien hebben dat niet.
De sleutel tot het draagbaar maken van elektronica – en het aandrijven van een ommekeer in de manier waarop we communiceren en informatie consumeren – was de commercialisering van lithium-ionbatterijen door Sony in 1991. Lithium-ionbatterijen zijn oplaadbaar, dus wanneer het apparaat is aangesloten op een oplader, herstelt het de batterij voor een ander gebruik.
Hoewel lithium-ionbatterijen onmiskenbare voordelen hebben, zoals relatief hoge energiedichtheden en lange levensduur in vergelijking met andere batterijen en middelen voor energieopslag, ze kunnen ook oververhit raken of zelfs exploderen en zijn relatief duur om te produceren. Aanvullend, hun energiedichtheid komt lang niet in de buurt van die van benzine. Dit maakt ze ongeschikt voor wijdverbreid gebruik in twee belangrijke schone technologieën:elektrische auto's en opslag op elektriciteitsnet voor zonne-energie. Een betere batterij zou het verschil kunnen maken. Dus wat houdt de vooruitgang tegen?
Professor Clare Gray is een van de toonaangevende batterijonderzoekers in het Verenigd Koninkrijk en leidt een grote onderzoeksgroep in Cambridge's Department of Chemistry. Met behulp van methoden zoals NMR-spectroscopie, haar groep bestudeert materialen die kunnen worden gebruikt in batterijen van de volgende generatie, brandstofcellen en supercondensatoren.
Een betere batterij is er een die veel meer energie kan opslaan of een die veel sneller kan worden opgeladen - idealiter beide. Grey's group ontwikkelt een reeks verschillende batterijen van de volgende generatie, inclusief lithium-luchtbatterijen (die oxidatie van lithium en reductie van zuurstof gebruiken om een stroom op te wekken), natriumbatterijen, magnesiumbatterijen en redoxflow-batterijen.
Een werkende lithium-luchtbatterij, bijvoorbeeld, zou een theoretische energiedichtheid hebben die tien keer zo groot is als die van een lithium-ionbatterij, waardoor het potentiële toepassingen in draagbare elektronica, transport en netopslag. Echter, hoewel deze hoge energiedichtheid vergelijkbaar zou zijn met die van benzine, de praktisch haalbare energiedichtheid is merkbaar lager en er moeten nog belangrijke onderzoeksuitdagingen worden aangepakt.
Terwijl Gray samenwerkt met industriële partners om de batterijen die tegenwoordig in elektrische auto's worden gebruikt te verbeteren, ze zegt dat de rol van universiteiten is om na te denken over geheel nieuwe soorten batterijen, zoals degene die ze in haar lab ontwikkelt.
"Universiteiten moeten over tien tot vijftien jaar met antwoorden komen - wij zijn degenen die het best geplaatst zijn om te innoveren, creatief denken en radicale, nieuwe oplossingen, " zegt ze. "We willen ervoor zorgen dat ons werk een impact heeft die veel verder gaat dan de batterijen van vandaag."
Naast het ontwikkelen van geheel nieuwe soorten batterijen, een belangrijk onderdeel van Grey's onderzoek is het opsporen van fouten. Als onderdeel van haar hoogleraarschap gefinancierd door de Royal Society, Gray probeert manieren te vinden om fouten in batterijen te lokaliseren voordat ze zich voordoen.
"Kunnen we indicatoren van fouten in batterijen detecteren voordat ze fout gaan? Als we ze kunnen vinden, dan kunnen we mogelijk voorkomen dat batterijen ontploffen. In aanvulling, we willen onderzoeken of een auto-accu die het einde van zijn levensduur heeft bereikt een tweede leven kan krijgen op het elektriciteitsnet, bijvoorbeeld. Als we zouden kunnen werken, live, waardoor de batterij verslechtert, we kunnen de manier waarop we de batterij gebruiken veranderen, ervoor zorgen dat het langer meegaat, "zegt ze. "Hoe meer we weten over de gezondheidstoestand van een batterij, hoe waardevoller die batterij wordt. Beide strategieën - het verlengen van de levensduur van de batterij en het vinden van een tweede gebruik - leiden tot goedkopere batterijen."
Gray is ook nauw betrokken bij de Faraday Institution, het Britse onafhankelijke nationale onderzoeksinstituut voor batterijen, gefinancierd door de overheid via haar industriële strategie. Ze leidt een van de vier 'fast start'-projecten, met negen andere universitaire en tien industriële partners, om te onderzoeken hoe omgevings- en interne batterijspanningen (zoals hoge temperaturen, laad- en ontlaadsnelheden) beschadigen de accu's van elektrische auto's na verloop van tijd.
"Als je aan andere elektronische apparaten denkt, je denkt over het algemeen maar aan één materiaal, dat is silicium, " zegt Dr. Siân Dutton van Cambridge's Cavendish Laboratory in het Department of Physics, en die ook werkt aan het Faraday Institution-project. "Maar batterijen zijn veel complexer omdat je met meerdere materialen kunt werken, plus alle verpakking, en je moet nadenken over hoe al deze componenten met elkaar omgaan en met welk apparaat je de batterij ook plaatst."
Onder andere projecten, De onderzoeksgroep van Dutton onderzoekt de mogelijkheid van een batterij-elektrolyt dat vast is in plaats van vloeibaar. Een van de belangrijkste veiligheidsproblemen met lithium-ionbatterijen is de vorming van dendrieten - spichtige metaalvezels die een batterij kortsluiten, waardoor de batterij mogelijk vlam vat of zelfs explodeert.
"Als de elektrolyt vast is, echter, je kunt nog steeds dendrieten krijgen, maar de batterijen zullen veel minder snel ontploffen, " zegt ze. "Het is belangrijk voor universiteiten om te kijken naar onconventionele batterijmaterialen zoals degene die we onderzoeken. Als iedereen in dezelfde richting beweegt, we krijgen niet de echte verandering die we nodig hebben."
Het vooruitzicht van een elektrische auto met een bereik van 1, 000 mijl, of een iPhone die in twee minuten oplaadt, of opgeslagen zonne-energie kunnen gebruiken nadat de zon ondergaat, misschien allemaal nog een paar jaar weg. Maar, zegt Gray:"Als we serieus willen overschakelen naar een koolstofarme economie, we moeten nu nadenken over hoe we deze problemen kunnen oplossen. We blijven nieuwe materialen en nieuwe methoden pushen omdat, zonder hen, onderzoeksvelden stagneren."
 Zware metalen uit water verwijderen met MOF's
Zware metalen uit water verwijderen met MOF's Paper Chromatography Science Projects with a Hypothesis
Paper Chromatography Science Projects with a Hypothesis  Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen
Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen Nieuw ontwikkelde molecule om geneesmiddelen te verbeteren, haalt inspiratie uit de gereedschapskist van de natuur
Nieuw ontwikkelde molecule om geneesmiddelen te verbeteren, haalt inspiratie uit de gereedschapskist van de natuur Hoe pure cafeïne te extraheren uit koffie
Hoe pure cafeïne te extraheren uit koffie
 Hoe een ecosysteem in een fles met vissen en planten te maken
Hoe een ecosysteem in een fles met vissen en planten te maken Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem
Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem Filippijnse Everest-veroveraar zet koers naar China
Filippijnse Everest-veroveraar zet koers naar China Vingerafdruk van oude abrupte klimaatverandering gevonden in Noordpoolgebied
Vingerafdruk van oude abrupte klimaatverandering gevonden in Noordpoolgebied Wat zijn de dolfijnen lichaamsdelen?
Wat zijn de dolfijnen lichaamsdelen?
Hoofdlijnen
- Hoe chromosomen vals spelen om kans te maken in een ei te komen
- Oude levensvorm ontdekt in afgelegen Tasmaanse vallei
- De soorten weefsels waarvan DNA kan worden geëxtraheerd om DNA-vingerafdrukken te maken
- Wat is een eencellige eukaryoot?
- Controversiële onkruidverdelger houdt EU in de knoop (Update)
- Genoomonderzoek daagt eerder begrip van de oorsprong van fotosynthese uit
- Cytoplasma bacteriecellen
- Wetenschappers ontcijferen mechanismen die ten grondslag liggen aan de biologie van veroudering
- De machtige Banyan-boom kan eeuwenlang lopen en leven
- Sites zoals Facebook, Google en Twitter lieten blanke supremacisten floreren. Wat nu?

- Dropbox verhoogt prijsklasse voorafgaand aan voorraaddebuut

- Stukje bij beetje, een oplossing om de wegversperring voor energieopslag omver te werpen

- Ghosn:een magnaat vol verrassingen

- Zou Super Mario Bros. beter zijn als je als jezelf kon spelen? We zullen, niet precies

 Hoe Amp om te zetten in Watts op Gasgeneratoren
Hoe Amp om te zetten in Watts op Gasgeneratoren Vissers in New England verliezen banen door klimaat:studie
Vissers in New England verliezen banen door klimaat:studie Naarmate bosbranden erger worden, rook verspreidt zich, wekt gezondheidsproblemen op
Naarmate bosbranden erger worden, rook verspreidt zich, wekt gezondheidsproblemen op Jeff Bezoss Blue Origin-raket maakt 12e testvlucht
Jeff Bezoss Blue Origin-raket maakt 12e testvlucht Roly-Poly Bug Facts
Roly-Poly Bug Facts  Lunar Showstopper:1e superblauwe bloedmaan in 35 jaar
Lunar Showstopper:1e superblauwe bloedmaan in 35 jaar Ruimtewet beschermt je tegen vallend puin, maar er zijn geen wettelijke sancties voor het achterlaten van rommel in een baan om de aarde
Ruimtewet beschermt je tegen vallend puin, maar er zijn geen wettelijke sancties voor het achterlaten van rommel in een baan om de aarde Airbnb geeft toe aan EU-druk op prijsaanbiedingen
Airbnb geeft toe aan EU-druk op prijsaanbiedingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

