
Wetenschap
Chemische vergelijkingen begrijpen:reactanten, producten en stoichiometrie
* De reactanten: Dit zijn de stoffen die bij de reactie betrokken zijn. Ze staan aan de linkerkant van de vergelijking.
* De producten: Dit zijn de nieuwe stoffen die bij de reactie ontstaan. Ze staan aan de rechterkant van de vergelijking.
* De stoichiometrie: Dit verwijst naar de relatieve hoeveelheden van elke betrokken reactant en product. Het wordt weergegeven door de coëfficiënten vóór elke chemische formule.
* De voorwaarden: Soms bevat een chemische vergelijking symbolen of annotaties om de omstandigheden aan te geven waaronder de reactie plaatsvindt, zoals hitte, druk of een katalysator.
Hier leest u hoe u een chemische vergelijking kunt ontleden om te begrijpen wat er gebeurt:
Voorbeeld:
De verbranding van methaan:
CH4 + 2O2 → CO2 + 2H2O
Interpretatie:
* Reactanten: Methaan (CH4) en zuurstof (O2)
* Producten: Kooldioxide (CO2) en water (H2O)
* Stoichiometrie:
* Eén molecuul methaan reageert met twee moleculen zuurstof.
*Er worden één molecuul koolstofdioxide en twee moleculen water geproduceerd.
* Voorwaarden: Deze reactie vereist warmte (meestal een vonk of vlam) om te starten.
Belangrijkste punten:
* Behoud van de massa: Chemische vergelijkingen moeten de wet van behoud van massa volgen, wat betekent dat de totale massa van de reactanten gelijk moet zijn aan de totale massa van de producten. Dit komt tot uiting in de evenwichtige coëfficiënten.
* Pijlen: De pijl (→) geeft de richting van de reactie aan. Het kan een enkele pijl zijn voor een eenrichtingsreactie of dubbele pijlen (⇌) voor een omkeerbare reactie waarbij producten kunnen reageren om opnieuw reactanten te vormen.
* States van materie: Soms wordt de fysische toestand van elke stof tussen haakjes aangegeven na de formule (bijvoorbeeld (s) voor vaste stof, (l) voor vloeistof, (g) voor gas, (aq) voor waterige oplossing).
Over het algemeen zijn chemische vergelijkingen een krachtig hulpmiddel voor het begrijpen en communiceren van de veranderingen die optreden tijdens chemische reacties. Ze stellen ons in staat het proces te visualiseren en de uitkomst van een reactie te voorspellen op basis van de betrokken reactanten en de omstandigheden waaronder deze plaatsvindt.
 Neemt het kannibalisme onder ijsberen toe?
Neemt het kannibalisme onder ijsberen toe?  Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië
Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië Plankton als klimaatdriver in plaats van de zon?
Plankton als klimaatdriver in plaats van de zon? Minnesota neemt regels voor schone auto's aan die meer elektrische voertuigen vereisen
Minnesota neemt regels voor schone auto's aan die meer elektrische voertuigen vereisen Oude schedel die waarschijnlijk toebehoort aan 's werelds oudste tsunami-slachtoffer
Oude schedel die waarschijnlijk toebehoort aan 's werelds oudste tsunami-slachtoffer
Hoofdlijnen
- Welke woorden beschrijven en beïnvloeden de evolutietheorie?
- Voordat de celdeling begint, bestaat elke chromosomen uit twee identieke verbonden genaamd?
- Uit onderzoek blijkt hoe lysozymeiwit in tranen gevaarlijke bacteriën vernietigt
- Onderzoekers ontdekken hoe voedselvergiftigingsbacteriën de darmen infecteren
- Waarom bouwen organismen weefsels die ze schijnbaar nooit gebruiken?
- Ribosomen: definitie, functie en structuur (eukaryoten en prokaryoten)
- Wat zijn niet -osjunctie -genen?
- Zangvogels met unieke kleuren worden eerder als huisdier verhandeld
- Welke structuur in de cel bevat instructies die vertellen hoe ze eiwitten kunnen maken?
- Het begrijpen van bederf- en kwaliteitsproblemen kan de Amerikaanse ambachtelijke kaasindustrie verbeteren

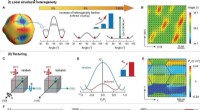
- Ultrahoge piëzo-elektrische prestaties aangetoond in keramische materialen
- Bioplottering van bot-mimetische 3D-weefselsteigers met osteogene effecten

- Onderzoekers identificeren nieuw proces om ammoniak te produceren met een veel kleinere ecologische voetafdruk

- Gegevensopslag met behulp van individuele moleculen

 Hoe worden magneten gebruikt in tv's?
Hoe worden magneten gebruikt in tv's?  Waar wordt de zon gevonden?
Waar wordt de zon gevonden?  Hoe doorzoeken reddingsteams een ondergelopen stad?
Hoe doorzoeken reddingsteams een ondergelopen stad?  Waarom zijn diepe waterstromingen belangrijk?
Waarom zijn diepe waterstromingen belangrijk?  Welke factoren helpen het type grond te bepalen, zoals diktelagen en hun samenstelling?
Welke factoren helpen het type grond te bepalen, zoals diktelagen en hun samenstelling?  Hoe label je een Bohr-model voor scandium?
Hoe label je een Bohr-model voor scandium?  Staat de Brunt-ijsplaat op de rand?
Staat de Brunt-ijsplaat op de rand?  Hoe de dag te berekenen dat ik geboren was
Hoe de dag te berekenen dat ik geboren was
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

