
Wetenschap
Bereken de pH van een 0,15 M calciumhydroxide-oplossing:stapsgewijze handleiding
1. Begrijp de dissociatie:
Calciumhydroxide (Ca(OH)₂) is een sterke base. Het dissocieert volledig in water:
Ca(OH)₂ (water) → Ca²⁺ (water) + 2OH⁻ (water)
Dit betekent dat je voor elke mol Ca(OH)₂ die oplost, 2 mol hydroxide-ionen (OH⁻) krijgt.
2. Bereken de hydroxide-ionenconcentratie:
* Omdat de concentratie van Ca(OH)₂ 0,15 M is, is de concentratie van OH⁻-ionen het dubbele:0,15 M * 2 =0,30 M
3. Bereken de pOH:
pOH is de negatieve logaritme van de hydroxide-ionconcentratie:
pOH =-log[OH⁻] =-log(0,30) ≈ 0,52
4. Bereken de pH:
De pH en pOH zijn gerelateerd aan de volgende vergelijking:
pH + pOH =14
Daarom:
pH =14 - pOH =14 - 0,52 ≈ 13,48
Daarom is de pH van een 0,15 M calciumhydroxideoplossing ongeveer 13,48.
 Wat is de belangrijkste bron van koolstof in een ecosysteem?
Wat is de belangrijkste bron van koolstof in een ecosysteem?  Uit de hand gelopen Australische bosbrand bedreigt huizen in Perth
Uit de hand gelopen Australische bosbrand bedreigt huizen in Perth Waar staten rangschikken op de overdracht van waterrechten
Waar staten rangschikken op de overdracht van waterrechten Dieren van de Coastal Desert Biome
Dieren van de Coastal Desert Biome  India moet de infrastructuurbehoeften heroverwegen om 100 nieuwe slimme steden duurzaam te maken
India moet de infrastructuurbehoeften heroverwegen om 100 nieuwe slimme steden duurzaam te maken
Hoofdlijnen
- Hoe vertelt de kern cell wat te doen?
- Hoe je een groeiende bevolking gezond voedsel kunt geven zonder de planeet te ruïneren
- Welke structuren voeren celbeweging uit?
- Wat scheiden elke spijsverteringsklier af?
- Is de oorsprong van gekweekte kumquatsoorten betrokken bij kumquats uit Hong Kong? Waarschijnlijk niet
- Wat is het gebruik en de toepassing van de biologische wetenschap?
- Evolutie in actie? Nieuwe studie vindt de mogelijkheid van stikstofbindende organellen
- Hoe beïnvloedt stress je hersens?
- Wat is een zuivere eigenschap en een hybride eigenschap?
- Slimme truc maakt 20 keer snellere beeldvorming mogelijk met elektronenmicroscopie
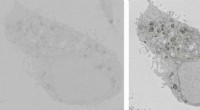
- Deze kunstmatige eiwitten hebben een stevige greep op metaal
- Isolatie met popcorn?

- Elk moment van ultrasnelle chemische binding vastgelegd op film
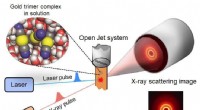
- Een nieuwe horizon voor vibrationele circulair dichroïsme spectroscopie
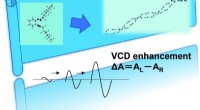
 Waarom groeien de cellen getransformeerd met PUC18 en Plasmide Lux in aanwezigheid van ampicilline?
Waarom groeien de cellen getransformeerd met PUC18 en Plasmide Lux in aanwezigheid van ampicilline?  Ondanks het koude weer, Mongolen protesteren tegen verslechterende smog
Ondanks het koude weer, Mongolen protesteren tegen verslechterende smog Deeltjesdetectoren een boost geven:nieuw apparaat werkt als een supergeleidingsschakelaar
Deeltjesdetectoren een boost geven:nieuw apparaat werkt als een supergeleidingsschakelaar  Wat is het verschil tussen een kasteel en een paleis?
Wat is het verschil tussen een kasteel en een paleis?  Wat is de atomaire radii -grootte voor alkali -metalen?
Wat is de atomaire radii -grootte voor alkali -metalen?  Welk metaal heeft de specifieke warmte van 0,30?
Welk metaal heeft de specifieke warmte van 0,30?  Hoeveel centimeter is drie en de helft?
Hoeveel centimeter is drie en de helft?  Waar komt de energie in fotosynthese vandaan?
Waar komt de energie in fotosynthese vandaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

