
Wetenschap
Hoe heeft Thomson ons begrip van het atoom geholpen?
1. Discovery of the Electron (1897):
* Experiment: Thomson voerde experimenten uit met kathodestraalbuizen. Hij merkte op dat stralen uit de kathode werden afgebogen door zowel elektrische als magnetische velden, wat bewees dat ze een negatieve lading droegen.
* Betekenis: Dit markeerde de eerste ontdekking van een subatomair deeltje, waaruit blijkt dat het atoom niet ondeelbaar was zoals eerder werd gedacht.
2. The Plum Pudding Model (1904):
* Model: Op basis van zijn bevindingen stelde Thomson een model voor waarbij het atoom een sfeer was van positief geladen materie (zoals pudding) met negatief geladen elektronen ingebed (zoals pruimen).
* impact: Dit model daagde het toenmalige aanzicht op het atoom uit als een solide sfeer. Het introduceerde het concept van subatomaire deeltjes en hun opstelling in het atoom.
Het werk van Thomson leidde tot verschillende cruciale vooruitgang in de atomaire theorie:
* sloop van het ondeelbare atoomconcept: Zijn ontdekking van het elektron bewees dat atomen inderdaad uit kleinere deeltjes waren samengesteld.
* Inleiding van het concept van subatomaire deeltjes: Dit maakte de weg vrij voor verdere ontdekkingen en de ontwikkeling van moderne atoommodellen.
* Foundation for Future Research: Thomson's model, hoewel later vervangen, vormde het toneel voor het baanbrekende goudfolie -experiment van Rutherford en de ontwikkeling van het nucleaire model.
Hoewel het "pruimpuddingmodel" uiteindelijk onnauwkeurig werd bewezen, was het een belangrijke stap om de structuur van het atoom te begrijpen. Het bood een raamwerk voor toekomstig onderzoek en maakte uiteindelijk de weg vrij voor het moderne begrip van het atoom als een kern omringd door elektronen.
 Hoe wordt de protongradiënt vastgesteld?
Hoe wordt de protongradiënt vastgesteld?  CuCl2 plus H2S voorspellen de producten?
CuCl2 plus H2S voorspellen de producten?  Een natuurlijk voorkomende stof in de vaste anorganische kristallijne toestand wordt bekend als een?
Een natuurlijk voorkomende stof in de vaste anorganische kristallijne toestand wordt bekend als een?  Antibacteriële prodrug door zich te richten op intracellulaire metaboliet
Antibacteriële prodrug door zich te richten op intracellulaire metaboliet Welk element accepteert het meest gemakkelijk elektronen?
Welk element accepteert het meest gemakkelijk elektronen?
 Dekkingskosten terugverdiend op Rolling Plains-katoen
Dekkingskosten terugverdiend op Rolling Plains-katoen VN waarschuwt dat impact van Caribische vulkaan andere eilanden kan treffen
VN waarschuwt dat impact van Caribische vulkaan andere eilanden kan treffen Onderzoekers analyseren infrastructuur en demografische gegevens om te zien waar tornado's het meest ontwrichtend zijn
Onderzoekers analyseren infrastructuur en demografische gegevens om te zien waar tornado's het meest ontwrichtend zijn  Nieuwe technologie verandert een zonnige dag in veilig water
Nieuwe technologie verandert een zonnige dag in veilig water  Ecoloog gebruikt wetenschappelijke benadering om 's werelds ergste problemen in nieuw boek te rangschikken
Ecoloog gebruikt wetenschappelijke benadering om 's werelds ergste problemen in nieuw boek te rangschikken
Hoofdlijnen
- Levensduur verlengd door remming van gemeenschappelijk enzym
- Bij het analyseren van resultaten regelen wetenschappers soms gegevens in wat?
- Wat is het enige menselijke orgaan dat zichzelf regenereert?
- Hoe genenpools werken
- Soorten sporenvormende bacteriën
- Hoe ondersteunt homologe structuur de evolutietheorie?
- De kern van het kweken van cowpea onder moeilijke omstandigheden
- Hoe ontwikkelen Candida auris en andere schimmels resistentie tegen geneesmiddelen? Een microbioloog legt het uit
- Wat is het IG -kanaal?
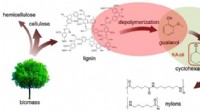
- Nieuw proces verandert papierproductieafval in waardevolle chemicaliën
- Video — Wijnsnobisme:feit versus fictie

- Onderzoek onthult eerste bewijs van RNA-getriggerde fasescheiding
- Nieuwe vingerafdrukken toegevoegd aan database voor chemische identificatie

- Diamanten in uw apparaten:kracht voor de volgende generatie energieopslag

 Steunt dendrieten het axon van binnenuit?
Steunt dendrieten het axon van binnenuit?  Hoe breng je chemische formules in evenwicht?
Hoe breng je chemische formules in evenwicht?  Boeren die zich niet bewust zijn van hun activiteiten veroorzaken klimaatschokken
Boeren die zich niet bewust zijn van hun activiteiten veroorzaken klimaatschokken Hoe te stoppen LED-lampjes knipperen te snel
Hoe te stoppen LED-lampjes knipperen te snel  Voorbeelden van een recessief allel
Voorbeelden van een recessief allel  Hoe kristal een geleider wordt
Hoe kristal een geleider wordt  Milieuproblemen in verband met kust- en binnenlandse natte gebieden
Milieuproblemen in verband met kust- en binnenlandse natte gebieden Lanceringsdatum vastgesteld voor NASA's PREFIRE-missie om polair energieverlies te bestuderen
Lanceringsdatum vastgesteld voor NASA's PREFIRE-missie om polair energieverlies te bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

