
Wetenschap
Hoe verschilt de moderne atoomtheorie van de Daltons -theorie?
Dalton's atomaire theorie:
* atomen zijn ondeelbaar en onverwoestbaar: Dit is nu bekend als onjuist. Atomen bestaan uit kleinere subatomaire deeltjes (protonen, neutronen en elektronen).
* Alle atomen van een bepaald element zijn identiek: Dit is ook onjuist. Isotopen van hetzelfde element hebben verschillende aantallen neutronen, waardoor ze iets anders in massa zijn.
* Atomen van verschillende elementen hebben verschillende massa's: Dit is correct. Verschillende elementen hebben verschillende aantallen protonen, wat resulteert in verschillende atoommassa's.
* Atomen combineren in gehele nummerverhoudingen om verbindingen te vormen: Dit wordt nog steeds als geldig beschouwd en weerspiegelt het idee van chemische formules en stoichiometrie.
Moderne atomaire theorie:
* atomen zijn deelbaar en bestaan uit subatomaire deeltjes: De ontdekking van protonen, neutronen en elektronen, en de daaropvolgende ontwikkeling van de kwantummechanica, veranderde ons begrip van de structuur van het atoom.
* Atomen van hetzelfde element kunnen verschillende aantallen neutronen (isotopen) hebben: Isotopen hebben hetzelfde aantal protonen maar verschillende aantallen neutronen, wat leidt tot variaties in atomaire massa.
* Elektronen bezetten specifieke energieniveaus (orbitalen): Elektronen draaien niet om de kern in een gedefinieerd pad zoals planeten rond de zon. In plaats daarvan bezetten ze specifieke energieniveaus, die overeenkomen met verschillende orbitalen.
* Atomen kunnen elektronen winnen, verliezen of delen om bindingen te vormen: Dit verklaart chemische reacties, waarbij atomen interageren door het overbrengen of delen van elektronen om moleculen te vormen.
Samenvattend:
De moderne atoomtheorie heeft de theorie van Dalton verfijnd en uitgebreid, met de ontdekking van subatomaire deeltjes, het bestaan van isotopen en de kwantumkarakter van elektronen. Terwijl de theorie van Dalton de basis legde voor ons begrip van materie, biedt de moderne atoomtheorie een veel gedetailleerder en nauwkeuriger beeld van de structuur en het gedrag van het atoom.
 Waarom lossen sommige stoffen niet in water op in water?
Waarom lossen sommige stoffen niet in water op in water?  Op de natuur geïnspireerd materiaal maakt gebruik van vloeibare versterking
Op de natuur geïnspireerd materiaal maakt gebruik van vloeibare versterking De afbraak van water kan worden veroorzaakt door?
De afbraak van water kan worden veroorzaakt door?  Nieuw record voor lengte koolstof-koolstof enkelvoudige binding
Nieuw record voor lengte koolstof-koolstof enkelvoudige binding Hoe bevordert chemische verwering mechanische verwering?
Hoe bevordert chemische verwering mechanische verwering?
 Tijdstip van vogelmigratie vertekend door klimaat, nieuwe onderzoeksresultaten
Tijdstip van vogelmigratie vertekend door klimaat, nieuwe onderzoeksresultaten Experts zeggen stedelijke wildgroei, klimaatverandering wandelen natuurbrandrisico
Experts zeggen stedelijke wildgroei, klimaatverandering wandelen natuurbrandrisico 5 tips om kinderen te leren over duurzaam leven
5 tips om kinderen te leren over duurzaam leven  Cool plan:studie zegt dat betere airconditioning de opwarming van de aarde kan vertragen
Cool plan:studie zegt dat betere airconditioning de opwarming van de aarde kan vertragen Watervoorziening van Honduras in kaart brengen
Watervoorziening van Honduras in kaart brengen
Hoofdlijnen
- Bereidheid om risico's te nemen - een persoonlijkheidskenmerk
- Kopiëren of innoveren? Studie werpt licht op chimpanseecultuur
- Hoe DNA wordt vernietigd door virus?
- Geliefde hondenrassen zullen net zo vaak bijten als verboden hondenrassen. Hier leest u hoe u ze kunt stoppen
- Waarom zijn eiwitten belangrijk voor de biochemie?
- Zullen grote ambities op het gebied van biodiversiteit voldoende zijn om de natuur te redden?
- Onderzoek toont aan dat plantengroeiregulatoren gunstig kunnen zijn voor de vestiging van uien, productie
- Wat is de functie van het reproductieve systeem van de organen?
- Onderzoekers lossen het oude mysterie op over hoe fagen pathogene bacteriën ontwapenen
- Geautomatiseerde optimalisatie en synthese van geneesmiddelen in de cloud

- Licht in het donker schijnen:nieuwe ontdekking maakt microscopische beeldvorming mogelijk in donkere omstandigheden

- Waarom macrofagen rusten in gezond weefsel?
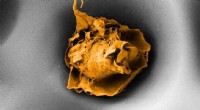
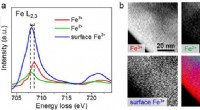
- Efficiënte waterstofconversie door splitsing van water door zonne-energie met behulp van op hematiet-mesocrystal gebaseerde fotoanodes
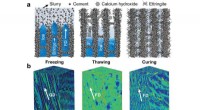
- Op hout geïnspireerd cement met hoge sterkte en multifunctionaliteit
 3D-luchtkaarten helpen bij het herstel van Australische brandweer
3D-luchtkaarten helpen bij het herstel van Australische brandweer Hoe beïnvloedt atomaire structuur interacties tussen atomen?
Hoe beïnvloedt atomaire structuur interacties tussen atomen?  Wat maakt een vaste stof anders dan een vloeistof?
Wat maakt een vaste stof anders dan een vloeistof?  Wat zijn de vijf meest voorkomende kenmerken die in alle energieoverdrachtsystemen?
Wat zijn de vijf meest voorkomende kenmerken die in alle energieoverdrachtsystemen?  Hoe is het lichtste deel van de schaduw die een zonsverduistering noemde?
Hoe is het lichtste deel van de schaduw die een zonsverduistering noemde?  Documentaires met grote problemen veranderen niet altijd ons gedrag
Documentaires met grote problemen veranderen niet altijd ons gedrag Hoe aardverschuivingen werken
Hoe aardverschuivingen werken  Wat zijn feiten over energietransformatie?
Wat zijn feiten over energietransformatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

