
Wetenschap
Waarom natriumion langzaam diffunderen dan een chloorion?
* Grootte: Natriumionen (Na+) zijn kleiner dan chloride-ionen (Cl-). Kleinere ionen diffunderen over het algemeen sneller omdat ze minder weerstand ervaren van het omliggende medium.
* Hydratatie: Ionen in oplossing worden omgeven door watermoleculen en vormen een hydratatieschaal. De sterkte van de hydratatieschaal beïnvloedt diffusie. Chloride -ionen hebben een zwakkere hydratatieschelp dan natriumionen, wat betekent dat ze minder worden bezwaard door watermoleculen en gemakkelijker kunnen diffunderen.
* opladen: Chloride -ionen hebben een enkele negatieve lading, terwijl natriumionen een enkele positieve lading hebben. De lading van een ion draagt ook bij aan zijn interactie met watermoleculen, en dit kan de diffusiesnelheden beïnvloeden. De effecten van de grootte en de hydratatieschaal zijn echter over het algemeen belangrijker.
factoren die de relatieve diffusiesnelheden van ionen kunnen beïnvloeden:
* Temperatuur: Hogere temperaturen leiden tot snellere diffusie.
* concentratiegradiënt: Een steilere concentratiegradiënt resulteert in snellere diffusie.
* medium: De viscositeit en samenstelling van het medium kunnen de diffusiesnelheden beïnvloeden.
Samenvattend:
Hoewel het verleidelijk is om te denken dat zwaardere ionen langzamer zouden diffunderen, is de grootte, hydratatie en lading van de ionen zijn belangrijker factoren. In de meeste gevallen diffunderen chloride -ionen sneller dan natriumionen .
 CryoSat onthult ijsverlies door gletsjers in Alaska en Azië
CryoSat onthult ijsverlies door gletsjers in Alaska en Azië Planetaire wetenschappers ontrafelen mysterie van Egyptisch woestijnglas
Planetaire wetenschappers ontrafelen mysterie van Egyptisch woestijnglas Waarom werd de perspectieftechniek in deze periode niet als mooi beschouwd?
Waarom werd de perspectieftechniek in deze periode niet als mooi beschouwd?  Redactioneel:Bescherm de milieu-erfenis van Californië tegen de aanvallen van Trump
Redactioneel:Bescherm de milieu-erfenis van Californië tegen de aanvallen van Trump Wat betekent doel in de wetenschap?
Wat betekent doel in de wetenschap?
Hoofdlijnen
- De ontdekking van een atypische hitteschokfactor, HSF5, die betrokken is bij meiotische mechanismen, heeft implicaties voor mannelijke onvruchtbaarheid
- Welk epitheel wordt alleen in een dikke huid gevonden?
- Delen van een dierencel voor kinderen
- Evolutie van de geslachten:wat een schimmel ons kan vertellen
- Onderzoekers verwachten dat nieuwe vispassage de trekvispopulaties zal herstellen
- Onderzoek onthult inzichten in de evolutie van eiwitten
- Wat is een wetenschapper die alles bestudeert?
- Waarom hebben eencellige organismen geen complexe structuren nodig voor gasuitwisseling?
- Scheidingswanden:hoe immuuncellen weefsel binnendringen
- Garen gemaakt van huidcellen kan worden geweven in menselijk textiel

- Xylitol en cellulose nanovezels maken van papierpasta – naar een groene en duurzame samenleving
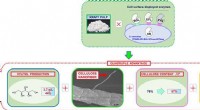
- Maretakbessen kunnen het geheim bevatten voor het maken van biologische superlijm

- Nieuwe RNA-modificerende tool corrigeert genetische ziekten, inclusief aanjager van triple-negatieve borstkanker

- De ontdekking van vloeibaar metaal luidt een nieuwe golf van chemie en elektronica in

 Oppervlakte-effecten beïnvloeden de verdeling van waterstof in metalen
Oppervlakte-effecten beïnvloeden de verdeling van waterstof in metalen Welke term wordt gebruikt om de massa van 1 mol moleculen van een stof weer te geven?
Welke term wordt gebruikt om de massa van 1 mol moleculen van een stof weer te geven?  Hoe beïnvloedt ionische binding de eigenschappen van verbindingen?
Hoe beïnvloedt ionische binding de eigenschappen van verbindingen?  Wat is de kracht die planeten in een baan om sterren en satellietenplaneten in een baan houdt?
Wat is de kracht die planeten in een baan om sterren en satellietenplaneten in een baan houdt?  Welk voorvoegsel verhoogt een SI -eenheid 1000 keer?
Welk voorvoegsel verhoogt een SI -eenheid 1000 keer?  Flexibele all-carbon elektronica geïntegreerd in planten, insecten, en meer
Flexibele all-carbon elektronica geïntegreerd in planten, insecten, en meer Hoe verhoudt een sterren radii zich tot hun massa?
Hoe verhoudt een sterren radii zich tot hun massa?  Haarlokken kunnen levensstijlgeheimen van criminelen onthullen
Haarlokken kunnen levensstijlgeheimen van criminelen onthullen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

