
Wetenschap
Functie van katalysator en remmer in reactiekinetisch?
katalysator en remmer in reactiekinetiek
katalysatoren en remmers Speel cruciale rollen bij het beïnvloeden van de snelheid van chemische reacties. Ze doen dit zonder in het proces te worden geconsumeerd, wat betekent dat ze herhaaldelijk kunnen worden gebruikt. Hier is een uitsplitsing van hun functies:
katalysator:
* Definitie: Een stof die de snelheid van een chemische reactie verhoogt zonder tijdens het proces te worden geconsumeerd.
* mechanisme: Katalysatoren bieden een alternatieve reactieroute met een lagere activeringsenergie. Dit betekent dat meer moleculen voldoende energie hebben om bij een gegeven temperatuur te reageren, wat leidt tot een snellere reactiesnelheid.
* Effect op reactiekinetiek:
* Lagere activeringsenergie (EA): Dit is het belangrijkste aspect van de katalyse. Een lagere EA resulteert in een snellere snelheidsconstante (k) volgens de Arrhenius -vergelijking.
* Verhoogde reactiesnelheid: Vanwege de verlaagde EA verloopt de reactie sneller bij een bepaalde temperatuur.
* Geen verandering in evenwichtsconstante (k): Katalysatoren hebben geen invloed op de positie van het evenwicht, alleen de snelheid waarmee deze wordt bereikt.
Voorbeelden:
* enzymen: Biologische katalysatoren die specifieke biochemische reacties in levende organismen versnellen.
* metalen katalysatoren: Gebruikt in verschillende industriële processen zoals het Haber-Bosch-proces voor ammoniaksynthese.
remmer:
* Definitie: Een stof die een chemische reactie vertraagt of voorkomt.
* mechanisme:
* het blokkeren van de actieve site: Remmers kunnen binden aan de actieve plaats van een katalysator, waardoor deze niet in wisselwerking staat met de reactanten.
* De structuur van de katalysator wijzigen: Remmers kunnen de structuur van de katalysator veranderen, waardoor deze minder effectief is.
* reageren met reactanten: Remmers kunnen reageren met reactanten, waardoor ze uit het reactiemengsel worden verwijderd.
* Effect op reactiekinetiek:
* Verhoogde activeringsenergie (EA): Remmers verhogen over het algemeen de activeringsenergie, waardoor de reactie wordt vertraagd.
* verlaagde reactiesnelheid: De reactie verloopt langzamer bij een bepaalde temperatuur vanwege de hogere EA.
* Geen verandering in evenwichtsconstante (k): Net als katalysatoren verschuiven remmers het evenwichtspunt niet, alleen de snelheid waarmee het wordt bereikt.
Voorbeelden:
* antioxidanten: Remt oxidatiereacties die bederf in voedsel veroorzaken.
* corrosieremmers: Voorkom dat metalen oppervlakken roesten of corroderen.
Belangrijkste verschillen:
| Feature | Katalysator | Remmer |
| ---------------- | ---------- | ---------- |
| Effect op snelheid | Verhoogt | Daalt |
| Effect op EA | Daalt | Verhoogt |
| Effect op K | Geen verandering | Geen verandering |
| Consumptie | Niet geconsumeerd | Niet geconsumeerd |
Samenvattend: Katalysatoren versnellen de reacties door alternatieve routes te bieden met lagere activeringsenergieën, terwijl remmers de reacties vertragen door de activeringsenergie te vergroten of actieve plaatsen te blokkeren. Beide spelen een belangrijke rol bij het regelen van de reactiesnelheden en hebben brede toepassingen op verschillende gebieden.
 Diepeutectische oplosmiddelen vervangen vervuilende industriële oplosmiddelen
Diepeutectische oplosmiddelen vervangen vervuilende industriële oplosmiddelen Welk atoom krijgt de meeste negatieve lading in een covalente binding met waterstof?
Welk atoom krijgt de meeste negatieve lading in een covalente binding met waterstof?  Wat is het verband tussen bijen- en wespensteken en zure alkaliën?
Wat is het verband tussen bijen- en wespensteken en zure alkaliën?  Hoeveel mol in 114 g SBCL3?
Hoeveel mol in 114 g SBCL3?  Nieuwe minerale piëzokatalysatoren bieden innovatieve benaderingen voor bodemsanering
Nieuwe minerale piëzokatalysatoren bieden innovatieve benaderingen voor bodemsanering
 Door klimaat veroorzaakte honger is meer dan verdubbeld in zwaarst getroffen landen:rapport
Door klimaat veroorzaakte honger is meer dan verdubbeld in zwaarst getroffen landen:rapport Wat moet een feit zijn een observatie of gevolgtrekking?
Wat moet een feit zijn een observatie of gevolgtrekking?  Studie onderzoekt hoeveel klimaatverandering het risico op gewapende conflicten beïnvloedt
Studie onderzoekt hoeveel klimaatverandering het risico op gewapende conflicten beïnvloedt  Virginia ziet plotselinge toename van het aantal eikenbomen, boswachters zeggen:
Virginia ziet plotselinge toename van het aantal eikenbomen, boswachters zeggen: Tafelresten kunnen worden gebruikt om de afhankelijkheid van fossiele brandstoffen te verminderen
Tafelresten kunnen worden gebruikt om de afhankelijkheid van fossiele brandstoffen te verminderen
Hoofdlijnen
- Wat is de relatie tussen chromosomen en genen -DNA?
- Nieuwe onderzoeken laten zien hoe je parasieten kunt redden en waarom dit belangrijk is
- Wat is de rol van nitrofying -bacteriën?
- Welke weefsels komen voor in planten en dieren?
- Kunnen mechanismen die tijdens de winterslaap worden gebruikt, dieren helpen nieuwe habitats te koloniseren?
- Wanneer is een worm geen worm? het zijn kwallen...
- Hebben zowel dier- als plantencellen semipermeabele membranen?
- Wat gebeurt er met een palissadecel als deze in een verdunde glucoseoplossing wordt geplaatst?
- Nieuwe ontdekking vergroot het begrip van hoe planten en bacteriën licht zien
- Eerste direct bewijs van chemische reacties in deeltjes

- Studie toont afstembaarheid van een moleculaire chaperonne aan

- Ingenieurs ontwikkelen kameleonmetalen die van oppervlak veranderen als reactie op hitte
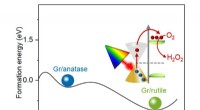
- Verbetering van de productie van waterstofperoxide door duurzame fotokatalyse
- Bio-ingenieurs onthullen verrassende zintuiglijke en zelfgenezende vermogens van zeedieren

 Waarom leren wetenschappers over de planeet?
Waarom leren wetenschappers over de planeet?  Wat wordt bedoeld met fenotype plasticiteit in wortels en scheuten?
Wat wordt bedoeld met fenotype plasticiteit in wortels en scheuten?  Wat zijn de twee vormen van wetenschappelijke methode?
Wat zijn de twee vormen van wetenschappelijke methode?  Antarctische ijskliffen dragen mogelijk niet zoveel bij aan zeespiegelstijging als voorspeld
Antarctische ijskliffen dragen mogelijk niet zoveel bij aan zeespiegelstijging als voorspeld Welke koninkrijken zijn heterotrofisch en autotroof?
Welke koninkrijken zijn heterotrofisch en autotroof?  Rossby-golven beïnvloeden ons weer en getijden, maar wat zijn ze?
Rossby-golven beïnvloeden ons weer en getijden, maar wat zijn ze? Hoe zagen de eerste slangen eruit?
Hoe zagen de eerste slangen eruit?  Waarom is kopersulfaat blauw?
Waarom is kopersulfaat blauw?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

