
Wetenschap
Is BACL2 plus Na2SO4 een redox -reactie?
* Redox -reacties omvatten een verandering in oxidatietoestanden. Bij redoxreacties wint de ene soort elektronen (reductie) terwijl de andere elektronen verliest (oxidatie).
* In deze reactie is er geen verandering in oxidatietoestanden. Barium (BA), chloor (CL), natrium (Na), zwavel (s) en zuurstof (O) handhaven allemaal hun dezelfde oxidatietoestanden tijdens de reactie.
De reactie is een dubbele verplaatsingsreactie:
Bacl₂ (aq) + na₂so₄ (aq) → baso₄ (s) + 2 NaCl (aq)
Verklaring:
* De kationen (ba²⁺ en na⁺) en anionen (cl⁻ en so₄²⁻) wisselen eenvoudig van partners.
* Bariumsulfaat (Baso₄) is onoplosbaar in water en neerslaat uit oplossing.
Key Takeaway: Hoewel de reactie een chemische verandering inhoudt, is het geen redox -reactie omdat er geen overdracht van elektronen is en geen verandering in oxidatietoestanden.
 Stralingsrisico op historische kernproeflocatie in WA, 70 jaar later
Stralingsrisico op historische kernproeflocatie in WA, 70 jaar later Wat zijn de effecten van niet-biologisch afbreekbaar afval?
Wat zijn de effecten van niet-biologisch afbreekbaar afval?  Fabrieken in Bangladesh moeten sluiten om belangrijke rivier te redden
Fabrieken in Bangladesh moeten sluiten om belangrijke rivier te redden Hoe past de varenplant zich aan aan zijn omgeving?
Hoe past de varenplant zich aan aan zijn omgeving?  Nieuwe methode maakt weersvoorspellingen zo goed als regen
Nieuwe methode maakt weersvoorspellingen zo goed als regen
Hoofdlijnen
- Waarom denk je dat het bestuderen van biologie essentieel is?
- Onderscheid maken tussen ouderlijke en recombinante fenotypes?
- Wat hebben vleermuizen, priesters en rabbijnen gemeen? Netwerkanalyse levert inzichten op
- leeuwen, chimpansees, haaien krijgen extra bescherming onder VN-verdrag
- Wat zijn de voordelen en nadelen van Flow Cytometry?
- Wat waren Gregor -wetten van genetica?
- Wat is een microscopisch kleine eencellige, eenvoudige plant, waarvan sommige schadelijk en nuttig zijn om te vormen?
- Hoe en wat horen vleermuizen?
- Hoe zeer resistente schimmelsoorten ontstaan
- Een manier om polystyreen te recyclen tot waardevollere producten

- Herbevestigen van de waarde van internationale samenwerkingen

- Designer-enzym overwint sulfietreductie, een knelpunt bij het opruimen van het milieu

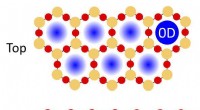
- Het bedekken van metalen katalysatoroppervlakken met dunne tweedimensionale oxidematerialen kan chemische reacties versterken
- Duurzamere recycling van kunststoffen

 Waarom worden covalente obligaties directionele obligaties genoemd?
Waarom worden covalente obligaties directionele obligaties genoemd?  Aan een waarnemer op een schip op zee welke breedtegraad verschijnt North Star het dichtst bij de horizon?
Aan een waarnemer op een schip op zee welke breedtegraad verschijnt North Star het dichtst bij de horizon?  Veg nudge:een extra vegetarische optie vermindert de vleesconsumptie zonder de verkoop van voedsel te deuken
Veg nudge:een extra vegetarische optie vermindert de vleesconsumptie zonder de verkoop van voedsel te deuken Gematigde Woodland & Shrubland Flowers
Gematigde Woodland & Shrubland Flowers  Kruising met Neanderthalers gaf mensen virusbescherming
Kruising met Neanderthalers gaf mensen virusbescherming  Wetenschappers ontdekken processen om de methaanemissies van dieren te verlagen
Wetenschappers ontdekken processen om de methaanemissies van dieren te verlagen Het bevorderen van fusie-energie door een beter begrip van snelle plasmadeeltjes
Het bevorderen van fusie-energie door een beter begrip van snelle plasmadeeltjes Frustratie inspireert nieuwe vorm van grafeen
Frustratie inspireert nieuwe vorm van grafeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

