
Wetenschap
Designer-enzym overwint sulfietreductie, een knelpunt bij het opruimen van het milieu

hoogleraar scheikunde Yi Lu, links, en afgestudeerde student Evan Mirts hebben een nieuw synthetisch enzym ontworpen dat de verbinding sulfiet tot sulfide reduceert - een notoir complexe meerstaps chemische reactie die scheikundigen jarenlang hebben ontgaan. Krediet:L. Brian Stauffer
Onderzoekers hebben een hindernis genomen voor het opruimen van bepaalde verontreinigingen in het milieu met een nieuw ontworpen synthetisch enzym dat de verbinding sulfiet tot sulfide reduceert - een notoir complexe meerstaps chemische reactie die scheikundigen al jaren ontgaan.
In het journaal Wetenschap , chemici van de Universiteit van Illinois in Urbana-Champaign beschreven hun enzym dat twee verschillende ijzerbevattende centra bevat die met elkaar zijn verbonden door een enkel enzym.
Sulfiet reductie, een veel voorkomende oxidatie-reductie- of redoxreactie kan interfereren met het opruimen van een belangrijke klasse van milieuverontreinigende stoffen, waaronder nitraat, arsenaat en perchloraat. Deze verontreinigingen komen in het milieu terecht als bijproducten van de productie van raketbrandstof, munitie en kunstmest. Sulfiet komt ook van nature voor en verstoort de eliminatie van meer giftige verbindingen, en chemici zijn er niet in geslaagd katalysatoren te maken om sulfiet te verwijderen, omdat het meerdere reactiestappen vereist met behulp van een complexe actieve plaats die moeilijk te ontwerpen en te synthetiseren is.
"Veel biochemische reacties vereisen een reeks enzymen die samenwerken om meerstapsreacties uit te voeren, maar sulfietreductie gebruikt slechts één enzym, sulfietreductase genoemd, dat doet al het werk, " zei Yi Lu, een professor in de chemie in Illinois. "De natuur heeft een zeer complexe enzymstructuur gecreëerd om deze chemische reactie aan te kunnen, en onderzoekers hebben het tot nu toe niet kunnen repliceren."
Eerdere groepen die hebben geprobeerd een synthetisch sulfietreducerend enzym te bouwen, hebben zich geconcentreerd op het maken van structurele modellen die eruitzien als de actieve plaats van inheemse enzymen, zei scheikundestudent Evan Mirts. Voor deze studie is het team gebruikte een enzym als stellage om clusters van ijzer- en zwavelatomen te verankeren die zich gedragen als kleine moleculaire batterijen, het overbrengen van de elektronen die nodig zijn om de redoxreactie te duwen.
"Ik geloof dat we succesvol waren omdat we ons concentreerden op de functionaliteit van ons synthetische enzym, niet de eenvoudigst mogelijke structuur herbouwen, Mirts zei. "We hebben rekening gehouden met interacties die doorgaans als secundair worden beschouwd, of minder belangrijk voor de algehele redoxreactie. Het blijkt dat deze interacties enorm belangrijk zijn."
"Toen we rekening hielden met die zogenaamde zwakkere interacties in ons ontworpen enzym, we zagen plotseling een redoxreactie-activiteit die erg leek op die van het natuurlijk voorkomende sulfietreducerende enzym, " zei Lu, ook een gezamenlijke aangestelde bij het Pacific Northwest National Laboratory van het Amerikaanse ministerie van Energie.
Het team stelt zich voor dat hun nieuw ontwikkelde enzym een nieuwe generatie katalysatoren inspireert om giftig afval in het milieu op te ruimen en de kwaliteit van aardolieproducten te helpen verbeteren.
"Naast de praktische toepassingen, Ik denk dat ons werk hier de grens heeft verlegd van het ontwerp van kunstmatige enzymen in termen van het ontcijferen van de complexiteit van redoxreacties en het ontwerpen van multifactorkatalysatoren met een zeer hoge activiteit, " zei Lu. "Met de succesvolle demonstratie van dit systeem, we kunnen nu beginnen met het ontwerpen van vele andere multicofactor-enzymen die nog complexere, moeilijke reacties waar we vroeger alleen maar van konden dromen."
 Wie is kwetsbaar voor de gevolgen van tropische cyclonen en waarom?
Wie is kwetsbaar voor de gevolgen van tropische cyclonen en waarom? NASA's GPM analyseerde regenval in ex-tropische cycloon 11S
NASA's GPM analyseerde regenval in ex-tropische cycloon 11S Koolstofput in tropische bossen wordt al snel zwakker
Koolstofput in tropische bossen wordt al snel zwakker Hoe een Copperhead Vs. te identificeren een melkslang
Hoe een Copperhead Vs. te identificeren een melkslang  Drie keer grotere reducties in de uitstoot van broeikasgassen in de VS dan eerder gemeld
Drie keer grotere reducties in de uitstoot van broeikasgassen in de VS dan eerder gemeld
Hoofdlijnen
- Wat gebeurt er in de interfase van de celcyclus?
- De natuur laat zien hoe bacteriën lignine afbreken en geeft beter inzicht om biobrandstoffen te maken
- Gemengde organisatie van darmbacteriën wordt onthuld door microbioombeeldvormingstechnologie
- Zou het hebben van een eigen kloon hetzelfde zijn als het hebben van een identieke tweeling?
- Hebben garnalen een zenuwstelsel?
- Door wetenschap ondersteunde manieren om een nieuwe studie te starten
- Wanneer is een mutatie in een DNA-molecuul overgegaan op nakomelingen?
- Maken planten muziek?
- Netwerken gebruiken om weefselspecifieke genregulatie te begrijpen
- Interfacing met de hersenen
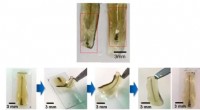
- Onderzoekers synthetiseren nieuwe vloeibare kristallen die gerichte transmissie van elektriciteit mogelijk maken

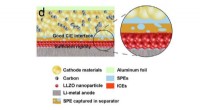
- Onderzoekers ontwerpen dendrietvrije lithiumbatterij
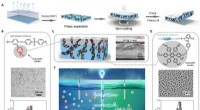
- Een efficiëntere op membraan gebaseerde generator voor het oogsten van osmotisch vermogen (update)
- Onderzoekers vinden een nieuw verband tussen celmetabolisme en celdeling
 Buitenaardse megastructuur niet de oorzaak van dimmen van de meest mysterieuze ster in het universum
Buitenaardse megastructuur niet de oorzaak van dimmen van de meest mysterieuze ster in het universum Olifanten- en koeienmest om duurzaam papier te maken
Olifanten- en koeienmest om duurzaam papier te maken Ounces converteren naar Mililiters
Ounces converteren naar Mililiters Quantum computing:wanneer onwetendheid gewenst is
Quantum computing:wanneer onwetendheid gewenst is Vissers in New England verliezen banen door klimaat:studie
Vissers in New England verliezen banen door klimaat:studie Een nieuw hulpmiddel om fundamentele zaken te onderzoeken
Een nieuw hulpmiddel om fundamentele zaken te onderzoeken Elektriciteit maken uit zout water
Elektriciteit maken uit zout water  What is a Math Compass?
What is a Math Compass?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

