
Wetenschap
Hoe bereiken niet -metalen de edelgasconfiguratie?
* Nobele gasconfiguratie: Nobele gassen zijn extreem stabiel vanwege hun volledige buitenste elektronenschalen. Daarom zijn ze niet -reactief.
* Niet -metalen neiging: Niet -metalen, met hun hoge elektronegativiteit, hebben de neiging elektronen aan te trekken. Dit maakt hen goed in het verkrijgen van elektronen om stabieler te worden.
* anionvorming: Wanneer een niet -metaal elektronen wint, wordt het een negatief geladen ion dat een anion wordt genoemd. Dit negatief geladen ion heeft een volledige buitenste schaal, die lijkt op de configuratie van het dichtstbijzijnde edelgas.
Voorbeelden:
* chloor (CL): Chloor heeft 7 valentie -elektronen. Het krijgt één elektron om de configuratie van argon (AR) te bereiken, die 8 valentie -elektronen heeft. Dit vormt het chloride-ion (Cl-).
* zuurstof (O): Zuurstof heeft 6 valentie -elektronen. Het krijgt twee elektronen om de configuratie van neon (NE) te bereiken, die 8 valentie -elektronen heeft. Dit vormt het oxide-ion (O2-).
Sleutelpunten:
* Niet -metalen vormen typisch ionische bindingen met metalen, waarbij ze elektronen uit het metaal krijgen om de adellijke gasconfiguratie te bereiken.
* Het aantal elektronen dat wordt verkregen door een niet -metaal wordt bepaald door zijn positie op de periodiek systeem en de elektronegativiteit.
* Het bereiken van de adellijke gasconfiguratie is een fundamenteel principe bij het begrijpen van de reactiviteit van niet -metalen.
Laat het me weten als je nog andere vragen hebt!
 Boomresten omzetten in slimme hydrogels
Boomresten omzetten in slimme hydrogels Wat is de chemische samenstelling van aluminiumbrons om een hardheid van 260-270 BHN te verkrijgen?
Wat is de chemische samenstelling van aluminiumbrons om een hardheid van 260-270 BHN te verkrijgen?  Hoe zou je goudstof scheiden van een mengsel van ijzervijlsel en zout?
Hoe zou je goudstof scheiden van een mengsel van ijzervijlsel en zout?  Meteorietinslagen kunnen een onverwachte vorm van silica veroorzaken
Meteorietinslagen kunnen een onverwachte vorm van silica veroorzaken Hoe DNA uit sinaasappels te extraheren
Hoe DNA uit sinaasappels te extraheren
Hoofdlijnen
- Wat betekent het resultaat in de wetenschap?
- Hoe wordt de studie van mensen genoemd?
- Een geprioriteerde lijst van invasieve uitheemse soorten die het milieu van het VK bedreigen
- Wetten van aantrekking:bestuivers gebruiken meerdere signalen om bloemen op verschillende continenten te identificeren
- Uit onderzoek blijkt hoe de adelborstvis zijn urenlange paringsroep volhoudt
- Wat is een geproduceerd aan het einde van de celcyclus?
- Welke soorten organismen bevatten chlorofyl?
- Rewilding van de landbouw kan helpen het milieu te herstellen en de productie van hoogwaardig voedsel te ondersteunen, zeggen onderzoekers
- Hoe bijenkoninginnen de prinsessen beheersen
- Wetenschappers ontwikkelen een innovatieve methode voor het vullen en afdichten van pleuraholtes

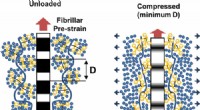
- Collageen in kraakbeenweefsel gedraagt zich als vloeibare kristallen op een smartphonescherm
- Unieke ferro-elektrische microstructuur voor het eerst onthuld

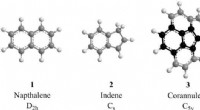
- Interstellaire chemie:vorming van indeen in de gasfase bij lage temperatuur in het interstellaire medium
- Hoe melk een dierlijk lichaam goed doet?

 Is het vriespunt van een mengselwater en zout hoger lager of dezelfde zuiver geen?
Is het vriespunt van een mengselwater en zout hoger lager of dezelfde zuiver geen?  China voltooit de bouw van een faciliteit met een stabiel hoog magnetisch veld
China voltooit de bouw van een faciliteit met een stabiel hoog magnetisch veld Wat gebeurde er vóór de oerknal?
Wat gebeurde er vóór de oerknal? Hoe worden zeldzame en mooie elementen genoemd?
Hoe worden zeldzame en mooie elementen genoemd?  Onderzoekers rapporteren eerste nanogestructureerd materiaal voor brede menging van lichtgolven
Onderzoekers rapporteren eerste nanogestructureerd materiaal voor brede menging van lichtgolven Zijn alle meteoren even groot?
Zijn alle meteoren even groot?  Wat heeft de Hubble -telescoop bijgedragen aan onze kennis van astronomie?
Wat heeft de Hubble -telescoop bijgedragen aan onze kennis van astronomie?  De energiebehoefte voor het depositieproces bedraagt?
De energiebehoefte voor het depositieproces bedraagt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

