
Wetenschap
Wat is de atomaire structuur van chloor?
Basisinformatie
* Atomisch nummer: 17 (dit betekent dat er 17 protonen in de kern zijn)
* Atomisch symbool: Klet
* Atomische massa: 35,45 U (dit is de gemiddelde massa van alle chloorisotopen)
structuur
* Nucleus:
* protonen: 17 (positief geladen)
* neutronen: 18 (geen lading) - Dit is de meest voorkomende isotoop van chloor. Er zijn andere isotopen met verschillende aantallen neutronen.
* elektronenschalen:
* 1e shell (k shell): 2 elektronen
* 2e shell (l shell): 8 elektronen
* 3e shell (m shell): 7 elektronen
Key Functies
* valentie -elektronen: De 7 elektronen in de buitenste schaal (m schaal) worden valentie -elektronen genoemd. Dit zijn de elektronen die betrokken zijn bij chemische binding.
* halogeen: Chloor is een halogeen, een groep zeer reactieve niet -metalen die gemakkelijk negatieve ionen (anionen) vormen door één elektron te winnen.
Waarom deze structuur ertoe doet
* Reactiviteit: De aanwezigheid van 7 valentie -elektronen maakt chloor zeer reactief, omdat het nog een elektron wil krijgen om zijn buitenste schaal te voltooien en een stabiele elektronenconfiguratie te bereiken zoals de edelgassen.
* binding: Deze reactiviteit verklaart waarom chloor sterke bindingen vormt met andere elementen, zoals in tabelzout (NaCl). Het krijgt een elektron van natrium en vormt een negatief chloride-ion (Cl-), terwijl natrium een elektron verliest om een positief natriumion te worden (Na+).
Laat het me weten als u meer details wilt over specifieke aspecten van de structuur, zoals elektronenconfiguratie of isotoopinformatie.
 Onderzoekers ontwikkelen brandvertragende coating met hernieuwbare materialen
Onderzoekers ontwikkelen brandvertragende coating met hernieuwbare materialen Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur
Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur Hoe verschillen isotopen van An van elkaar?
Hoe verschillen isotopen van An van elkaar?  Wat zijn enkele eigenschappen die u kunt identificeren door het smelt- en kookpunt van chemisch te kennen?
Wat zijn enkele eigenschappen die u kunt identificeren door het smelt- en kookpunt van chemisch te kennen?  Wat is de functie van vloeibaar wasmiddel bij DNA-isolatie?
Wat is de functie van vloeibaar wasmiddel bij DNA-isolatie?
 Valt zure regen altijd over het gebied dat fases produceerde of kan het op een afstand verderop?
Valt zure regen altijd over het gebied dat fases produceerde of kan het op een afstand verderop?  Orkaan Ida treft Louisiana als storm van categorie 4
Orkaan Ida treft Louisiana als storm van categorie 4 Een stijging van 50% van het kooldioxidegehalte zou de regenval in de Amazone meer kunnen verminderen dan ontbossing
Een stijging van 50% van het kooldioxidegehalte zou de regenval in de Amazone meer kunnen verminderen dan ontbossing Dieren zien de wereld in andere kleuren dan mensen:een nieuwe camera laat zien hoe dit eruit ziet
Dieren zien de wereld in andere kleuren dan mensen:een nieuwe camera laat zien hoe dit eruit ziet  De koudegolf in de VS was een speling van de natuur, snelle analyse vindt
De koudegolf in de VS was een speling van de natuur, snelle analyse vindt
Hoofdlijnen
- Wat is de belangrijkste rol van het mannelijke reproductieve systeem van de accessoire klieren?
- Vissenseks zo luid dat dolfijnen doof kunnen worden
- Welk orgaansysteem is het externe lichaamsbelasting?
- Welk klein deel van een zaad dat in een nieuwe plant groeit?
- Wat betekent het woord gezin in de wetenschap?
- Hoe zal klimaatverandering het geografische bereik van salamandersoorten in de VS en Canada beïnvloeden?
- Waarom het leren van dierengeluiden cruciaal kan zijn voor de taalontwikkeling van kinderen
- Hoe DNA gekoppeld aan de rol van ribosomen in een cel?
- Genoomsequencing laat zien hoe salmonella een niche verovert in de varkensvleesproductie
- Hoe drie mutaties samenwerken om nieuwe SARS-CoV-2-varianten te stimuleren
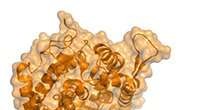
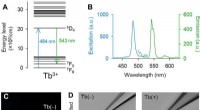
- Met terbium (III) gedoteerd fluorescerend glas voor biomedisch onderzoek
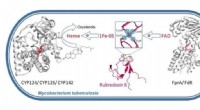
- Nieuwe studie verklaart Mycobacterium tuberculosis hoge weerstand tegen medicijnen en immuniteit
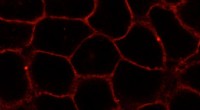
- Hoe wetenschappers celmembranen analyseren
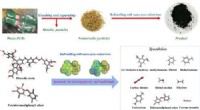
- Naar een veiligere verwijdering van printplaten
 IJskernen suggereren dat pandemieën uit de 16e eeuw mogelijk een daling van de CO₂-uitstoot in de atmosfeer hebben veroorzaakt
IJskernen suggereren dat pandemieën uit de 16e eeuw mogelijk een daling van de CO₂-uitstoot in de atmosfeer hebben veroorzaakt  Biologen ontdekken hoe planten stamcellen reconstrueren
Biologen ontdekken hoe planten stamcellen reconstrueren  Studie:Sociale netwerken kunnen de perceptie van het risico op klimaatverandering beïnvloeden
Studie:Sociale netwerken kunnen de perceptie van het risico op klimaatverandering beïnvloeden  Wat zijn de voorbeelden van elektromagnetische energie?
Wat zijn de voorbeelden van elektromagnetische energie?  De economische activiteit is gehalveerd tijdens de coronacrisis in Spanje, studie suggereert:
De economische activiteit is gehalveerd tijdens de coronacrisis in Spanje, studie suggereert: De ene ramp na de andere:waarom we iets moeten doen aan de redenen waarom sommige gemeenschappen grotere risico's lopen
De ene ramp na de andere:waarom we iets moeten doen aan de redenen waarom sommige gemeenschappen grotere risico's lopen Wat is een fatale genetische aandoening waarin metabole afvalstoffen het lichaam opbouwen?
Wat is een fatale genetische aandoening waarin metabole afvalstoffen het lichaam opbouwen?  Fotonische kristallen onthullen hun interne kenmerken met nieuwe methode
Fotonische kristallen onthullen hun interne kenmerken met nieuwe methode
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

