
Wetenschap
Wat zijn enkele eigenschappen die u kunt identificeren door het smelt- en kookpunt van chemisch te kennen?
1. Intermoleculaire krachten:
* Hoge smelt-/kookpunten: Suggereren sterke intermoleculaire krachten (IMF) zoals waterstofbinding, dipool-dipoolinteracties of dispersiekrachten in Londen. Sterker IMF vereist meer energie om te overwinnen, wat leidt tot hogere smelt- en kookpunten.
* Lage smelt-/kookpunten: Geef een zwak IMF aan. Stoffen met alleen London Dispersion -troepen hebben meestal lage smelt- en kookpunten.
2. Moleculaire structuur:
* vertakking: Vertakte moleculen hebben zwakkere dispersiekrachten in Londen dan lineaire moleculen van vergelijkbaar molecuulgewicht. Dit betekent dat vertakte moleculen lagere smelt- en kookpunten hebben.
* polariteit: Polaire moleculen hebben sterkere dipool-dipool interacties dan niet-polaire moleculen. Dit resulteert in hogere smelt- en kookpunten voor polaire verbindingen.
* Molecuulgewicht: Zwaardere moleculen hebben sterkere dispersietroepen in Londen. Daarom komt in het algemeen een hoger molecuulgewicht overeen met hogere smelt- en kookpunten.
3. Fysieke toestand bij kamertemperatuur:
* solide: Als het smeltpunt boven kamertemperatuur ligt, is de stof vast bij kamertemperatuur.
* vloeistof: Als het smeltpunt onder kamertemperatuur is en het kookpunt boven kamertemperatuur ligt, is de stof vloeibaar bij kamertemperatuur.
* gas: Als zowel de smelten- als de kookpunten onder kamertemperatuur zijn, is de stof een gas bij kamertemperatuur.
4. Zuiverheid:
* scherp smeltpunt: Een scherp, goed gedefinieerd smeltpunt duidt op een pure stof.
* breed smeltbereik: Een breed smeltbereik suggereert dat onzuiverheden aanwezig zijn.
5. Volatiliteit:
* Laag kookpunt: Stoffen met lage kookpunten zijn vluchtig, wat betekent dat ze gemakkelijk verdampen.
* Hoog kookpunt: Stoffen met hoge kookpunten zijn minder vluchtig.
6. Compatibiliteit:
* Vergelijkbare kookpunten: Chemicaliën met vergelijkbare kookpunten zijn eerder compatibel en kunnen samen worden gebruikt in mengsels of reacties.
Belangrijke opmerking:
Hoewel deze eigenschappen kunnen worden afgeleid uit smelten- en kookpunten, is het essentieel om te onthouden dat dit slechts generalisaties zijn. Er zijn altijd uitzonderingen en andere factoren (zoals druk en externe omstandigheden) kunnen deze eigenschappen beïnvloeden.
 Onderzoekers passen de katalysator van de hoofdgroep aan met atomair gedispergeerde in-sites voor zeer efficiënte oxidatieve dehydrogenering
Onderzoekers passen de katalysator van de hoofdgroep aan met atomair gedispergeerde in-sites voor zeer efficiënte oxidatieve dehydrogenering Hoe beïnvloedt pH-niveau enzymactiviteit?
Hoe beïnvloedt pH-niveau enzymactiviteit?  Hoe kun je een wetenschap maken op kleine alchemie?
Hoe kun je een wetenschap maken op kleine alchemie?  Kun je een doel geven voor het bakken van frisdrank vulkaan?
Kun je een doel geven voor het bakken van frisdrank vulkaan?  Wat beschrijft een isotoop het beste?
Wat beschrijft een isotoop het beste?
Hoofdlijnen
- Kunnen dierencellen hun eigen cellen maken?
- Wat is de ultieme oorzaak van allelen?
- Insecten eten:zoals roerbakken of curry?
- Onderzoek identificeert een nieuw mechanisme dat betrokken is bij de voortplantingsfunctie
- Wat is aegyptopithecus?
- Onder welke tak van de wetenschap zou je anatomie classificeren?
- Welke circulatie heeft Agnatha?
- Wereldprimeur gebruikt satellieten en oceaanmodellen om de biodiversiteit op de Antarctische zeebodem te verklaren
- Biomoleculaire condensaten:onderzoek onthult een slechte voorspellende kracht van gevestigde vloeistof-vloeistoffasescheidingstesten
- Complexe moleculen aan het werk zien
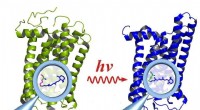
- Onderzoekers ontwikkelen biohernieuwbare, biologisch afbreekbare kunststoffen

- Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
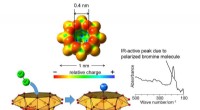
- Nieuwe stikstof-assemblage koolstofkatalysator heeft potentieel om chemische productie te transformeren

- Hoe antilichamen te gebruiken om chemische reacties onder controle te houden?
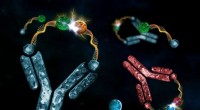
 Betrokkenheid bij het gezin en school heeft specifieke voordelen voor jonge leerlingen
Betrokkenheid bij het gezin en school heeft specifieke voordelen voor jonge leerlingen Nieuwe polymeer mesofasestructuur ontdekt
Nieuwe polymeer mesofasestructuur ontdekt De pandemie in het VK heeft minderheden gehamerd, zelfstandige:studie
De pandemie in het VK heeft minderheden gehamerd, zelfstandige:studie Hoe beïnvloedt het plastic vissen?
Hoe beïnvloedt het plastic vissen?  Thermochemische nanolithografie maakt nu meerdere chemicaliën op een chip mogelijk
Thermochemische nanolithografie maakt nu meerdere chemicaliën op een chip mogelijk Wat is het begin van een maancyclus?
Wat is het begin van een maancyclus?  Hoe te converteren van BTU naar Fahrenheit
Hoe te converteren van BTU naar Fahrenheit  Wat absorbeert gammastraling?
Wat absorbeert gammastraling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

