
Wetenschap
Waarom wordt de reactie beperkt door een hoeveelheid van één stof?
Het concept van beperkende reactanten
* Niet alle reactanten zijn gelijk gemaakt: In een chemische reactie combineren reactanten in specifieke verhoudingen op basis van hun stoichiometrie (de coëfficiënten in de gebalanceerde chemische vergelijking).
* Eén reactant loopt eerst op: Wanneer een reactant volledig wordt geconsumeerd, stopt de reactie, zelfs als andere reactanten nog steeds aanwezig zijn. Deze reactant is de beperkende reactant.
* de "limiter": De beperkende reactant beperkt de hoeveelheid product die kan worden gevormd, omdat het bepaalt hoeveel van de andere reactanten daadwerkelijk kunnen worden gebruikt.
Voorbeeld:
Stel je voor dat je broodjes maakt met 4 plakjes brood en 3 plakjes kaas. Elke sandwich heeft 2 plakjes brood en 1 plakje kaas nodig.
* Je hebt genoeg brood om 2 broodjes te maken (4 plakjes / 2 plakjes per sandwich =2 sandwiches).
* je hebt genoeg kaas om 3 sandwiches te maken (3 plakjes / 1 plak per sandwich =3 sandwiches).
De beperkende reactant is het brood Omdat je maar 2 broodjes kunt maken voordat je geen brood meer hebt, ook al heb je genoeg kaas om 3 te maken.
gevolgen van het beperken van reactanten
* Maximale productopbrengst: De hoeveelheid gevormde product is recht evenredig met de hoeveelheid beperkende reactant die wordt gebruikt.
* overtollige reactanten: De reactant die niet volledig wordt geconsumeerd, wordt de overtollige reactant genoemd. Een deel ervan blijft nadat de reactie is voltooid.
het bepalen van de beperkende reactant
Om de beperkende reactant te vinden, moet u:
1. Breng de chemische vergelijking in evenwicht: Dit geeft u de stoichiometrische verhoudingen.
2. Converteer gegeven hoeveelheden reactanten in mollen: Gebruik de molaire massa's van de reactanten.
3. Vergelijk de molverhoudingen met de stoichiometrische verhoudingen: De reactant met de kleinste molverhouding (vergeleken met zijn coëfficiënt in de evenwichtige vergelijking) is de beperkende reactant.
Samenvattend: De beperkende reactant is de stof die de maximale hoeveelheid product bepaalt die kan worden gevormd in een chemische reactie. Inzicht in het concept van beperkende reactanten is cruciaal voor het optimaliseren van chemische reacties en het voorspellen van hun resultaten.
 Fout gevonden in waterbehandelingsmethode:het proces kan onbewust schadelijke chemicaliën genereren
Fout gevonden in waterbehandelingsmethode:het proces kan onbewust schadelijke chemicaliën genereren Wat is het verschil tussen ionische en covalente bindingen?
Wat is het verschil tussen ionische en covalente bindingen?  Hoe een hygrometer te bouwen
Hoe een hygrometer te bouwen Beeldvorming met superresolutie onthult het mechanisme van GLUT1-clustering
Beeldvorming met superresolutie onthult het mechanisme van GLUT1-clustering Wat zijn de twee klassen van Phylum Anthophyta?
Wat zijn de twee klassen van Phylum Anthophyta?
 Australië keurt nieuw steenkoolproject goed naarmate klimaatwaarschuwingen toenemen
Australië keurt nieuw steenkoolproject goed naarmate klimaatwaarschuwingen toenemen Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien
Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien De rol van tijgers in het ecosysteem
De rol van tijgers in het ecosysteem Hydrologie data tool helpt gebruikers bij het beheren van waterbronnen, infrastructuur beschermen
Hydrologie data tool helpt gebruikers bij het beheren van waterbronnen, infrastructuur beschermen Detectivemissie om de geschiedenis van een nieuwe Afrikaanse meteoriet te karakteriseren en te traceren
Detectivemissie om de geschiedenis van een nieuwe Afrikaanse meteoriet te karakteriseren en te traceren
Hoofdlijnen
- Bepalen genen al uw geërfde eigenschappen?
- Studie wakkert de discussie aan over waarom vrouwtjesvogels extra partners zoeken
- Welke delen van de cel zijn betrokken bij cellulaire ademhaling?
- Wat is de naam voor iets doorgegeven aan een organisme van zijn ouders?
- Van koralen tot gewassen:hoe het leven de plannen voor zijn cellulaire energiecentrales beschermt
- Hoe evolutie werkt
- Exotische dieren en de jacht op goud
- Wat is een tweede neef? Het ontrafelen van de stamboom
- Nectarivoren:een wereld van zoetekauwen
- Kleverige situatie:nieuw proces verandert houtsnippers in tape

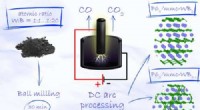
- Superharde materiaalsynthese goedkoper gemaakt
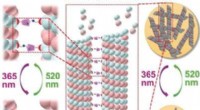
- Lichtgecontroleerde omkeerbare aggregatie van microtubuli gemedieerd door paclitaxel-gemodificeerd cyclodextrine
- Onderzoekers ontwikkelen snellere test voor cannabiskwaliteit

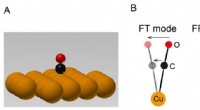
- Opheldering van trillingsenergie van een enkel molecuul in een extern krachtveld
 Wat zijn de bekwaamheden van tien?
Wat zijn de bekwaamheden van tien?  Nieuw nanobiomateriaal van de zijde van een mijt met veelbelovende biomedische eigenschappen
Nieuw nanobiomateriaal van de zijde van een mijt met veelbelovende biomedische eigenschappen Ruimtetoerisme:nieuwe testvlucht gepland voor Virgin Galactic
Ruimtetoerisme:nieuwe testvlucht gepland voor Virgin Galactic De wet laat slachtoffers van financieel misbruik door hun partner in de steek, waarschuwt onderzoek
De wet laat slachtoffers van financieel misbruik door hun partner in de steek, waarschuwt onderzoek  Coronavirus:waarom het VK een basisinkomen nodig heeft voor alle werknemers
Coronavirus:waarom het VK een basisinkomen nodig heeft voor alle werknemers Wat heeft de pH-waarde van 13?
Wat heeft de pH-waarde van 13?  Als het gaat om gow is de aarde gevormd welke verklaring volgt de atmosfeer voornamelijk waterstof en helium?
Als het gaat om gow is de aarde gevormd welke verklaring volgt de atmosfeer voornamelijk waterstof en helium?  Klimaatverandering zal waarschijnlijk de vliegtuigturbulentie verhogen
Klimaatverandering zal waarschijnlijk de vliegtuigturbulentie verhogen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

