
Wetenschap
Lichtgecontroleerde omkeerbare aggregatie van microtubuli gemedieerd door paclitaxel-gemodificeerd cyclodextrine
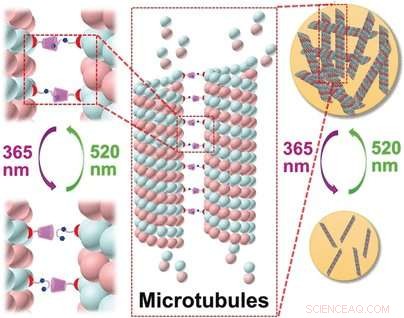
Krediet:Wiley
Een combinatie van natuurlijke microtubuli en synthetische macrocyclische receptoren zorgt voor lichtgecontroleerde, omkeerbare aggregatie van de microtubuli tot grotere nanostructuren. Zoals Chinese wetenschappers hebben gerapporteerd in het tijdschrift Angewandte Chemie , wanneer in een cellulaire omgeving deze geaggregeerde microtubuli ook de celmorfologie kunnen veranderen, celdood veroorzaken. De onderzoekers hopen meer te weten te komen over ziekten die worden veroorzaakt door een onjuiste aggregatie van eiwitten.
In de natuur, de aggregatie van moleculen tot superstructuren speelt een belangrijke rol. Dynamische microtubuli zijn eiwitfilamenten die samen met andere componenten de cytoskeletten van onze cellen vormen. Tijdens de celcyclus, microtubuli worden constant geassembleerd en gedemonteerd. Wetenschappers van de Nankai University en het Collaborative Innovation Centre of Chemical Science and Engineering (Tianjin, China) bedacht het idee om microtubuli te combineren tot grotere supramoleculaire aggregaten met behulp van synthetische 'receptoren'. Op deze manier hoopten ze innovatieve biomaterialen te produceren en nieuwe kennis op te doen over biologische aggregatieprocessen.
Om de synthetische receptoren aan de microtubuli te hechten, het team dat met Yu Liu werkte, koos voor een kankermedicijn genaamd paclitaxel. Dit molecuul bindt aan microtubuli en blokkeert de deconstructie van het cytoskelet, celdeling stoppen en celdood veroorzaken. Als receptor, de onderzoekers kozen een groot komvormig molecuul uit de cyclodextrinefamilie. Deze macrocyclische moleculen kunnen andere moleculen als "gasten" in hun grote holtes opnemen. In dit geval is de gast een arylazopyrazol (AAP), een molecuul met twee aromatische ringen overbrugd door een stikstof-stikstof dubbele binding. Het molecuul kan twee vormen aannemen:een gebogen cis-vorm en een rechte trans-vorm. Alleen de rechte versie past in de "beker" van cyclodextrine. De slimme truc hier is dat, door licht van twee verschillende golflengten te gebruiken, de AAP kan naar believen heen en weer worden geschakeld tussen zijn twee vormen.
De onderzoekers gebruikten paclitaxel als connector om "cups" en hun "gasten" aan microtubuli te bevestigen. Bestraling met zichtbaar en UV-licht schakelt de microtubuli tussen een geaggregeerde en niet-geaggregeerde vorm, respectievelijk, zoals aangetoond door spectroscopisch en microscopisch onderzoek. De aggregaten nemen een breed scala aan morfologische variaties aan, variërend van nanovezels tot nanolinten en nanodeeltjes van verschillende groottes.
Het is bijzonder interessant dat de aggregatie van de microtubuli ook in cellen kan worden geactiveerd. Dit zorgt ervoor dat de cellen krimpen en afsterven, wat aantoont dat het cytotoxische effect van paclitaxel aanzienlijk kan worden verhoogd.
De onderzoekers hopen dat hun aanpak ons begrip zal vergroten van de processen die betrokken zijn bij fysiologische en pathologische eiwit-nanoassemblage, en zou nieuwe perspectieven kunnen creëren bij de behandeling van ziekten die worden veroorzaakt door de onjuiste aggregatie van eiwitten.
 Ingenieurs bedenken nieuwe methode om schadelijke E. coli uit water te verwijderen
Ingenieurs bedenken nieuwe methode om schadelijke E. coli uit water te verwijderen Onderzoeksteam pioniert sneller, goedkopere en groenere manier om aminozuren te produceren uit plantaardig afval
Onderzoeksteam pioniert sneller, goedkopere en groenere manier om aminozuren te produceren uit plantaardig afval Methoden voor het ontgassen van buffers
Methoden voor het ontgassen van buffers Transparant keramisch pantser biedt superieure ballistische bescherming ten opzichte van traditionele glaslaminaten
Transparant keramisch pantser biedt superieure ballistische bescherming ten opzichte van traditionele glaslaminaten Een nieuwe methode voor proximity-labeling op nanometerschaal die zich richt op histidine-residuen
Een nieuwe methode voor proximity-labeling op nanometerschaal die zich richt op histidine-residuen
 Extreem weer wordt steeds extremer
Extreem weer wordt steeds extremer Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten
Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten Natuurkundigen tonen aan dat interacties tussen rook en wolken een onverwacht verkoelend effect hebben
Natuurkundigen tonen aan dat interacties tussen rook en wolken een onverwacht verkoelend effect hebben Fosfortekort kan regionale voedselvoorzieningsketens verstoren
Fosfortekort kan regionale voedselvoorzieningsketens verstoren Duurzaamheid beoefenen tijdens een pandemie
Duurzaamheid beoefenen tijdens een pandemie
Hoofdlijnen
- Verrassend snelle evolutie waargenomen bij hagedissoorten
- Is maretak meer dan alleen een excuus voor een kus?
- Hoe ribosomen het proteoom vormen
- Wilt u 41 procent van de zeer bedreigde gewervelde planeten redden? Werken op eilanden
- Geen hondenleven voor oudere dieren in Singapore Zoo
- Prehistorische skeletten van vrouwen tonen impact van rigoureuze handenarbeid
- Daar is een studie over:het stenen tijdperk had net zoveel linkse mensen
- Hoe succesvol te zijn in Microbiology
- Blade runner benen geven verminkte Thaise hond nieuw leven
- Een groene benadering van het maken van ammoniak kan de wereld helpen voeden

- Wetenschap onthult geheimen van een mummieportret

- Nieuwe sensortechnologie maakt supergevoelige live monitoring van menselijke biomoleculen mogelijk

- Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen

- Metalen nanokatalysatoren imiteren de structuur van enzymen

 Jongens, vaders en mentoren werken samen voor STEM-betrokkenheid
Jongens, vaders en mentoren werken samen voor STEM-betrokkenheid Onderzoek toont aan dat online stemmen transformerend kan zijn voor inheemse gemeenschappen
Onderzoek toont aan dat online stemmen transformerend kan zijn voor inheemse gemeenschappen Hoe de dichtheid van een persoon te meten
Hoe de dichtheid van een persoon te meten Nieuwe technologie maakt internetmemes toegankelijk voor mensen met een visuele beperking
Nieuwe technologie maakt internetmemes toegankelijk voor mensen met een visuele beperking Wetenschappers ontwikkelen topologische defectdetectiemethode
Wetenschappers ontwikkelen topologische defectdetectiemethode Zou zilte landbouw de toekomst van kustlandbouw kunnen zijn?
Zou zilte landbouw de toekomst van kustlandbouw kunnen zijn? Chemie:toegang tot verboden ringen
Chemie:toegang tot verboden ringen Wetenschap zegt:waarom sommige vliegtuigen niet bij hoge temperaturen vliegen
Wetenschap zegt:waarom sommige vliegtuigen niet bij hoge temperaturen vliegen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

