
Wetenschap
Wat is de valentie van fluor?
Fluor heeft een valentie van 1 .
Dit is waarom:
* Elektronische configuratie: Fluor heeft 7 elektronen in zijn buitenste schaal (2S² 2P⁵). Het heeft nog een elektron nodig om een stabiele octetconfiguratie te bereiken, zoals de Noble Gas Neon.
* Elektronen verkrijgen: Fluor bereikt deze stabiliteit door één elektron te verkrijgen en een fluoride -ion te vormen (F⁻). Deze winst van één elektron maakt zijn valentie 1.
 NASA volgt hittegolf boven het zuidwesten van de VS
NASA volgt hittegolf boven het zuidwesten van de VS Bomen spelen een belangrijke rol bij het voorkomen van de opwarming van de aarde door kooldioxide te absorberen en water in de atmosfeer te pompen?
Bomen spelen een belangrijke rol bij het voorkomen van de opwarming van de aarde door kooldioxide te absorberen en water in de atmosfeer te pompen?  Hoe noem je elementen die niet op natuurlijke wijze bestaan?
Hoe noem je elementen die niet op natuurlijke wijze bestaan?  Meer dan 1 miljoen barrières op Europese rivieren:studie
Meer dan 1 miljoen barrières op Europese rivieren:studie Model:Hoe ziet het toegenomen gebruik van houtachtige biomassa eruit voor het mondiale bosecosysteem
Model:Hoe ziet het toegenomen gebruik van houtachtige biomassa eruit voor het mondiale bosecosysteem
Hoofdlijnen
- Elk organisme dat zijn eigen voedsel maakt door fotosynthese is?
- Waarom het zo goed voelt om bang te zijn
- Wat zijn de functies van een levercel?
- Wat is de rol van water voor levende organismen?
- Commerciële voorouderstests kunnen onthullen hoeveel Neanderthaler-DNA u heeft
- Waarom kunnen slangen niet knipperen?
- Stijgende temperaturen veranderen grote populatie zeeschildpadden vrouw
- Waar staat NUC voor in een cel?
- Microbiële verstekelingen:verspreiden schepen ziekten?
- Geavanceerde microscopie onthult ongebruikelijke DNA-structuur

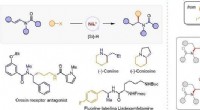
- Chirale amines gesynthetiseerd door nikkel-gekatalyseerde asymmetrische reductieve hydroalkylering
- Potentieel van polymeervermogen
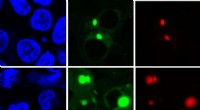
- Nieuwe methode gebruikt fluorescentie om ziekteverwekkende vormen van eiwitten te identificeren
- Chemie:toegang tot verboden ringen
 Wat is de naam die wordt gebruikt om donkere bands te beschrijven die Jupiter omringt?
Wat is de naam die wordt gebruikt om donkere bands te beschrijven die Jupiter omringt?  Chemici ontwikkelen methode om katalysator-, oppervlakteactieve en sjabloonvrije polymere nanodeeltjes
Chemici ontwikkelen methode om katalysator-, oppervlakteactieve en sjabloonvrije polymere nanodeeltjes Aardverschuiving Myanmar doodt 34, veel meer gevreesd vermist
Aardverschuiving Myanmar doodt 34, veel meer gevreesd vermist Amerikaanse klimaatsceptici doen rillingen over de Arctische samenwerking
Amerikaanse klimaatsceptici doen rillingen over de Arctische samenwerking Chemicus creëert nieuwe katalysatoren voor klikreacties
Chemicus creëert nieuwe katalysatoren voor klikreacties De koopkracht van de consument is diverser dan ooit
De koopkracht van de consument is diverser dan ooit Wanneer zendt de aarde aardstraling uit?
Wanneer zendt de aarde aardstraling uit?  Hoe gebruikt elektromagnetische energieverbruik op het gebied van geneeskunde?
Hoe gebruikt elektromagnetische energieverbruik op het gebied van geneeskunde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

