
Wetenschap
Wat is een volume bezet door 0,02 mol chloorgas?
1. Ideale gaswet:
De ideale gaswet relateert druk (P), volume (V), aantal mol (N) en temperatuur (T):
PV =NRT
Waar:
* R is de ideale gasconstante (0,0821 L · atm/mol · k)
2. Veronderstellingen:
* We moeten standaard temperatuur en druk (STP) aannemen om dit probleem op te lossen. STP wordt gedefinieerd als 0 ° C (273,15 K) en 1 atm druk.
3. Herschik de vergelijking:
Los de ideale gaswet op voor volume:
V =nrt / p
4. Sluit de waarden aan:
* n =0,02 mol
* R =0,0821 l · atm/mol · k
* T =273.15 K
* P =1 ATM
5. Berekenen:
V =(0,02 mol * 0,0821 l · atm / mol · k * 273.15 k) / 1 atm
V ≈ 0,448 l
Daarom wordt ongeveer 0,448 liter volume bezet door 0,02 mol chloorgas bij STP.
 Waarom verandert kopersulfaat massa wanneer verwarmd?
Waarom verandert kopersulfaat massa wanneer verwarmd?  Wanneer er een overdracht van elektronen van het ene atoom naar het andere plaatsvindt en er een sterke aantrekkingskracht is op tegengesteld geladen atomen, welk type binding ontstaat er dan?
Wanneer er een overdracht van elektronen van het ene atoom naar het andere plaatsvindt en er een sterke aantrekkingskracht is op tegengesteld geladen atomen, welk type binding ontstaat er dan?  In welke vorm wordt ijzer aangetroffen?
In welke vorm wordt ijzer aangetroffen?  Gebruiken fotosynthetische complexen kwantumcoherentie om hun efficiëntie te vergroten?
Gebruiken fotosynthetische complexen kwantumcoherentie om hun efficiëntie te vergroten?  Vitamine B7-bewakingsapparaat voor analyse van voedsel en klinische monsters
Vitamine B7-bewakingsapparaat voor analyse van voedsel en klinische monsters
 Hoe wordt zuurstof uit onze waterwegen 'gezogen'?
Hoe wordt zuurstof uit onze waterwegen 'gezogen'?  Een mogelijke verklaring waarom West-Antarctica sneller opwarmt dan Oost-Antarctica
Een mogelijke verklaring waarom West-Antarctica sneller opwarmt dan Oost-Antarctica Gesprekken om een rommelig juridisch gevecht over de emissieregels van Californië te voorkomen, lijken vastgelopen
Gesprekken om een rommelig juridisch gevecht over de emissieregels van Californië te voorkomen, lijken vastgelopen De meeste voedseluitgaven ondersteunen de verwerking, geen boeren:studeren
De meeste voedseluitgaven ondersteunen de verwerking, geen boeren:studeren Wetenschappers krijgen als eerste inzicht in oorzaak van aardbevingen in slow motion
Wetenschappers krijgen als eerste inzicht in oorzaak van aardbevingen in slow motion
Hoofdlijnen
- Genomen van wilde tomaten bieden waardevolle hulpbron voor tomatenverbetering
- Wat voor soort chemische stof geeft een zigeunermot vrij om vrienden aan te trekken?
- Wat is een Dekadollar?
- Wat is een voorbeeld van culturele evolutie?
- Heeft een botcel organellen?
- Wat zijn enkele fysieke aanpassingen voor een kraai?
- Waarom gebruikte Hooky de term cellen?
- Mondbacteriën 'battle royale' helpen verklaren hoe een ziekteverwekker ziekenhuisinfecties veroorzaakt
- Hoe hiv bevestigd met gastheercel?
- Computermodel voor het ontwerpen van eiwitsequenties die zijn geoptimaliseerd om te binden aan medicijndoelen

- Onderzoekers demonstreren een fundamenteel nieuwe benadering van echografie

- Upcycling van fast fashion om afval en vervuiling te verminderen

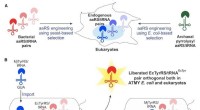
- Gemanipuleerde genetische machinerie afgeleid van E. coli levert nieuwe aminozuren aan eiwitten
- Kalkoenborst met een lager natriumgehalte wint sensorische test dan volzoutoptie

 Onderzoekers produceren 's werelds eerste programmeerbare nanoprocessor
Onderzoekers produceren 's werelds eerste programmeerbare nanoprocessor Luchtvervuilingsniveaus zijn afhankelijk van motregen
Luchtvervuilingsniveaus zijn afhankelijk van motregen Wat is de woordvergelijking voor reactiekalksteen, voornamelijk calciumcarbonaat, wanneer het reageert met verdund zoutzuur?
Wat is de woordvergelijking voor reactiekalksteen, voornamelijk calciumcarbonaat, wanneer het reageert met verdund zoutzuur?  Waltzing-nanodeeltjes kunnen het zoeken naar betere methoden voor medicijnafgifte bevorderen
Waltzing-nanodeeltjes kunnen het zoeken naar betere methoden voor medicijnafgifte bevorderen Wat is landbrezze?
Wat is landbrezze?  Wie was de eerste moderne astronoom die een op de zon gecentreerd zonnestelsel concentreerde?
Wie was de eerste moderne astronoom die een op de zon gecentreerd zonnestelsel concentreerde?  Wat is de beste streamingdienst voor jou? Hoe kabelalternatieven zich verhouden voor snoersnijders
Wat is de beste streamingdienst voor jou? Hoe kabelalternatieven zich verhouden voor snoersnijders Experts verklaren het effect van klimaatverandering op infrastructuur
Experts verklaren het effect van klimaatverandering op infrastructuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

