
Wetenschap
Wat is het oxidatienummer voor stikstof?
Algemene regels:
* gratis element: Het oxidatienummer van een element in zijn elementaire vorm is altijd 0. Dus, n₂ (stikstofgas) heeft een oxidatienummer van 0.
* Monatomische ionen: Het oxidatienummer van een monatomisch ion is gelijk aan de lading. N³⁻ (nitride -ion) heeft bijvoorbeeld een oxidatienummer van -3.
* zuurstof: Zuurstof heeft meestal een oxidatienummer van -2, behalve in peroxiden (zoals H₂o₂) waar het -1 is.
* waterstof: Waterstof heeft meestal een oxidatienummer van +1, behalve in metaalhydriden (zoals NAH) waar het -1 is.
* som van oxidatienummers: De som van de oxidatienummers in een neutrale verbinding moet nul gelijk zijn, en in een polyatomisch ion moet het gelijk zijn aan de lading van het ion.
Voorbeelden:
* NH₃ (ammoniak): H is +1, dus 3 H -atomen dragen +3 bij. Om in evenwicht te zijn, moet n -3 zijn.
* hno₃ (salpeterzuur): O is -2, dus 3 O -atomen dragen bij -6 bij. H is +1. Om in evenwicht te zijn, moet N +5 zijn.
* n₂o (stikstofoxide): O is -2. Om in evenwicht te zijn, moet elke n +1 zijn.
* no₂ (stikstofdioxide): O is -2, dus 2 O -atomen dragen -4 bij. Om in evenwicht te zijn, moet N +4 zijn.
belangrijke opmerkingen:
* Oxidatienummers worden toegewezen, niet gemeten: Ze zijn een manier om elektronenoverdracht bij te houden in reacties.
* Het oxidatienummer kan fractioneel zijn: In sommige gevallen, zoals in N₂o, is het oxidatienummer voor stikstof niet een heel getal.
Laat het me weten als je een specifiek stikstofbevattend molecuul in gedachten hebt en ik kan je helpen het oxidatienummer te bepalen.
 Bij EPA, coronavirus verstoort onderzoek en roept vragen op over impact op luchtkwaliteit
Bij EPA, coronavirus verstoort onderzoek en roept vragen op over impact op luchtkwaliteit Grote westerse merken vervuilen oceanen met goedkoop plastic in Filipijnen:rapport
Grote westerse merken vervuilen oceanen met goedkoop plastic in Filipijnen:rapport Frequentie van gecombineerde droogtes en hittegolven is de afgelopen 50 jaar aanzienlijk toegenomen in het westen van de VS
Frequentie van gecombineerde droogtes en hittegolven is de afgelopen 50 jaar aanzienlijk toegenomen in het westen van de VS Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden
Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden Planten die in grotten wonen
Planten die in grotten wonen
Hoofdlijnen
- 'Vliegende vaccinator':kunnen genetisch gemanipuleerde muggen een nieuwe strategie tegen malaria bieden?
- Welk vierkant is groter? Honingbijen zien visuele illusies zoals mensen dat doen
- Wanneer is het Golgi -apparaat ontdekt?
- Gregor Mendel - Vader van genetica: biografie, experimenten en feiten
- Noem de externe spijsverteringsklieren geassocieerd met het systeem van mensen?
- Waarom voeren wetenschapper investagaties uit?
- Wat is microtoxine?
- Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden
- Hoe MRNA van een cel te isoleren
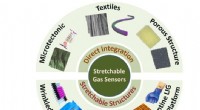
- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
- Na 150 jaar, een doorbraak in het begrijpen van de omzetting van CO2 naar elektrobrandstoffen

- Microdeeltjes gecreëerd door een nieuwe 3D-fabricagemethode kunnen lang na injectie medicijnen of vaccins vrijgeven

- Zeemosselen zijn een model voor het verbeteren van kracht, rekbaarheid en hechting in hydrogels voor wondgenezing

- Van één uur tot één minuut:nieuwe analysetechniek vereenvoudigt het proces om bisfenol A-verontreinigingen te detecteren

 Een mariene microbe zou een steeds belangrijkere rol kunnen spelen bij het reguleren van het klimaat
Een mariene microbe zou een steeds belangrijkere rol kunnen spelen bij het reguleren van het klimaat Adiabatische processen: definitie, vergelijking en voorbeelden
Adiabatische processen: definitie, vergelijking en voorbeelden  Hoe de angstaanjagende evacuaties van de Twin Towers op 9/11 hielpen de wolkenkrabbers van vandaag veiliger te maken
Hoe de angstaanjagende evacuaties van de Twin Towers op 9/11 hielpen de wolkenkrabbers van vandaag veiliger te maken Uit onderzoek blijkt dat afvalenergiecentrales een laag gezondheidsrisico vormen
Uit onderzoek blijkt dat afvalenergiecentrales een laag gezondheidsrisico vormen  Slechte E. coli kennen we, maar goede coli?
Slechte E. coli kennen we, maar goede coli?  Nieuwe bevindingen kunnen wetenschappers helpen bij het temmen van schadelijke hitte-uitbarstingen in fusiereactoren
Nieuwe bevindingen kunnen wetenschappers helpen bij het temmen van schadelijke hitte-uitbarstingen in fusiereactoren Hoe DNA-bewijs werkt
Hoe DNA-bewijs werkt  Onderzoekers ontwikkelen nieuwe theoretische benadering om licht te manipuleren
Onderzoekers ontwikkelen nieuwe theoretische benadering om licht te manipuleren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

