Wetenschap
Waarom combineert zilvernitraat eerst met chloride -ionen in water en niet K2CRO4?
Dit is waarom:
* Oplosbaarheid: Oplosbaarheid verwijst naar de maximale hoeveelheid van een stof die kan oplossen in een bepaald oplosmiddel bij een specifieke temperatuur.
* Vorming van neerslag: Wanneer de oplosbaarheid van een stof wordt overschreden, gaat deze uit de oplossing als een vaste stof.
* Relatieve oplosbaarheid: AGCL is praktisch onoplosbaar in water (zeer lage oplosbaarheid), terwijl Ag₂cro₄ enigszins oplosbaar is (wat betekent dat een kleine hoeveelheid oplost).
In een oplossing die zowel Cl⁻- als Cro₄²⁻ -ionen bevat, gebeurt het volgende:
1. Agno₃ dissocieert: Agno₃ lost op in water, waardoor Ag⁺ en No₃⁻ ionen worden vrijgeeft.
2. Agcl -vorming: De Ag⁺ -ionen reageren onmiddellijk met Cl⁻ -ionen, waardoor vaste agcl vormt, die uit oplossing neerslaat vanwege de extreem lage oplosbaarheid.
3. Ag₂cro₄ Formatie: De resterende Ag⁺ -ionen zullen dan reageren met Cro₄²⁻ ionen om Ag₂cro₄ te vormen. Omdat Ag₂cro₄ echter enigszins oplosbaar is, zal een kleine hoeveelheid oplossen en in oplossing blijven, terwijl de rest neerslaat.
Daarom vormt AGCL eerst omdat de lage oplosbaarheid de reactie op voltooiing drijft, waardoor Ag⁺ -ionen effectief worden verwijderd van de oplossing en de vorming van significante hoeveelheden Ag₂cro₄. voorkomen.
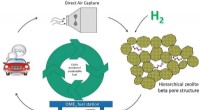
 Geconstrueerde bacteriële biofilms die nanodeeltjes immobiliseren, maken diverse katalytische toepassingen mogelijk
Geconstrueerde bacteriële biofilms die nanodeeltjes immobiliseren, maken diverse katalytische toepassingen mogelijk Wat zijn drie methoden om een chemische reactie te versnellen?
Wat zijn drie methoden om een chemische reactie te versnellen?  De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren
De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren Een blanco reactie treedt op wanneer een stof meestal koolstof bevat met zuurstof om energie te produceren in de vorm van warmte en licht?
Een blanco reactie treedt op wanneer een stof meestal koolstof bevat met zuurstof om energie te produceren in de vorm van warmte en licht?  Wanneer is Acid Black Cherry gecreëerd?
Wanneer is Acid Black Cherry gecreëerd?
 Lijst met kleine insecten
Lijst met kleine insecten Hittegolf Zuid-Australië breekt recordtemperaturen
Hittegolf Zuid-Australië breekt recordtemperaturen Slechts 10 riviersystemen dragen tot 95 procent bij aan plastic in oceanen
Slechts 10 riviersystemen dragen tot 95 procent bij aan plastic in oceanen  Heeft Californië iets geleerd van de laatste droogte? Gokken met water gaat door
Heeft Californië iets geleerd van de laatste droogte? Gokken met water gaat door Wat zijn drie soorten extreme omgevingen kunnen archaebacteriën overleven?
Wat zijn drie soorten extreme omgevingen kunnen archaebacteriën overleven?
Hoofdlijnen
- Wetenschappers hebben fundamentele ontdekkingen gedaan over de manier waarop eigenschappen van embryonale stamcellen worden gecontroleerd
- Wat is een groep weefsels met een gemeenschappelijke functie die wordt genoemd?
- Ideeën voor Cookie Science Fair Projects
- Ziekteproducerende bacteriën komen uit welk koninkrijk?
- Wat is de meest voorkomende chromosomale afwijking bij mensen?
- Wat zijn specifieke biotechnologietoepassingen voor DNA-vingerafdrukken?
- Waarom geloven wetenschappers dat virus geen levende organismen zijn?
- Is een amoeba beweeglijk of sessiel?
- Wetenschappers ontdekken hoe een groep rupsen giftig werd
 Team ontwikkelt nieuwe wiskundige vergelijking om cavitatie te voorspellen
Team ontwikkelt nieuwe wiskundige vergelijking om cavitatie te voorspellen Waarom gedragen leden van een gezinselementen hetzelfde in chemische reacties?
Waarom gedragen leden van een gezinselementen hetzelfde in chemische reacties?  De toekomst van de Amerikaanse beroepsbevolking zal afhangen van AI, maar tel menselijke werkers nog niet mee
De toekomst van de Amerikaanse beroepsbevolking zal afhangen van AI, maar tel menselijke werkers nog niet mee Acceleratie kan het beste worden omschreven als?
Acceleratie kan het beste worden omschreven als?  Hoe worden dinosaurussen fossielen?
Hoe worden dinosaurussen fossielen?  Zomerhitte te warm voor jou? Wat is comfortabel?
Zomerhitte te warm voor jou? Wat is comfortabel?  Wat is een zin die het woord microbiologie gebruikt?
Wat is een zin die het woord microbiologie gebruikt?  Wat gebeurt er met niet-polaire moleculen in water?
Wat gebeurt er met niet-polaire moleculen in water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com