
Wetenschap
Hoe kan een vaste stof in gas veranderen zonder door de liguid toestand te gaan?
Hier is hoe het werkt:
* sublimatie is een fase -overgang waarbij een vaste stof direct in een gas verandert zonder de vloeibare fase te passeren.
* Dit gebeurt wanneer de moleculen in een vaste winst voldoende energie wonen om los te komen van hun vaste posities en te ontsnappen in de gasvormige toestand.
* De energie die nodig is voor sublimatie wordt meestal geleverd door warmte of een vermindering van de druk.
Voorbeelden van sublimatie:
* droog ijs: Solid kooldioxide (CO2) sublimeert bij kamertemperatuur, waardoor een "mist" van CO2 -gas ontstaat.
* Mothballs: Deze zijn gemaakt van naftaleen, die langzaam sublimeert en een damp vrijgeeft die motten afstoot.
* bevroren water: In zeer koude en droge omgevingen kan ijs rechtstreeks in waterdamp sublimeren, wat leidt tot het fenomeen van sneeuw verdwijnt zonder te smelten.
Voorwaarden voor sublimatie:
* Lage druk: Sublimatie komt eerder op bij lagere drukken, omdat moleculen minder druk hebben die ze in de vaste toestand houden.
* Hoge temperatuur: Hogere temperaturen bieden meer energie voor moleculen om de krachten te overwinnen die ze in de vaste toestand houden.
* specifieke stoffen: Van sommige stoffen, zoals droogijs en jodium, staan erom bekend dat ze onder bepaalde omstandigheden gemakkelijk sublimeren.
Opmerking: Het omgekeerde sublimatieproces wordt depositie genoemd , waarbij een gas direct in een vaste stof verandert zonder de vloeibare toestand te passeren.
 Bij batterij een chemische reactie tussen welke twee metalen stroom produceerden?
Bij batterij een chemische reactie tussen welke twee metalen stroom produceerden?  Witte wijn, Combo met citroensap voorkomt ongewenste verkleuring van deeg
Witte wijn, Combo met citroensap voorkomt ongewenste verkleuring van deeg Nieuwe methode maakt gebruik van enantioselectieve nikkelkatalyse om multifunctionele chirale alkylboorverbindingen te synthetiseren
Nieuwe methode maakt gebruik van enantioselectieve nikkelkatalyse om multifunctionele chirale alkylboorverbindingen te synthetiseren  Worden opgewonden elektronen van het acceptormolecuul naar de elektronentransportketen gestuurd?
Worden opgewonden elektronen van het acceptormolecuul naar de elektronentransportketen gestuurd?  Hoe kom je erachter wat atoom heeft met alleen de elektronen?
Hoe kom je erachter wat atoom heeft met alleen de elektronen?
 Amazon-gemeenschap zet residuen om in hulpbronnen
Amazon-gemeenschap zet residuen om in hulpbronnen Wie geloofde dat er vuurbal was in de aarde?
Wie geloofde dat er vuurbal was in de aarde?  Hoe zeesneeuw de planeet afkoelt
Hoe zeesneeuw de planeet afkoelt Waren de oude Maya's een waarschuwend verhaal voor de landbouw? Misschien niet, suggereert een nieuwe studie
Waren de oude Maya's een waarschuwend verhaal voor de landbouw? Misschien niet, suggereert een nieuwe studie  Nieuwe indicator voor zuurstofniveaus in vroege oceanen ontwikkeld
Nieuwe indicator voor zuurstofniveaus in vroege oceanen ontwikkeld
Hoofdlijnen
- PITT-traject:Wetenschappers ontdekken hoe cellen een levensduurbevorderend 'recyclingsysteem' repareren
- "Recessive Allele: What is it?", 3, [[& Waarom gebeurt het? (met eigenschappenkaart)
- Welke twee structuren vormen een enkel gerepliceerd chromosoom?
- Hoe virussen werken
- Wat gebeurt er met planten en dierlijke cellen bij plaatsing in hypertonische, hypotone en isotone omgevingen?
- Beeldvorming met hoge resolutie geeft een ongeëvenaard beeld van hoe schimmels groeien
- Wie kreeg de eerste Nobelprijs voor biologie?
- De voor- en nadelen van grote oren voor vleermuissoorten
- Wat veroorzaakte het massale uitsterven van de eerste dieren op aarde?
- De kracht van honing door zijn eiwitten begrijpen

- Wetenschappers zorgen voor metingen met hoge resolutie voor koolstofdiplomatie

- Zichtbaar licht en nanodeeltjeskatalysatoren produceren gewenste bioactieve moleculen

- Een stap in de richting van het creëren van materialen gecontroleerd door kunstmatige genen
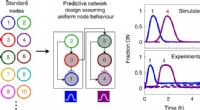
- Hygroscopische polymere gels:het verzamelen van zoet water en energie uit luchtvochtigheid
 Wat zijn vier soorten chimische reacties?
Wat zijn vier soorten chimische reacties?  E-mailen tijdens Zoom-vergaderingen? Nieuw onderzoek toont de voordelen aan van multicommunicatie op het werk, in de klas
E-mailen tijdens Zoom-vergaderingen? Nieuw onderzoek toont de voordelen aan van multicommunicatie op het werk, in de klas  Lekken zullen de afvang en opslag van koolstof niet doen zinken
Lekken zullen de afvang en opslag van koolstof niet doen zinken NASA's nieuwe Marsrover raakt stoffige rode weg, 1e reis 21 voet
NASA's nieuwe Marsrover raakt stoffige rode weg, 1e reis 21 voet Daimler roept meer auto's terug vanwege fraude met emissies:rapport
Daimler roept meer auto's terug vanwege fraude met emissies:rapport Afscheid van defecte software?
Afscheid van defecte software?  Onderzoeker ontdekt dat wanneer sperma concurreert, eieren hebben een keuze
Onderzoeker ontdekt dat wanneer sperma concurreert, eieren hebben een keuze Waarom is het zonlicht gratis goed?
Waarom is het zonlicht gratis goed?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

