
Wetenschap
Wat is de lading van radium?
Radium zelf is een neutraal element. radiumatomen kunnen echter ionen vormen met een lading van +2.
Dit is waarom:
* Radium (RA) bevindt zich in groep 2 van de periodieke tabel, wat betekent dat het 2 valentie -elektronen heeft (elektronen in de buitenste schaal).
* Om een stabiele elektronenconfiguratie te bereiken, verliest radium deze twee valentie -elektronen.
* Dit verlies van elektronen resulteert in een positief geladen ion, het radiumkation genoemd (ra²⁺).
Dus, hoewel radium als een neutraal element geen lading heeft, bestaat het meestal als een +2 ion in verbindingen.
 Californië heeft de afgelopen seizoenen de meeste regen gehad. Zet de trend zich voort in 2022?
Californië heeft de afgelopen seizoenen de meeste regen gehad. Zet de trend zich voort in 2022? Coronavirus:waarom we een einde moeten maken aan het pandemische verbod op herbruikbare bekers
Coronavirus:waarom we een einde moeten maken aan het pandemische verbod op herbruikbare bekers EPA verleent vrijstelling van vervuiling aan nutsbedrijven in Florida na Irma
EPA verleent vrijstelling van vervuiling aan nutsbedrijven in Florida na Irma NASA-gegevens helpen ozongaten op weg naar herstel
NASA-gegevens helpen ozongaten op weg naar herstel Matige tot sterke La Nina dit jaar:UN
Matige tot sterke La Nina dit jaar:UN
Hoofdlijnen
- Meer carrièremogelijkheden kunnen verklaren waarom minder vrouwen een baan in de wetenschap en wiskunde nastreven
- Onderzoek naar enzymatische chemische reacties kan erop wijzen hoe de eerste cellen kolonies vormden
- Wat is de betekenis van gentherapie?
- Waarom werkt natuurlijke selectie alleen aan fenotypes?
- Versteende cirkels in het zand aan de Zuid-Afrikaanse kust zijn mogelijk kunstwerken van onze vroege voorouders
- Wat is het verschil tussen bioloog en wetenschapper?
- De griezelige vraag van de vogelgriep:hoe miljoenen pluimvee te doden
- Fysieke aanpassingen van rondwormen
- Een wetenschapper vergelijkt gegevens van haar controlegroep en experimentele groep. Welke wetenschappelijke methode presteert ze?
- Raamwerkdiversiteit van koolstofnitrides biedt een rijk platform voor katalyse met één atoom

- Onderzoekers maken kunstmatig parelmoer met behulp van bacteriën

- Kalkoenborst met een lager natriumgehalte wint sensorische test dan volzoutoptie

- Is uw machine learning-trainingsset bevooroordeeld? Hoe nieuwe medicijnen te ontwikkelen op basis van samengevoegde datasets

- Wetenschappers tonen aan dat een veelbelovende vaste elektrolyt hydrofoob is
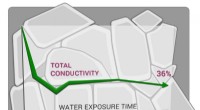
 Nieuw concept legt uit hoe kleine deeltjes door waterlagen navigeren, met implicaties voor het behoud van de zee
Nieuw concept legt uit hoe kleine deeltjes door waterlagen navigeren, met implicaties voor het behoud van de zee  Waarom kunt u geen breuken toevoegen met in tegenstelling tot noemers?
Waarom kunt u geen breuken toevoegen met in tegenstelling tot noemers?  Intel:Hot Chips-evenementdetails AI-krachtige processors
Intel:Hot Chips-evenementdetails AI-krachtige processors Ras, etnische minderheden worden kwetsbaarder voor bosbranden
Ras, etnische minderheden worden kwetsbaarder voor bosbranden Met Facebook-functie kunnen mensen hulp vragen bij een pandemie
Met Facebook-functie kunnen mensen hulp vragen bij een pandemie Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen
Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen Uit onderzoek blijkt dat de armen in de steden in de derde wereld politiek geëngageerd zijn
Uit onderzoek blijkt dat de armen in de steden in de derde wereld politiek geëngageerd zijn Hoe atoombrekers werken
Hoe atoombrekers werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

